治療規劃的制作方法
本發明尤其應用于輻射治療系統。系統。然而,應認識到,所描述的技術也可以應用于其他治療系統、其他輻射劑量控制情形,或其他輻射劑量遞送技術。
背景技術:
輻射處置常常被應用于隨著患者呼吸移動的腫瘤。通常,在輻射治療規劃期間定義目標體積,使得目標在全部運動相位中被覆蓋。該方法輻照顯著量的健康組織。例如,通用的基于群體的邊緣能夠被用于在運動存在時確保目標劑量。因此,圍繞目標的正常組織可能接收不必要的劑量,從而導致處置之后的差的患者結果和降低的生活質量。常規的靜態規劃目標體積(PTV)被創建,從而涵蓋目標的全部量化位置(例如,如從CT掃描等確定的)。因此,在常規處置遞送期間的任何給定時間點處,顯著量的正常組織接收不必要的劑量。
在外部射束輻射治療(EBRT)中的處置規劃通常為一次性的過程,跟隨其處置在多個分段上被遞送。一些系統提供使用來自目標的實時跟蹤信息以及估計一個或多個運動參數以量化該運動的功能。在這些處置遞送分段之間以及期間的目標運動妨礙如規劃地遞送處置的能力。
本申請涉及一種新的且改進的系統和方法,其通過提供實時目標體積跟蹤,克服了在處置期間的輻照健康組織和患者運動的問題,其克服了上述問題及其他問題。
技術實現要素:
根據一個方面,一種減少對目標體積附近的健康組織的輻射劑量的方法,包括:生成針對在4D運動模型中識別的所述目標體積的多個運動相位中的每個的動態規劃目標體積,所述4D運動模型是在計算機斷層攝影(CT)數據采集期間通過跟蹤目標體積的運動生成的,其中,所述運動相位是根據從所采集的CT數據重建的一幅或多幅CT圖像識別的。此外,所述方法包括在處置階段期間跟蹤所述目標體積;并且在所述目標體積的每個運動相位處:選擇對應于所述運動相位的動態PTV以覆蓋所述目標體積;并且輸出用于在所述目標體積的每個運動相位處輻照所選擇的動態PTV的指令。
根據另一方面,一種便于減少對目標體積附近的健康組織的輻射劑量的治療規劃系統,包括:跟蹤模塊,其使用從所述目標體積的所采集的CT掃描數據重建的一幅或多幅4D計算機斷層攝影(CT)圖像來跟蹤目標體積運動。所述系統還包括處理器,所述處理器被配置為:使用由所述跟蹤模塊生成的跟蹤信息,來生成針對所述目標體積的4D運動模型;并且生成針對在所述運動模型中識別的所述目標體積的多個運動相位中的每個的動態規劃目標體積(PTV)。此外,所述系統包括:運動估計工具,其被配置為跟蹤所述目標體積。所述處理器還被配置為,在所述目標體積的每個運動相位處:選擇對應于所述運動相位的動態PTV,以覆蓋所述目標體積;并且輸出用于在所述目標體積的每個運動相位處輻照所選擇的動態PTV的指令。
根據另一方面,一種減少對目標體積附近的健康組織的輻射劑量的方法,包括:向運動估計工具提供來自所述目標體積的4D運動模型的跟蹤目標體積位置信息;并且將從所述運動估計工具輸出的運動參數信息鏈接到由CT掃描數據指示的所述目標體積的運動相位。所述方法還包括:生成在每個運動相位中覆蓋所述目標體積的動態規劃目標體積(PTV);將針對每個運動相位的所述動態PTV鏈接到針對每個各自的運動相位的跟蹤運動參數;并且輸出用于輻照針對每個運動相位的PTV的指令。
一個優點在于,對健康組織的輻射劑量被減少。
另一優點在于,對目標體積的期望輻射劑量被實現。
本領域普通技術人員在閱讀并理解了以下詳細描述后,應認識到本發明的另外的優點。
附圖說明
本發明可以采取各種部件和各部件的布置的形式,并且可以采取各種步驟和各步驟安排的形式。附圖僅是出于圖示優選實施例的目的而不應被解釋為對本發明的限制。
圖1圖示了根據本文描述的一個或多個方面的用于在外部射束輻射治療(EBRT)期間減少對健康組織的輻射劑量的工作流程。
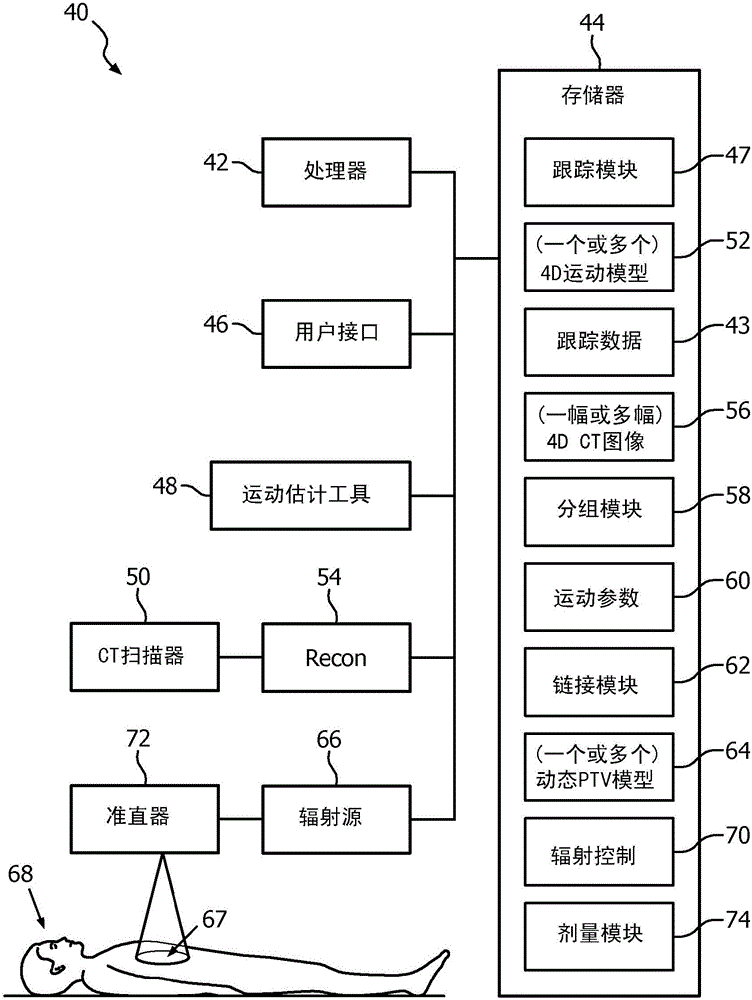
圖2圖示了根據本文描述的一個或多個方面的便于減少對正常組織的輻射劑量的系統。
圖3圖示了根據本文描述的一個或多個方面的用于減少對圍繞規劃目標體積的正常組織的劑量的方法。
圖4圖示了根據本文描述的一個或多個方面的,由超越模擬、處置規劃和處置遞送的新穎方法/工作流程實現的,用于減少對正常組織的輻射劑量的方法。
圖5圖示了根據本文描述的一個或多個方面的,使用實時跟蹤、對4D CT相位的一對一映射,以及用于沿軌跡跟蹤目標體積(虛線卵形)的運動預測的動態變化的PTV(實線卵形)。
圖6圖示了根據本文描述的一個或多個方面的,使用實時跟蹤、對4D CT相位的多對一映射,以及運動預測的動態變化的PTV(實線卵形)。
具體實施方式
本發明通過采用實時目標體積跟蹤(其使用目標位置對運動狀態的映射),克服了對目標體積附近的健康組織的非期望的輻照的上述問題。在輻射治療規劃期間,目標體積針對每個運動狀態被定義。在治療期間,跟蹤患者運動并且確定當前運動狀態。使用查找表等,針對當前運動相位的治療規劃被確定。輻射源控制模塊通過控制被定位在輻射源與患者之間的準直器來操縱治療射束,并且劑量模塊調制射束以如由針對當前運動相位的處置規劃指示地控制劑量。本文中使用的“目標體積”指代要被輻照(或使用粒子治療或任何其他適當的治療類型消融、處置)的腫瘤或團塊,并且“規劃目標體積”或“PTV”指代覆蓋或涵蓋目標體積的體積。盡管系統和方法在本文中參考輻射治療規劃等被描述,但是本領域技術人員應認識到,這樣的系統和方法也可應用于其他治療類型,包括但不限于,消融治療、粒子治療,或任何其他適當類型的治療。
圖1圖示了根據本文描述的一個或多個方面的用于在外部射束輻射治療(EBRT)期間減少對健康組織的輻射劑量的工作流程10。工作流程包括三個主要階段,包括模擬階段12、處置規劃階段14以及遞送階段16。模擬階段12包括跟蹤步驟18,其中,在4D運動研究中跟蹤目標(例如腫瘤等)位置。在一個實施例中,在18處執行電磁(EM)跟蹤。運動估計工具20a(例如遞送劑量調查工具(DiDIT),諸如被提供在Philips的Pinnacle3系統等中)被用于生成參數化數據集22a,所述參數化數據集包括例如目標體積在運動期間的平移、旋轉、比例、變形向量等。4D計算機斷層攝影(CT)掃描器24采用參數化集合數據22a,并且在處置規劃階段14中,在26處定義動態規劃目標體積(PTV)。在處置遞送階段16中,在28處實時執行目標體積跟蹤,以在輻射遞送期間跟蹤目標位置。在一個實施例中,EM跟蹤被用于跟蹤目標體積。運動估計工具20b被用于生成參數化集合數據22b。運動估計工具20b可以相似或相同于運動估計工具20a。在30處,基于參數化集合數據22a、參數化集合數據22b以及在26處定義的動態PTV,來動態選擇并處置PTV。以這種方式,與輻照由移動的PTV穿過的整個體積的常規方法相比,所描述的工作流程10便于輻照在多個不同PTV位置處的移動的PTV,以便將對圍繞PTV的健康組織的輻射劑量最小化。
將認識到,本文描述的DiDIT運動估計工具是通過范例來提供的,并且所描述的系統和方法不限于此。所描述的運動估計工具20a、20b能夠前瞻性地(在模擬期間)并且在處置遞送期間被利用以參數化目標運動,以及回顧性地被利用。
圖2圖示了根據本文描述的一個或多個方面的便于減少對正常組織的輻射劑量的系統40。所述系統包括可操作地被耦合到存儲器44和用戶接口46的處理器42。處理器42運行用于執行本文描述的各種功能、方法、流程等的計算機可執行指令(例如,例程、程序、算法、軟件代碼、模塊等),并且存儲器44存儲所述計算機可執行指令。額外地,本文使用的“模塊”指代一組計算機可執行指令、軟件代碼、程序、例程,或用于執行所描述的功能的其他計算機可執行單元等,其被存儲在計算機可讀介質上和/或由一個或多個處理器運行,如本領域技術人員將理解的。
存儲器可以為在其上存儲控制程序的計算機可讀介質,諸如磁盤、硬盤驅動等。非易失計算機可讀介質的常見形式例如包括軟盤、柔性磁盤、硬盤、磁帶或任何其他磁性存儲介質,CD-ROM、DVD或任何其他光學介質,RAM、ROM、PROM、EPROM、FLASH-EPROM,它們的變體,其他存儲器芯片或盒,或處理器能夠從其讀取和運行的任何其他有形介質。在該背景下,本文中描述的系統可以被實施在以下上或被實施為以下:一個或多個通用計算機、(一個或多個)專用計算機、編程微處理器或微控制器以及外周集成電路元件、ASIC或其他集成電路、數字信號處理器、硬連線電子或邏輯電路(諸如,分立元件電路)、可編程邏輯設備(諸如,PLD、PLA、FPGA、圖形卡CPU(GPU)或PAL)等。
系統40還包括在CT掃描期間跟蹤目標體積位置的跟蹤模塊47,以及在CT掃描器50中的運動估計工具48。處理器42使用由跟蹤模塊47生成的運動跟蹤數據53,在模擬期間生成患者中的目標體積(例如腫瘤等)的4D運動模型52。由運動估計工具采用的跟蹤技術的范例包括但不限于植入式無線電磁(EM)跟蹤器、表面跟蹤(使用光學形狀感測或高頻攝像機)、外部基準跟蹤(使用高頻攝像機)、內部解剖標記物跟蹤(使用連續透視法)等。重建處理器54將由CT掃描器50采集的CT掃描數據重建為目標體積的4D CT圖像56(第4維為時間)。處理器運行分組模塊58,所述分組模塊將4D CT圖像分組為N個運動相位或位置,其中,N為整數。運動估計工具48(例如,DiDIT或任何其他適當的運動估計工具)計算針對目標體積的每個被跟蹤的位置的運動參數60(因此,目標體積和/或PTP的例如平移、旋轉、縮放因數、可變形向量場等)。
處理器運行鏈接模塊62,所述鏈接模塊將運動參數鏈接到4D CT數據集中的目標體積的特定相位或位置N。這能夠使用來自所記錄的跟蹤數據和CT圖像56的時間信息來執行。也能夠使用其他配準技術,諸如將跟蹤數據波形配準到對從CT圖像分析獲得的目標運動的估計。在一個實施例中,通過在模擬期間以延長的時間段監測患者,從而捕獲大量的數據點,來構成4D運動模型52。在該過程期間,能夠令患者執行罕見的但在治療遞送期間可能發生的不平常的任務(例如咳嗽、深呼吸、淺呼吸等)。
在處置規劃階段期間,處理器生成一個或多個動態PTV模型64。在一個實施例中,通過鏈接模塊62將來自運動估計工具的運動參數輸出60的每個集合鏈接到4D CT數據集的唯一相位或位置(一對一映射)。在這種情況下,運動估計工具的每個輸出集合被分配唯一的PTV 64,所述唯一的PTV被繪制在4D CT數據集中的對應的相位上(例如參見圖5)。該方法采用時間密集的4D CT數據集。在另一實施例中,來自運動估計工具的多個輸出集合由鏈接模塊62鏈接到4D CT數據集中的給定相位(多對一映射)。在這種情況下,運動估計工具的多個運動參數輸出集合被分配公共PTV,所述公共PTV被繪制在那些輸出對應于的4D CT數據集的相位上(例如參見圖6)。在這種方法下,4D CT數據集能夠相對稀疏(例如,10個相位或特定其他預先確定數量的相位)。盡管本文描述的4D數據集如是從CT掃描數據和/或圖像生成的,但是應認識到,任何適當的成像模態能夠與所描述的治療規劃系統和方法結合被采用,所述任何適當的成像模態包括但不限于,例如超聲、磁共振(MR)、核成像模態(諸如正電子發射斷層攝影(PET)、單光子發射計算機斷層攝影(SPECT))、X射線、xCT,前述這些的變體等。
在處置遞送階段期間,輻射源66(例如線性加速器等)被提供有指令,以在輻射劑量遞送期間使用由運動估計工具48提供的實時跟蹤信息,向患者68中的動態變化的PTV 67遞送輻射劑量。在一個范例中,模擬相位期間使用的跟蹤模態也在處置遞送期間被連續地被利用(例如EM跟蹤、透視影片等)。基于對運動估計工具中的進入跟蹤數據的實時分析,在模擬期間創建的4D運動模型52和與在處置規劃階段期間生成的動態PTV模型64有關的信息被用于確定在何者時間或相位處使用何者PTV邊緣。輻射控制模塊70由處理器運行,并且采用一個或多個運動預測算法來確定多葉準直器(MLC)葉片位置并且在劑量遞送期間控制準直器72,以便輻照在目標體積運動的每個相位處的PTV,同時減少對目標電話附近的健康組織的輻射劑量。額外地,劑量模塊74能夠由處理器運行以調制輻射源射束,從而進一步控制輻射劑量。例如,如果患者在處置遞送期間咳嗽,則目標體積將偏離其正常路徑:4D運動模型能夠被用于估計將由目標體積穿過的位置,以返回其“正常”或預期路徑。基于該信息,提前選擇針對那些時刻的適當的PTV,并且準直器72被控制以在給定時刻處向PTV的所述位置遞送輻射。
以這種方式,使用在模擬和處置遞送期間的實時跟蹤,所描述的系統和方法減少對正常組織的劑量。所描述的方法能夠被實施在Pinnacle3中,例如使用Pinnacle3的運動估計功能(DiDIT)。可以使用電磁(EM)跟蹤、對外部身體表面的光學形狀感測(OSS)、高頻攝像機等來實現實時跟蹤,它們都不會將患者暴露于額外的輻射劑量。
繼續參考圖1和圖2,圖3圖示了根據本文描述的一個或多個方面的用于減少對圍繞規劃目標體積的正常組織的劑量的方法。所述方法能夠由計算機和/或處理器42(圖2),結合存儲器44(圖2)和用戶接口46(圖2)和/或圖1和/或圖2的任何其他適當的部件來運行。
在80處,在模擬相位期間使用跟蹤技術和4D CT圖像針對目標創建4D運動模型。在82處,跟蹤目標位置被饋送到運動估計工具(例如Pinnacle3的DiDIT,其依據相對于參考位置的平移和旋轉將目標位置參數化)。在84處,運動估計工具的參數化輸出被鏈接到4D CT相位。在86處,在處置規劃期間生成動態PTV。例如,動態PTV在4D CT相位的每個上被創建。在88處,基于在80處創建的4D運動模型,動態PTV被鏈接到跟蹤目標運動參數,并且輻照規劃(例如計算機可執行指令等)被輸出,例如到輻射源控制器等。在90處,在遞送期間使用實時跟蹤信息向動態PTV遞送輻射劑量。對目標的實時跟蹤和4D CT運動模型被用于根據遞送時間確定要使用何者PTV。
圖4圖示根了據本文描述的一個或多個方面的,由超越模擬、處置規劃和處置遞送的新穎方法/流程實現的,用于減少對正常組織的輻射劑量的方法。所述方法能夠由計算機和/或處理器42(圖2),結合存儲器44(圖2)和用戶接口46(圖2)和/或圖1和/或圖2的任何其他適當的部件來運行。
在110處,在模擬期間使用運動跟蹤針對目標體積(例如腫瘤或病變等)創建4D運動模型。跟蹤技術的范例包括但不限于植入式無線電磁(EM)跟蹤器、表面跟蹤(使用光學形狀感測或高頻攝像機)、外部基準跟蹤(使用高頻攝像機)、內部解剖標記物跟蹤(使用連續透視法)等。在112處,目標體積的4D CT圖像被獲得并被分組為N個相位,其中,N為整數。在114處,運動估計工具(例如DiDIT或任何其他適當的運動估計工具)計算針對目標體積的每個被跟蹤的位置的運動參數(例如平移、旋轉、縮放因子、可變形向量場等)。在116處,來自運動估計工具的參數化輸出集合被存儲在存儲器或數據庫中,并且被鏈接到4D CT數據集的特定相位N。這能夠使用來自所記錄的跟蹤數據和CT圖像的時間信息來執行。也能夠使用其他配準技術,諸如將跟蹤數據波形配準到從CT圖像分析獲得的對目標運動的估計。通過在模擬期間以延長的時間段監測患者,從而捕獲大量數據點,來構成4D運動模型。在該過程期間,令患者執行罕見的但在治療遞送期間可能發生的不平常的任務(例如咳嗽、深呼吸、淺呼吸等)。所述方法的模擬相位因此包括動作110、112、114和116,但不限于此。
在118處,在處置規劃階段期間生成動態PTV。在一個實施例中,來自運動估計工具(例如,DiDIT)的參數輸出的每個集合被鏈接到4D CT數據集上的唯一相位(一對一映射)。在一對一映射的情況下,運動估計工具的每個輸出集合被分配唯一的PTV,所述唯一的PTV被繪制在4D CT數據集的對應相位上(例如參見圖5)。該方法采用時間密集的4D CT數據集。
在另一實施例中,來自運動估計工具(例如DiDIT)的多個輸出集合被鏈接到4D CT數據集上的給定相位(多對一映射)。在多對一映射的情況下,運動估計工具的多個輸出集合被分配公共PTV,所述公共PTV被繪制在那些輸出對應于的4D CT數據集的相位上(例如,參見圖6)。在這種方法下,4D CT數據集能夠相對稀疏(例如,10個相位或特定其他預先確定數量的相位)。
在120處,在遞送期間使用實時跟蹤信息向動態變化的PTV遞送輻射劑量。在一個范例中,模擬相位期間使用的跟蹤模塊也在處置遞送期間被連續利用(例如,EM跟蹤、透視影片等)。基于對運動估計工具中的進入跟蹤數據的實時分析,在模擬期間(在110處)創建的4D運動模型和在處置規劃階段期間(在118處)生成的動態PTV被用于確定在何者時間處使用何者PTV邊緣。在122處,運行一個或多個運動預測算法以預測遞送期間的多葉準直器(MLC)葉片位置。例如,如果患者在處置期間咳嗽,則目標體積將偏離其正常路徑:4D運動模型能夠被用于估計將由目標體積穿過的位置,以返回其“正常”或預期路徑。基于該信息,提前選擇針對那些時刻的適當的PTV,并且控制準直器以在給定時刻處向PTV的所述位置遞送輻射。
將理解,本文描述的范例盡管涉及輻射治療,但是不限于此。相反地,所描述的系統和方法應用于任何治療規劃和/或遞送類型,例如包括消融治療、粒子治療等。
圖5圖示了根據本文描述的一個或多個方面的,使用實時跟蹤、對4D CT相位的一對一映射以及用于沿軌跡跟蹤目標體積142(虛線卵形)的運動預測的動態變化的PTV 140(實線卵形)。目標體積運動的相位然后被用于控制輻射源和準直器在沿軌跡的每個位置或相位處向圍繞目標體積142的PTV 140遞送輻射劑量,而不是如常規地輻照涵蓋全部目標體積位置的一個大的總PTV 144。以這種方式,對圍繞目標體積的健康組織的輻射劑量被減少。
圖6圖示了根據本文描述的一個或多個方面的,使用實時跟蹤、對4D CT相位的多對一映射,以及運動預測的動態變化的PTV 160(實線卵形)。目標體積運動的相位然后被用于控制輻射源和準直器在沿軌跡的每個位置或相位處向圍繞目標體積162(虛線卵形)的PTV 160遞送輻射劑量,而不是如常規地輻照涵蓋全部目標體積位置的一個大的總PTV。以這種方式,對圍繞目標體積的健康組織的輻射劑量被減少。
已經參考若干實施例描述了本發明。他人在閱讀和理解了前文的詳細描述后,可以實現修改和變化。本發明旨在被解釋為包括所有這樣的修改和變化,只要其落入權利要求書或其等價方案的范圍內。
- 還沒有人留言評論。精彩留言會獲得點贊!