抗菌肽與抗生素組合抗菌藥物及其使用方法與流程
本發明屬于生物醫藥領域,主要涉及一種抗菌肽與抗生素組合的抗菌藥物及其使用方法。
背景技術:
抗生素是用于預防和治療細菌感染的藥物。抗生素的出現,拯救了無數生命,但是細菌對于抗生素產品的耐藥性問題也逐年加重,新藥研發的速度遠跟不上細菌耐藥的速度,抗生素耐藥性會導致更高的醫療費用,更長的住院時間和更多死亡。抗生素耐藥性是指引起感染的普通細菌所出現的對抗生素的耐藥性,它在細菌對使用該類藥物發生反應并改變時出現,一般是由于耐藥基因導致的這種變化。
據世界衛生組織報告,僅在歐盟地區,僅在2014年耐藥細菌估計就造成了25000例死亡,每年因此發生的衛生保健支出和生產力損失超過了15億美元。因此急需改變開處方和使用抗生素的方法。
在常見菌種如金黃色葡萄球菌對于抗生素的耐藥性日益嚴重的當今,生物體產生的抗菌肽類物質因其能夠在幾千年中仍保有殺菌抗菌作用而被選為抗菌藥物的后備軍。抗菌肽也稱為宿主防御肽,具有廣譜高效殺菌活性,對革蘭氏陰性菌、革蘭氏陽性菌、真菌、病毒及癌細胞等均具有強有力的殺傷作用,其作用機制包括抑制細菌細胞壁的合成、破壞細胞膜,激活自溶酶,抑制dna、rna和蛋白質的合成等。研究表明很少有細菌對抗菌肽有耐藥性,現在已經有一些抗菌肽在臨床上研究使用。
中國專利申請201410241068.9《抗菌肽抗菌活性預測方法及抗菌肽》中公開了人工設計的dp系列抗菌肽,其序列為v-q-w-r-i-r-x1-x2-v-i-r-x3,其中x1=i或v,x2=a或c,x3=a、r或k;或者:v-q-l-r-i-r-v-x4-v-i-r-x5,其中x4=a或c,x5=r或k。dp系列抗菌肽具有很好的廣譜抗菌活性,尤其是氨基酸序列為vqwrirvavirk(seqno.4)的dp7,對革蘭氏陽性菌、革蘭氏陰性菌、真菌具有很好的抗菌活性,并且對真核細胞具有較低的毒性以及較低的溶血效應。如何能進一步提高dp系列抗菌肽的抗菌活性,尤其是使使細菌更難產生耐藥性,以及對耐藥細菌具有更好的抗菌作用,是本領域的難題。
技術實現要素:
本發明要解決的技術問題是為本領域的抗感染治療提供一種新的有效選擇。本發明解決上述技術問題的技術方案是提供了一種抗菌藥物。該抗菌藥物包括抗菌肽與抗生素作為主要活性成分。
其中,上述抗菌藥物中所述的抗菌肽具有如下所示的氨基酸序列:
v-q-w-r-i-r-x1-x2-v-i-r-x3,其中x1=i或v,x2=a或c,x3=a、r或k;
或者:
v-q-l-r-i-r-v-x4-v-i-r-x5,其中x4=a或c,x5=r或k;
或者為上述序列多肽的碳末端進行了酰胺化和/或氮末端進行了乙酰化的衍生物中的至少一種。
進一步的,上述抗菌藥物中所述的抗菌肽的氨基酸序列選自序列表中seqidno.1~seqidno.16中的至少一條。
其中,上述抗菌藥物中所述的抗生素為糖肽類抗生素、氨基苷類抗生素、大環內脂類抗生素、β-內酰胺類抗生素中的至少一種。
其中,上述抗菌藥物中所述的β-內酰胺類抗生素為青霉素類抗生素或頭孢菌素類抗生素中的至少一種。
進一步的,所述的青霉素類抗生素為青霉素g、青霉素v、氟氯西林、苯唑青霉素、氨芐西林、羧芐西林、匹氨西林、磺芐西林、替卡西林、哌拉西林或阿莫西林中的至少一種。所述的頭孢菌素類抗生素為:頭孢羥氨芐、頭孢氨芐、頭孢唑啉、頭孢拉啶、頭孢丙烯,頭孢呋辛脂、頭孢克洛、頭孢孟多、頭孢噻肟、頭孢曲松、頭孢克肟、頭孢地尼、頭孢皮羅、頭孢吡肟或頭孢唑南中的至少一種。
其中,上述抗菌藥物中所述的氨基苷類抗生素為鏈霉素、慶大霉素、卡那霉素、妥布霉素、丁胺卡那霉素、新霉素、西索米星、妥布霉素、阿米卡星、奈替米星、核糖霉素、小諾霉素或阿斯霉素中的至少一種。
其中,上述抗菌藥物中所述的多肽類抗生素為萬古霉素、去甲萬古霉素、多粘菌素b或替考拉寧中的至少一種
其中,上述抗菌藥物中所述的大環內脂類抗生素為紅霉素、白霉素、無味紅霉素、依托紅霉素、乙酰螺旋霉素、麥迪霉素、交沙霉素或阿奇霉素中的至少一種。
進一步的,上述抗菌藥物的其劑型為注射劑。
其中,上述抗菌藥物中所述的抗菌肽與抗生素處于獨立的包裝中。
進一步的,上述抗菌藥物中所述的獨立包裝的抗菌肽的劑型為注射劑,抗生素的劑型為口服制劑或注射劑。
同時,本發明還提供了一種抗菌方法。該抗菌方法包括以下步驟:對于非生物物體或者帶菌生物體施用有效量的抗菌肽與抗生素,進行抗菌處理。
其中,上述的抗菌方法中抗菌肽具有如下所示的氨基酸序列:
v-q-w-r-i-r-x1-x2-v-i-r-x3,其中x1=i或v,x2=a或c,x3=a、r或k;
或者:
v-q-l-r-i-r-v-x4-v-i-r-x5,其中x4=a或c,x5=r或k;
或者;
為對上述氨基酸序列所示多肽的碳末端進行了酰胺化和/或氮末端進行了乙酰化的衍生物中的至少一種。
進一步的,上述方法中所述抗菌肽的氨基酸序列選自序列表中seqidno.1~seqidno.16中的至少一條。
其中,上述的抗菌方法中所述的抗生素為多肽類抗生素、氨基苷類抗生素、大環內脂類抗生素、β-內酰胺類抗生素中的至少一種。進一步的,各類抗生素的具體種類也如前所述。
其中,上述的抗菌方法中所述的抗菌肽和抗生素為同時或者分時施用。
其中,上述的抗菌方法中所述的抗菌肽和抗生素使用相同或不同的給藥途徑施用。
進一步的,當對生物體施用時,上述抗菌方法中所述抗菌肽和抗生素施用在生物體的體表和/或體內。
當施用在生物體的體表時,上述抗菌方法中可施用抗菌肽和抗生素在生物體的皮膚和/或毛發處,以用于皮膚和毛發的抗菌。
當施用在生物體的體表時,上述抗菌方法中也能施用抗菌肽和抗生素在生物體表的傷口和/或感染處。
上述抗菌方法中,所述的生物為人或非人的脊椎動物。
本發明開展抗菌肽與抗生素類藥物的聯合使用研究,以期使其達到協同抗菌作用。但是由于不同的藥物往往具有不同的抗菌機制,聯合用藥與單獨用藥相比雖然可能使細菌更難產生耐藥性,但是哪些藥物之間有可能產生協同作用是難以預期的。在大量工作的基礎上,本發明創造性地發現dp系列的抗菌肽和抗生素類藥物之間能較好的配合使用,且能進一步產生協同作用。
本發明的有益效果在于:本發明抗菌肽抗生素組合藥能可有效提高抗菌效果,降低藥物尤其是抗生素的使用劑量,減少毒副作用;同時本發明抗菌肽抗生素組合藥物,將抗菌肽與抗生素聯合使用可有效降低菌株的耐藥性,對耐藥菌的抗菌效果也有明顯的提升,試驗證明對已有的耐藥株也有良好的殺菌效果,為本領域提供了一種新的有效選擇。
附圖說明
圖1、聯合用藥的藥物在96孔板排版布局示意圖。其中的blank是僅有培養基的對照,control是加菌液的培養基,未加藥物的對照。
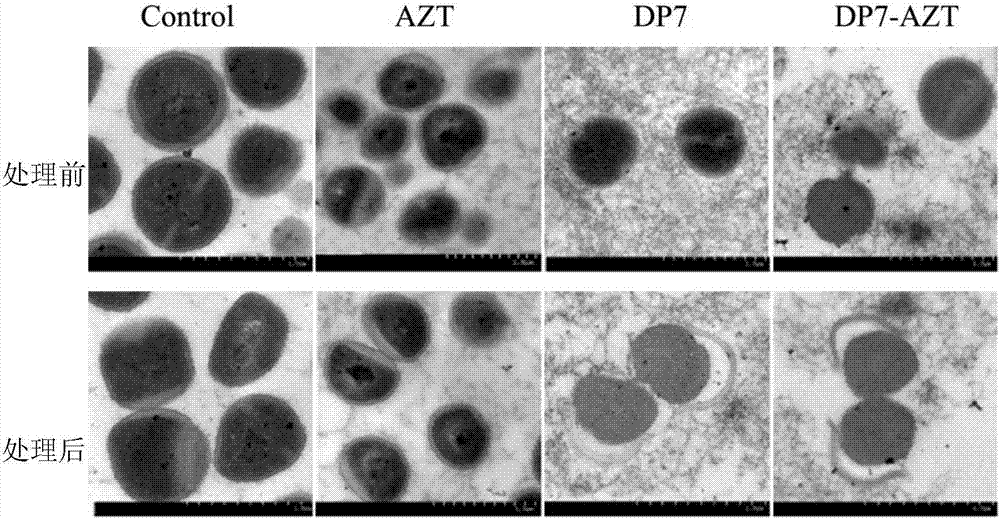
圖2、金黃色葡萄球菌耐藥株s5375經過不同藥物處理后細胞形態的透射電鏡圖。
具體實施方式
以下將結合附圖和實施例詳細說明本發明。
實施例1dp7與多種抗生素聯用對多種臨床分離耐藥菌的協同抗菌作用以及與cls001的協同抗菌效果比較:
將抗菌肽dp7(氨基酸序列vqwrirvavirk-nh2,碳末端進行了酰胺化)分別與抗生素藥物萬古霉素(van)、慶大霉素(gen)、阿奇霉素(azt)和阿莫西林(amo)用棋盤法進行藥物聯用抑菌實驗,并選取了重慶西南醫院和四川省疾控中心獲得的臨床分離耐藥金黃色葡萄球菌菌株(sau系列)、臨床分離耐藥大腸桿菌菌株(eco系列)、臨床分離耐藥綠膿桿菌菌株(paer系列)和臨床分離耐藥鮑曼不動桿菌菌株(aba系列)各三株用于聯合用藥效果測試。同時,本發明選取了目前處于臨床iii期評估階段的抗菌肽藥物omiganan(cls001,其氨基酸序列為ilrwpwwpwrrk(seqno.17),并在碳末端進行了酰胺化),代替dp7重復以上的聯合用藥抗菌實驗,以比較cls001和dp7的抗菌效果以及協同抗菌的效果。
1、抗菌肽與抗生素對于臨床分離耐藥菌的最小抑菌濃度測定
根據臨床和實驗室標準化協會(clsi)系列文件(m7-a7)指導,使用微量肉湯稀釋法測定抗菌藥物的最低抑菌濃度(mic)。主要操作方法如下:將細菌涂于mha平板,于37℃培養箱中生長24小時,然后挑取的菌落用mh肉湯系列稀釋至1×106cfu/ml,備用;藥物用mh肉湯進行等二倍系列稀釋,藥物濃度范圍從512mg/l到0.50mg/l,然后分別加入到96板相應的孔中,每孔加入100μl,每個藥物濃度有三個復孔;再向相應板孔中96孔板中加入100μl的5×106cfu/ml細菌;于37℃培養箱中培養20小時后,用酶標儀檢測od595波長下的吸光度值,三復孔測得的值取平均值,并計算抑菌率,以抑菌率大于或等于80%的抗菌藥物濃度作為其對這種細菌的mic值。抑菌率計算公式如下:
結果見表1,最小抑菌濃度實驗表明,大部分實驗用的各臨床分離耐藥菌菌株對慶大霉素和阿莫西林都具有非常嚴重的耐藥性,而阿奇霉素和萬古霉素對大部分菌株的抗菌效果也較差,抗菌肽dp7和cls001對所有菌株都有不錯的抗菌效果,就整體抗菌效果來說,dp7要稍微優于cls001。
表1.臨床分離菌株的mic
(金黃色葡萄球菌菌株、大腸桿菌菌株、綠膿桿菌菌株和鮑曼不動桿菌)
2、抗菌肽與抗生素聯用對臨床分離耐藥菌的協同抗菌作用
抗菌肽與抗生素聯合使用的部分抑菌濃度指數(ficis)是通過棋盤肉湯稀釋法測定mic后計算得來,可評價兩種藥物的體外協同抑菌效果。
抗菌肽與抗生素對于臨床分離耐藥菌的最小抑菌濃度(mic)測定的棋盤法的具體步驟如下:
(1)取需要聯用對抗菌藥物母液(10mg/ml),然后稀釋至4×2倍mic濃度,并配置2倍梯度稀釋藥液。
(2)按照棋盤法布局混合各個濃度的藥液:聯合用藥孔每孔加每種藥物50μl,當藥物孔加入藥物50μl,培養基50μl,每個藥物處理濃度設置二副孔。
(3)除blank孔,每孔加入100μl5×106cfu/ml的待試菌液。每孔的液體體積為200μl,blank孔只含200μl培養基。
(4)將96孔板放置于37℃細菌孵箱培養中,培養20小時后取出用酶標儀測量od595的值,計算各孔的抑菌率。
(5)聯合用藥的藥物在96孔板排版布局如圖1所示。
ficis的計算公式如下:
按照棋盤法布局混合各個濃度的藥液,取需要聯用對抗菌藥物母液(10mg/ml),然后稀釋至4×2倍mic濃度,并配置2倍梯度稀釋藥液。聯合用藥孔每孔加每種藥物50μl,單藥物孔(對應聯用藥0×mic)加入藥物50μl,培養基50μl,每個藥物處理濃度設置二副孔。除blank孔,每孔加入100μl5×106cfu/ml的待試菌液。每孔中液體中體積200μl,blank孔只含200μl培養基。
將96孔板放置于37℃細菌孵箱培養,培養20小時后取出用酶標儀測量od595的值,計算各孔的抑菌率,以抑菌率大于或等于90%的抗菌藥物濃度作為其對這種細菌的mic值。
結果見表2,在聯合抗菌實驗中,dp7與cls001這兩種抗菌肽的聯用對所有菌株都沒有發現協同作用(抑菌濃度指數fici≤0.5表明有協同作用)。抗菌肽dp7與萬古霉素聯用時,所有菌株中有50%的菌株具協同作用,與慶大霉素、阿奇霉素和阿莫西林聯用時有協同作用的菌株比例分別為20%、60%和20%。抗菌肽cls001與萬古霉素、慶大霉素、阿奇霉素和阿莫西林聯用時有協同作用的菌株比例分別為30%、20%、10%和40%。從整體的協同效果上看,dp7與抗生素聯用時的具有協同效果的聯合抗菌結果比cls001與抗生素聯用時的結果更多。而抗菌肽與抗生素萬古霉素和阿奇霉素聯用時具有更高的協同抗菌頻率。
表2.dp7或cls001與抗生素聯用的部分抑菌濃度指數ficis
注:部分抑菌濃度指數fici與協同作用關系:協同作用(fici≤0.5),部分協同作用(0.5<fici<1),無協同作用(1≤fici<4.0),拮抗作用(fici≥4.0)。
實施例2dp7與萬古霉素和阿奇霉素聯合抗菌的擴大實驗
抗菌肽dp7與萬古霉素和阿奇霉素聯用時,對于金黃色葡萄球菌臨床分離耐藥菌株和綠膿桿菌臨床分離耐藥菌株的協同抗菌具有更好的效果,因此我們擴大dp7與萬古霉素和阿奇霉素聯用抗菌實驗的金黃色葡萄球菌臨床分離耐藥菌和綠膿桿菌臨床分離耐藥菌的菌株數目以進一步研究協同抗菌效果。
采用實時定量pcr(qpcr)的方法確定臨床分離耐藥菌菌種的準確性。用dneasyblood&tissuekit(qiagen)提取細菌的總dna,dna濃度用thermoscientificnanodrop2000分光光度儀檢測,dna樣品的a260吸光度測定的濃度應大于10ng/ml,a260/a280值應大于1.8;用microbialdnaqpcrmulti-assaykits(qiagen)鑒定細菌萬古霉素耐藥基因和阿奇霉素耐藥基因;用qpcr軟件計算每個孔的臨界循環數(cq值),與陰性對照(ntc)的cq值相比,樣品cq值大于ntc-6的結果為陰性,小于ntc-6的結果為陽性。處于陽性和陰性之間的值為沒有顯著差異。根據cq值,確定臨床分離耐藥菌,然后進行聯合用藥實驗。
結果見表3,對于金黃色葡萄球菌臨床分離耐藥菌,抗菌肽dp7與萬古霉素聯用(dp7–van)有協同作用的占總菌株數量的40%,有部分協同作用的占40%;dp7與阿奇霉素聯用(dp7–azt)有協同作用的占總菌株數量的50%。對綠膿桿菌臨床分離耐藥菌,抗菌肽dp7與萬古霉素聯用有協同作用的占總菌株數量的50%,有部分協同作用的占20%;然而dp7與阿奇霉素聯用有協同作用的只占總菌株數量的10%,有部分協同作用的占30%。
表3.dp7、萬古霉素和阿奇霉素對金黃色葡萄球菌臨床分離
耐藥菌和綠膿桿菌臨床分離耐藥菌的mic以及聯合抗菌效果
實施例3dp7與阿奇霉素的協同作用與阿奇霉素耐藥基因之間的聯系
綜合dp7與阿奇霉素或萬古霉素聯用時的協同抗菌效果以及各菌株對阿奇霉素或萬古霉素的耐藥情況,我們采用實時定量pcr(qpcr)的方法,對金黃色葡萄球菌臨床分離耐藥菌和綠膿桿菌臨床分離耐藥菌進行了常見的萬古霉素耐藥基因和阿奇霉素耐藥基因的鑒定分析,本實施例涉及到的耐藥基因是萬古霉素耐藥基因(vanb、vanc)和阿奇霉素耐藥基因(erma,ermb,ermc,mefa,msra)。
結果見表4和表5、我們從qpcr基因鑒定結果得出,分離得到的金黃色葡萄球菌耐藥菌和綠膿桿菌臨床分離耐藥菌均沒有萬古霉素耐藥基因vanb和vanc(數據沒呈現)。針對于阿奇霉素耐藥基因,13株金黃色葡萄球菌臨床分離耐藥菌中有11株攜帶ermb基因,6株攜帶ermc基因(同時均攜帶ermb基因);9株綠膿桿菌臨床分離耐藥菌中有4株攜帶erma基因,6株攜帶ermb基因,6株攜帶ermc基因;這幾種金黃色葡萄球菌臨床分離耐藥菌和綠膿桿菌臨床分離耐藥菌均不攜帶mefa和msra基因。我們對這13株金黃色葡萄球菌臨床分離耐藥菌和9株綠膿桿菌臨床分離耐藥菌的耐藥性及耐藥基因種類數量的統計分析發現,阿奇霉素耐藥基因種類越多的菌株,其最低抑菌濃度(mic)越大;然而,絕大多數存在協同作用的耐藥菌株都含有兩種及以上的耐藥基因,阿奇霉素耐藥基因種類越多的菌株,其dp7與azt聯用的部分抑菌濃度指數(fici)越小,協同作用越好;這些結果表明dp7與阿奇霉素對于金黃色葡萄球菌臨床分離耐藥菌和綠膿桿菌臨床分離耐藥菌的協同抗菌作用可能與菌株的耐藥基因種類和數量有關。
表4.各個耐藥基因菌株在阿奇霉素耐藥菌中所占的比例
表5.耐藥基因在阿奇霉素耐藥菌的分布及dp7與阿奇霉素聯用的fici
注:“+”代表cq<ntc-6,鑒定為陽性;“-”代表cq≥ntc-6,鑒定為陰性。
實施例4金黃色葡萄球菌耐藥菌s5375被抗菌肽dp7與阿奇霉素處理后的形態學變化
本實例通過對藥物處理前后,通過透射電鏡來觀察細菌形態的變化,說明藥物對細菌殺傷的方式。
取對數生長期的金黃色葡萄球菌耐藥菌s5375,分組4組(control、dp7、dp7-azt、azt),然后每組用各自藥物處理60分鐘;900g離心10分鐘,獲得的沉淀有1m磷酸鹽緩沖液洗滌2次;然后2.5%戊二醛/磷酸鹽緩沖夜固定細胞,4度過夜;在透射顯微鏡下拍照。
結果見圖2,與control對照組相比,我們發現azt處理后的細胞顯示核區顏色變深暗和有清晰的細胞壁,dp7組處理后的細胞的細胞壁發生斷裂,dp7-azt組處理后的細胞壁斷裂程度比dp7更加嚴重。這些結果說明了dp7通過破壞細胞壁而殺菌,而azt可能是通過阻斷相關蛋白質合成而殺菌。兩者通過不同的機理達成了協同的效果。
- 還沒有人留言評論。精彩留言會獲得點贊!