哌甲酯前藥、其制備和使用方法與流程
相關申請本申請是針對于申請日為2012年7月27日、申請號為201280037735.0、發明名稱為“哌甲酯前藥、其制備和使用方法”的母案申請作出的分案申請,上述母案申請的內容以引入的方式并入本文中。本申請要求2011年7月28日提交的標題為methylphenidate-oxoacidconjugates,processesofmakingandusingthesame的美國臨時申請61/512,658的優先權權益,將其全部內容并入本申請作為參考。聯邦政府資助的研究或者開發[不適用]
背景技術:
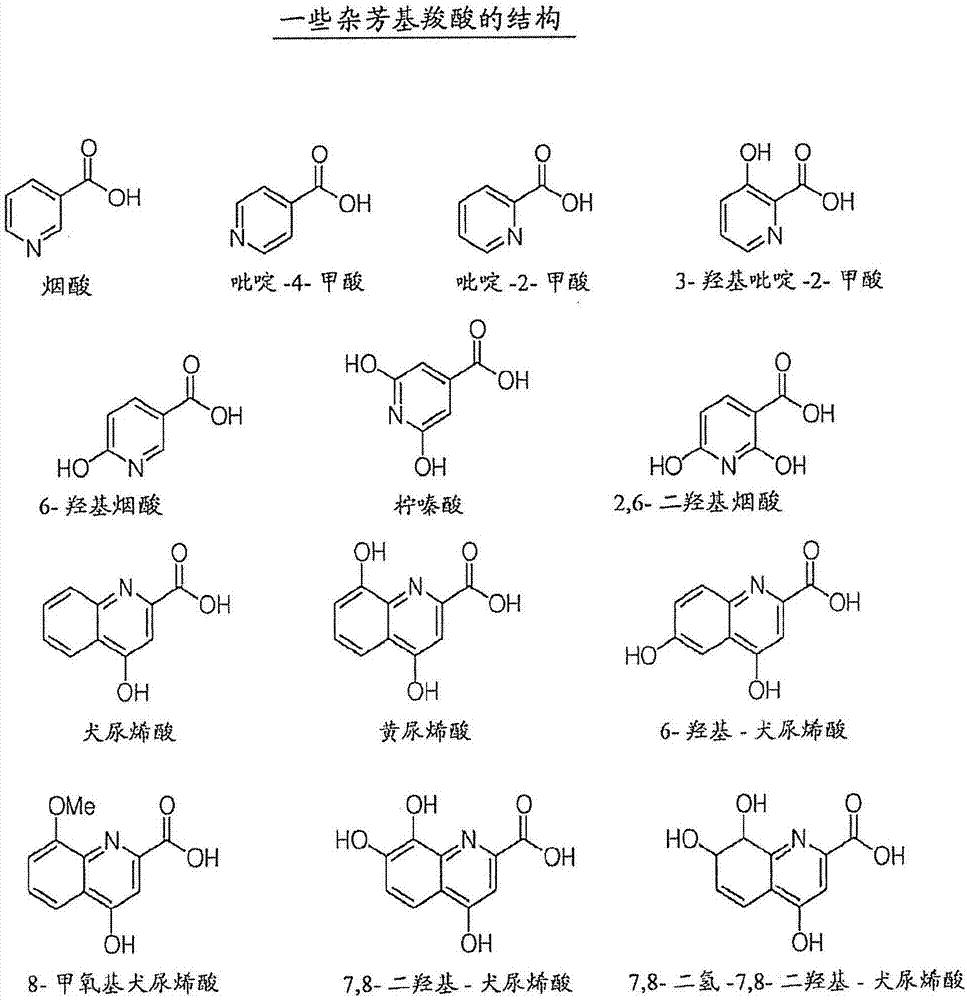
:哌甲酯(methylphenidate)為精神興奮藥,其為鏈取代的苯丙胺衍生物。類似于苯丙胺和可卡因,哌甲酯靶向中樞神經系統,具體為多巴胺轉運蛋白(dat)和去甲腎上腺素轉運蛋白(net)。哌甲酯被認為通過提高突觸間隙中的多巴胺和去甲腎上腺素的濃度來發揮作用,因為哌甲酯具有多巴胺轉運蛋白(dat)和去甲腎上腺素轉運蛋白(net)結合能力。盡管哌甲酯為苯丙胺衍生物,但是哌甲酯和苯丙胺的藥理學不同,因為苯丙胺為多巴胺轉運底物,而哌甲酯充當多巴胺轉運阻滯劑。作為去甲腎上腺素和多巴胺再攝取抑制劑,哌甲酯因此阻斷多巴胺和去甲腎上腺素(正腎上腺素)再攝取至突觸前神經元中(并且可能刺激多巴胺以高劑量從多巴胺神經末梢釋放),由此提高多巴胺和去甲腎上腺素在突觸中的水平。在一些體外研究中已經證實,與多巴胺相比,哌甲酯作為去甲腎上腺素攝取/再攝取的抑制劑更有效。然而,一些體內研究已經指出,與去甲腎上腺素濃度相比,哌甲酯在提高細胞外多巴胺濃度方面更有效。不同于苯丙胺,在科學和/或臨床研究團體中已經提出,在治療劑量哌甲酯似乎不顯著促進這兩種單胺神經遞質的釋放。已知存在哌甲酯的四種異構體:d-赤-哌甲酯、l-赤-哌甲酯、d-蘇-哌甲酯,和l-蘇-哌甲酯。最初,哌甲酯作為兩種外消旋物d/l-赤-哌甲酯和d/l-蘇-哌甲酯的混合物市售。隨后的研究顯示,該混合物的大部分藥理學活性與在分離的蘇-哌甲酯外消旋物的市售中得到的蘇-異構體相關。后來,科學界確定,d-蘇-異構體對于刺激活性負大部分責任。因此,開發了僅含d-蘇-哌甲酯(也稱為“d-蘇-mph”)的新產品。刺激物(包括哌甲酯(“mph”))被認為增強交感神經系統和/或中樞神經系統(cns)的活性。刺激物如mph及其各種形式和衍生物用于治療一系列病癥和障礙,其主要包括例如注意力缺陷伴多動癥(attentiondeficithyperactivitydisorder,adhd)、注意力缺陷障礙(attentiondeficitdisorder,add)、肥胖癥、發作性睡病、厭食、抑郁癥、焦慮癥和/或失眠癥。哌甲酯目前由美國食品和藥物管理局(“fda”)批準用于治療注意力缺陷伴多動癥和發作性睡病。哌甲酯對于一些核準標示外使用的適應癥(包括抑郁癥、肥胖癥和嗜睡)也顯示有效。在一些實施方案中,本發明技術的前藥可給藥用于治療注意力缺陷伴多動癥和發作性睡病,或者需要阻斷去甲腎上腺素和/或多巴胺轉運蛋白的任何病癥。兒童中的注意力缺陷伴多動癥(adhd)已經用刺激物治療了許多年。然而,最近,用于成年人中的adhd治療的處方數目的增加有時勝過兒科市場的增長。盡管目前具有多種用于治療adhd的藥物(包括一些刺激物和一些非刺激物藥物),但是哌甲酯(可從例如novartisinternationalag(位于basel,switzerland)在商標下商購)是常用的處方藥。而且,在課堂試驗中顯示,非刺激物在改善患有adhd的兒童的行為和注意力方面與苯丙胺衍生物相比效果較差。當藥效減弱時,通常在下午或者傍晚,在相當部分的患有adhd的兒童中觀察到行為惡化(反彈或者“崩潰”)。反彈癥狀包括例如應激性、偏執、與未給藥狀態相比惡化的活動過度、悲傷、哭泣,和在罕見的情況下的精神病發作。癥狀可快速平息或者持續數小時。一些患者可經歷嚴重的反彈/崩潰,以至于必須停止治療。通過誘使患者給藥額外劑量的刺激物以預防預期的反彈/崩潰負面結果和副作用,反彈/崩潰作用也可引起成癮行為。在現有技術中已經證實,刺激物如哌甲酯和苯丙胺呈現去甲腎上腺素能的和多巴胺能的效果,其可導致心血管事件,包括例如心率增快、高血壓、心悸、心動過速和在個別情況下的心肌病、中風、心肌梗塞和/或猝死。因此,目前可利用的刺激物將患有預先存在的心臟結構異常或者其它嚴重心臟適應癥的患者暴露于甚至更大的健康危險中,并且在這種患者群體中經常不使用或者謹慎地使用。哌甲酯如同其它刺激物和苯丙胺衍生物一樣,可變得上癮并易于物質濫用。已經報導了口服濫用,并且通過鼻內和靜脈內給藥可實現幸福愉快感。哌甲酯也具有有限的水溶性,尤其是以未結合形式。有限生物利用度和有限水溶性的性質使得配制用于口服給藥的哌甲酯更加困難,因為用于給藥的劑型受限。在本領域中需要生物利用度和水溶性更高的哌甲酯形式,其在給藥時,具體地,經口服途徑給藥時保持藥理學益處。技術實現要素:本發明技術使用例如哌甲酯、其各種形式和衍生物與某些醇、胺、含氧酸、硫醇或者它們的衍生物的共價結合,以提供例如與未結合的哌甲酯相比而言改善的生物利用度和提高的水溶性。提高的生物利用度和/或提高的水溶性在一些情況中提供以下能力:前藥或者組合物以未結合的哌甲酯不易使用的形式給藥。例如,所述綴合物與未結合的哌甲酯相比而言提高的水溶性提供以下能力:所述綴合物或者前藥以與未結合的哌甲酯相比而言具有較高劑量負載能力的口服薄膜或者條片的形式給藥。在一個方面,本發明技術提供前藥組合物,其包含至少一種綴合物,所述綴合物包含至少一種哌甲酯,和至少一種醇、胺、含氧酸、硫醇,或者它們的衍生物。在一些方面,前藥組合物還包含連接體,其中所述連接體使至少一種哌甲酯與至少一種醇、胺、含氧酸、硫醇或者它們的衍生物化學結合。在一些方面,連接體包含至少一個(酰基氧基)烷基氧基部分、其衍生物,或者其組合。在其它方面,本發明技術提供一種或者多種哌甲酯綴合物,所述哌甲酯綴合物包含哌甲酯、其衍生物或者它們的組合和至少一種醇、胺、含氧酸、硫醇或者它們的衍生物,其中所述至少一種含氧酸為羧酸。在另一方面,本發明技術提供至少一種前藥組合物,其包含哌甲酯、哌甲酯衍生物或者它們的組合和至少一種無機含氧酸或者具有游離-oh基團的無機含氧酸的衍生物、無機含氧酸的有機衍生物、無機含氧酸的無機衍生物或者它們的組合的至少一種綴合物。在又一方面,本發明技術提供至少一種前藥組合物,其包含哌甲酯、其衍生物或者它們的組合和醇、胺、含氧酸、硫醇或者它們的衍生物和連接體的至少一種綴合物,其中所述連接體包含具有通式-c(o)o-x-o-的(酰基氧基)烷基氧基、其衍生物或者它們的組合,其中x選自代表性基團,其包括任選取代的烷基、任選取代的芳基、任選取代的烷基芳基、任選取代的雜烷基、任選取代的雜芳基、任選取代的雜環基、任選取代的烯基、任選取代的炔基、任選取代的環烷基、任選取代的環烯基、任選取代的環炔基,或者任選取代的烷氧基。在另一方面,本發明技術提供前藥組合物,其包含至少一種具有式(i)或者式(ii)的結構的哌甲酯的綴合物:其中x選自o、s、se和nr1;其中y不存在或者選自o、s、se、nr2和cr3r4;其中r1和r2獨立地選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基羰基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、環烯基、環烯基烷基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基,和聚乙二醇基團;其中r3和r4獨立地選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基、氨基、氨基羰基、銨基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、氰基、環烯基、環烯基烷基、羧基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵素、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、硝基、氧代、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基、聚乙二醇基團和硫醇基;其中l不存在或者為-[-a-z-]-n;其中對于每個重復亞單元,a獨立地選自cr5r6、芳基、取代的芳基、亞芳基、碳環基、環烯基、環烷基、環炔基、雜環基和雜芳基;其中r5和r6彼此獨立地并且對于每個重復亞單元而言獨立地選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基、氨基、氨基羰基、銨基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、氰基、環烯基、環烯基烷基、羧基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵素、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、硝基、氧代、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基、聚乙二醇基團和硫醇基;其中z不存在或者對于每個重復亞單元而言獨立地選自o、s、se和nh;其中n為0-50;其中g對于每個重復亞單元而言獨立地選自醇、胺、氨基酸、銨、含氧酸、肽、聚(乙二醇)(peg)、硫醇,它們的衍生物和上述物質的組合;其中e為含氧酸;以及其中m為0-5。在另一方面,本發明技術提供至少一種前藥組合物,其包含至少一種綴合物,其中所述至少一種綴合物可為,例如,煙酸-ch2oco-哌甲酯、磷酸-ch2oco-哌甲酯、磷酸-ch2oco-哌甲酯、沒食子酸-ch2oco-哌甲酯、沒食子酸-ch2oco-哌甲酯、乳酸-ch2oco-哌甲酯、哌甲酯-co2ch2-煙酰基-asp、哌甲酯-co2ch2-煙酰基-val、哌甲酯-co2ch2-煙酰基-gly-ala、val-6-氨基己酸-ch2oco-哌甲酯、哌甲酯-co2ch2-煙酰胺、6-氨基己酸-ch2oco-哌甲酯、哌甲酯-co2ch2-煙酰基-otbu、哌甲酯-co2ch2-煙酸酯、哌甲酯-co2ch2-煙酰基-oet、哌甲酯-co2ch2-吡啶、異煙酸-ch2oco-哌甲酯,或者磷酸-(對-水楊酸)-ch2oco-哌甲酯。而且,本發明技術提供至少一種前藥組合物,其包含至少一種氨基甲酸氧基烷基酯。在又一方面,通過實施適當步驟以使哌甲酯與至少一個配體結合,本發明技術提供化學合成任何本發明技術的哌甲酯綴合物的方法。在其它方面,本發明技術的前藥組合物被認為意料不到地呈現與游離或者未修飾的哌甲酯相等的釋放速率。在其它方面,本發明技術的一種或者多種前藥組合物被認為令人驚訝地呈現與未修飾的哌甲酯相比隨時間推移較慢的釋放速率。在其它方面,本發明技術的綴合物或者前藥被認為意料不到地呈現與未修飾的哌甲酯相比在口服給藥時提高的吸收。另外,本發明技術的綴合物或者前藥被認為令人驚訝地具有與未修飾的哌甲酯相比提高的生物利用度。在其它方面,本發明技術的綴合物或者前藥被認為在口服藥代動力學(pk)分布方面令人驚訝地呈現與未結合的哌甲酯相比較少的患者間差異性。在又一方面,本發明技術的綴合物或者前藥以這樣的量提供:與未結合的哌甲酯相比,當以等摩爾劑量口服給藥時足以提供增加的auc。在其它方面,所述綴合物或者前藥以這樣的量提供:與未結合的哌甲酯相比,當以等摩爾劑量口服給藥時足以提供意料不到的增加的cmax。在其它方面,本發明技術的綴合物或者前藥以這樣的量提供:與未結合的哌甲酯相比,當以等摩爾劑量口服給藥時足以提供令人驚訝的增加的cmax和增加的auc。在可選擇方面,與未結合的哌甲酯相比,當以等摩爾劑量給藥時,本發明技術的綴合物或者前藥提供降低的副作用,并且還設想在一些可選擇方面提供與未結合的哌甲酯相比降低的濫用可能性。另外,本發明技術的綴合物或者前藥也被認為意料不到地提供與未結合的哌甲酯相比當以等摩爾劑量給藥時延長的t最大,和/或提供與未結合的哌甲酯相比當以等摩爾劑量給藥時相等的t最大。而且,本發明技術提供至少一種治療一種或者多種具有至少一種由控制、預防、限制或者抑制神經遞質攝取/再攝取或者激素攝取/再攝取介導的疾病、障礙或者病癥的患者(人或者動物)的方法,所述方法包括向一種或者多種患者口服給藥藥學有效量的至少一種本發明技術的前藥組合物。在其它方面,本發明技術提供至少一種治療具有至少一種需要刺激患者的中樞神經系統的障礙或者病癥的所述患者(人或者動物)的方法,所述方法包括口服給藥藥學有效量的一種或者多種本發明技術的前藥組合物。在又一方面,本發明技術提供一種或者多種給藥至少一種本發明技術的[哌甲酯]組合物或者前藥的方法,其中與未結合的哌甲酯相比,所述給藥減少產生的代謝物的數目和/或量。在其它方面,所述一種或者多種給藥一種或者多種本發明技術的[哌甲酯]組合物或者前藥的方法被認為與未結合的哌甲酯相比減少所述患者向利他林酸的暴露。在又一實施方案中,與未結合的哌甲酯相比,本發明技術的一種或者多種組合物或者前藥被認為提供基于哌甲酯的綴合物或者前藥的提高的水溶性。在另一實施方案中,提高的水溶性被認為允許前藥以比未結合的哌甲酯更高的濃度、劑量強度或者更高劑量負載能力形成某些劑型。在一些實施方案中,這種劑型包括,例如,口服薄膜或者條片。在又一實施方案中,與未結合的哌甲酯相比,一種或者多種基于哌甲酯的組合物或者前藥的給藥被認為提供哌甲酯血漿濃度的降低的患者間差異性,并且被認為具有改善的安全性分布。在又一可選實施方案中,本發明技術提供至少一種治療注意力缺陷伴多動癥的方法,其包括給藥藥學有效量的一種或者多種本發明技術的綴合物或者前藥組合物。在另一其它實施方案中,本發明技術提供至少一種前藥組合物,其用于治療至少一種具有需要刺激患者的中樞神經系統的障礙或者病癥的所述患者,其中與未結合的哌甲酯相比,所述至少一種前藥或者組合物在給藥時具有降低的濫用可能性。在另一實施方案中,與游離的未結合的哌甲酯相比,當以等摩爾量給藥時,本發明技術的一種或者多種基于哌甲酯的前藥或者綴合物組合物預期在通過腸胃外途徑給藥時呈現降低的或者抑制的藥理學活性,或者在通過鼻內、靜脈內、肌內、皮下或者直腸給藥時呈現降低的釋放的哌甲酯的血漿或者血液濃度。在又一實施方案中,本發明技術提供至少一種基于哌甲酯的綴合物前藥組合物,其與未結合的哌甲酯相比,當以等摩爾劑量口服給藥時具有延長的或者受控的通過釋放的哌甲酯的血漿濃度測量的釋放分布。在一些實施方案中,從前藥釋放的哌甲酯的血漿濃度將在口服給藥后更緩慢地和歷經較長時間地提高,從而導致與未結合的哌甲酯相比,釋放的哌甲酯的峰值血漿濃度的延遲和較長的作用持續時間。在另一方面,本發明技術提供藥物試劑盒,其包含在包裝中的指定量的單個劑量,所述單個劑量含有藥學有效量的至少一種哌甲酯綴合物。附圖說明圖1.用于制備本發明技術的綴合物的一些羥基苯甲酸類的化學結構。圖2.用于制備本發明技術的綴合物的一些雜芳基羧酸類的化學結構。圖3.用于制備本發明技術的綴合物的一些苯基乙酸類的化學結構。圖4.用于制備本發明技術的綴合物的一些芐基乙酸類的化學結構。圖5.用于制備本發明技術的綴合物的一些肉桂酸類的化學結構。圖6.用于制備本發明技術的綴合物的一些二羧酸類的化學結構。圖7.用于制備本發明技術的綴合物的一些三羧酸類的化學結構。圖8.用于制備本發明技術的綴合物的一些無機含氧酸的化學結構。圖9.用于制備本發明技術的綴合物的一些無機含氧酸衍生物的化學結構。圖10.用于制備本發明技術的綴合物的一些標準氨基酸類的化學結構。圖11.用于制備本發明技術的綴合物的一些非標準氨基酸類的化學結構。圖12.用于制備本發明技術的綴合物的一些合成氨基酸類的化學結構。圖13.在大鼠中比較煙酸-ch2oco-mph綴合物與未結合的哌甲酯的口服pk曲線。圖14.在大鼠中比較磷酸-ch2oco-mph綴合物(從三個研究組合的數據)與未結合的哌甲酯(從六個研究組合的數據)的口服pk曲線。圖15.在大鼠中比較磷酸-ch2oco-mph綴合物與未結合的哌甲酯的口服pk曲線。圖16.在大鼠中比較沒食子酸-ch2oco-mph綴合物與未結合的哌甲酯(從六個研究組合的數據)的口服pk曲線。圖17.在大鼠中比較沒食子酸-ch2oco-mph綴合物與未結合的哌甲酯的口服pk曲線。圖18.在大鼠中比較乳酸-ch2oco-mph綴合物與未結合的哌甲酯的口服pk曲線。圖19.在大鼠中比較mph-co2ch2-煙酰基-asp和mph-co2ch2-煙酰基-val綴合物與未結合的哌甲酯的口服pk曲線。圖20.在大鼠中比較mph-co2ch2-煙酰基-gly-ala和val-6-氨基己酸-ch2oco-mph綴合物與未結合的哌甲酯的口服pk曲線。圖21.在大鼠中比較6-氨基己酸-ch2oco-mph綴合物與未結合的哌甲酯的口服pk曲線。圖22.在大鼠中比較mph-co2ch2-煙酰基-otbu和mph-co2ch2-煙酸酯綴合物與未結合的哌甲酯的口服pk曲線。圖23.在大鼠中比較mph-co2ch2-煙酰基-otbu綴合物與未結合的哌甲酯的鼻內pk曲線。圖24.在大鼠中比較mph-co2ch2-煙酸酯綴合物與未結合的哌甲酯的鼻內pk曲線。圖25.在大鼠中比較mph-co2ch2-煙酰基-oet、mph-co2ch2-煙酰胺和mph-co2ch2-吡啶綴合物與未結合的哌甲酯的口服pk曲線。圖26.在大鼠中比較mph-co2ch2-煙酰胺綴合物與未結合的哌甲酯的鼻內pk曲線。圖27.在大鼠中比較mph-co2ch2-吡啶綴合物與未結合的哌甲酯的鼻內pk曲線。圖28.在大鼠中比較mph-co2ch2-煙酰胺綴合物與未結合的哌甲酯的靜脈內pk曲線。圖29.在大鼠中比較mph-co2ch2-吡啶綴合物與未結合的哌甲酯的靜脈內pk曲線。圖30.在大鼠中比較異煙酸-ch2oco-mph和磷酸-(對-水楊酸)-ch2oco-mph綴合物與未結合的哌甲酯的口服pk曲線。具體實施方式本發明技術提供與至少一種有機或者無機含氧酸結合以形成氨基甲酸氧基烷基酯的至少一種哌甲酯或者其一種或者多種衍生物或者組合(mph,苯基(哌啶-2-基)乙酸甲基酯),其為哌甲酯的新穎前藥組合物和/或綴合物。在一些實施方案中,通過經由各種連接體分子使哌甲酯與一系列有機或者無機含氧酸結合,意料不到地發現了至少一種本發明技術的綴合物或者前藥。在一些實施方案中,所述連接體為(酰基氧基)烷基氧基部分或者其衍生物。所述連接體鏈在一端經仲氨基甲酸酯鍵與哌甲酯連接并在另一端經酯鍵與含氧酸連接。本申請使用的術語“哌甲酯”意在包括哌甲酯的任何立體異構體形式,其包括四種立體異構體:d-赤-哌甲酯、l-赤-哌甲酯、d-蘇-哌甲酯和l-蘇-哌甲酯及其鹽和衍生物。哌甲酯可與苯基(哌啶-2-基)乙酸甲酯互換。術語“哌甲酯”包括所有鹽形式。哌甲酯也被稱為商品名sr、er(均可商購自novartisinternationalag,basil,switzerland)。在本發明技術中使用的哌甲酯可為哌甲酯的任何立體異構體,包括但不限于,d-赤-哌甲酯、l-赤-哌甲酯、d-蘇-哌甲酯和l-蘇-哌甲酯。在一些實施方案中,哌甲酯可為兩種或者更多種外消旋物的混合物,例如,但不限于,d/l-赤-哌甲酯和d/l-蘇-哌甲酯。在一些優選實施方案中,所述綴合物含有外消旋蘇-哌甲酯。在其它優選實施方案中,醇、胺、含氧酸或者硫醇與單一d-蘇-哌甲酯異構體連接。取決于連接體以及醇、胺、含氧酸和硫醇的化學結構以及它們連接的哌甲酯的手性組成,所得前藥綴合物可為異構體、外消旋混合物、單一異構體或者其組合的光學活性混合物。本申請使用的短語如“降低的”、“減少的”、“減小的”或者“減弱的”意在包括與未結合的哌甲酯相比,本發明技術的綴合物的藥理學活性、曲線下面積(auc)和/或峰值血漿濃度(cmax)的至少約10%的變化,對于濫用可能性和過量可能性的降低,優選較大的百分比變化。例如,所述變化也可大于約10%、約15%、約20%、約25%、約35%、約45%、約55%、約65%、約75%、約85%、約95%、約96%、約97%、約98%、約99%,或者其中的增量。本申請使用的術語“前藥”指的是在體內通過化學或者生物反應從藥物的惰性形式轉化成活性藥物的物質。在本發明技術中,前藥為至少一種藥物(哌甲酯)和例如至少一種含氧酸的綴合物。因此,本發明技術的綴合物為前藥并且本發明技術的前藥為綴合物。前藥經常是有用的,因為在一些實施方案中,它們可比母體藥物較容易地給藥或者處理。例如,它們可更易于通過口服給藥而生物利用,而母體藥物則不容易。與母體藥物相比,前藥也可在藥物組合物中具有改善的溶解性。前藥的實施方案將為哌甲酯綴合物,其代謝以暴露活性部分。在某些實施方案中,在體內給藥后,前藥化學轉化成化合物的在生物學上、在藥學上或者在治療上更有效的形式。在某些實施方案中,前藥通過一個或者多個步驟或者過程酶促代謝成化合物的生物學、藥學或者治療活性形式。為了制備前藥,將藥學活性化合物改性,使得活性化合物將在體內給藥后再生。將前藥設計成改變藥物的代謝或者運輸特征,在某些實施方案中,用于掩蔽副作用或者毒性、改善生物利用度和/或水溶性、改善藥物的滋味,或者在其它個別實施方案中用于改變藥物的其它特征或者性質。在一些實施方案中,本發明技術提供至少一種前藥組合物,其包含至少一種綴合物。所述至少一種綴合物可包含至少一種哌甲酯和至少一種醇、胺、含氧酸、硫醇,或者它們的衍生物。在一些實施方案中,所述綴合物還包含至少一個連接體。所述連接體使哌甲酯與醇、胺、含氧酸或者硫醇經一個或者多個共價鍵化學結合。取決于連接體和與哌甲酯結合的醇、胺、含氧酸和硫醇或者它們的衍生物,形成的至少一種前藥可為中性的(不帶電荷)、游離酸、游離堿或者藥用陰離子的或者陽離子的鹽形式或者在陽性和陰性組分之間具有任何比率的鹽混合物。這些陰離子的鹽形式可包括但不限于,例如,乙酸鹽、l-天冬氨酸鹽、苯磺酸鹽、碳酸氫鹽、碳酸鹽、d-樟腦磺酸鹽、l-樟腦磺酸鹽、檸檬酸鹽、乙二磺酸鹽、甲酸鹽、富馬酸鹽、葡糖酸鹽、氫溴酸鹽/溴化物、鹽酸鹽/氯化物、d-乳酸鹽、l-乳酸鹽、d,l-乳酸鹽、d,l-蘋果酸鹽、l-蘋果酸鹽、甲磺酸鹽、雙羥萘酸鹽、磷酸鹽、琥珀酸鹽、硫酸鹽、硫酸氫鹽、d-酒石酸鹽、l-酒石酸鹽、d,l-酒石酸鹽、內消旋-酒石酸鹽、苯甲酸鹽、葡庚糖酸鹽、d-葡糖醛酸鹽、羥苯酰苯酸鹽、羥乙基磺酸鹽、丙二酸鹽、甲基硫酸鹽、2-萘磺酸鹽、煙酸鹽、硝酸鹽、乳清酸鹽、硬脂酸鹽、甲苯磺酸鹽、硫氰酸鹽、醋茶堿鹽(acefyllinate)、乙酰甘氨酸鹽、氨基水楊酸鹽、抗壞血酸鹽、硼酸鹽、丁酸鹽、樟腦酸鹽、樟腦碳酸鹽、癸酸鹽、己酸鹽、膽酸鹽、環戊丙酸鹽、二氯乙酸鹽、依地酸鹽(edentate)、乙基硫酸鹽、糠酸鹽(furate)、褐霉酸鹽、粘酸鹽(半乳糖二酸鹽)、半乳糖醛酸鹽、沒食子酸鹽、龍膽酸鹽、谷氨酸鹽、谷氨酸鹽、戊二酸鹽、甘油磷酸鹽、庚酸鹽(enanthate)、羥基苯甲酸類、馬尿酸鹽、苯基丙酸鹽、碘化物、昔萘酸鹽、乳糖酸鹽、月桂酸鹽、馬來酸鹽、扁桃酸鹽、甲磺酸鹽、肉豆蔻酸鹽、萘二磺酸鹽、油酸鹽、草酸鹽、棕櫚酸鹽、苦味酸鹽、新戊酸鹽、丙酸鹽、焦磷酸鹽、水楊酸鹽、水楊酰硫酸鹽、磺基水楊酸鹽、鞣酸鹽、對苯二酸鹽、硫代水楊酸鹽、三溴酚鹽(tribrophenate)、戊酸鹽、丙戊酸鹽、己二酸鹽、4-乙酰氨基苯甲酸鹽、樟腦磺酸鹽、辛酸鹽、依托酸鹽、乙磺酸鹽、羥乙酸鹽、硫氰酸鹽,或者十一烯酸鹽。陽離子鹽形式可包括但不限于例如,鈉鹽、鉀鹽、鈣鹽、鎂鹽、鋅鹽、鋁鹽、鋰鹽、膽堿鹽、賴氨酸鎓鹽、銨鹽,或者丁三醇胺鹽。不希望受限于以下理論,據信,本發明技術的前藥/綴合物在體內經歷酯鍵的酶促水解,其隨后導致級聯反應,從而導致哌甲酯和相應的含氧酸、其代謝物和/或它們的衍生物的快速再生。本發明技術的醇、胺、含氧酸、硫醇或者其衍生物無毒或者在給定劑量水平具有極低毒性,并且優選為已知藥物、天然產物、代謝物,或者gras(通常認為是安全的)化合物(例如,防腐劑、染料、矯味劑等)或者無毒類似物或者其衍生物。一般結構和定義用于本發明技術的綴合物的組分的縮寫包括:mph表示哌甲酯;mph·hcl表示哌甲酯鹽酸鹽;asp表示天冬氨酸;val表示纈氨酸;tbu表示叔丁基;et表示乙基。在一些實施方案中,本發明技術的哌甲酯的前藥的一般結構可通過式(i)或者通過式(ii)表示:為了簡化圖畫,也可將式(i)和(ii)表示為:其中x選自o、s、se或者nr1;y不存在或者選自o、s、se、nr2或者cr3r4;r1和r2獨立地選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基羰基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、環烯基、環烯基烷基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基,或者聚乙二醇基團;r3和r4獨立地選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基、氨基、氨基羰基、銨基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、氰基、環烯基、環烯基烷基、羧基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵素、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、硝基、氧代、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基、聚乙二醇基團或者硫醇基;l不存在或者為對于每個重復亞單元,a獨立地選自cr5r6或者任選取代的芳基、亞芳基、碳環基、環烯基、環烷基、環炔基、雜環基、雜芳基;r5和r6彼此獨立地并且對于每個重復亞單元而言獨立地選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基、氨基、氨基羰基、銨基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、氰基、環烯基、環烯基烷基、羧基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵素、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、硝基、氧代、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基、聚乙二醇基團或者硫醇基;z不存在或者對于每個重復亞單元而言獨立地選自o、s、se或者nh;n為0-50;g對于每個重復亞單元而言獨立地選自醇、胺、氨基酸、銨、含氧酸、肽、聚(乙二醇)(peg)或者硫醇,或者其衍生物或者它們的組合;e為含氧酸;并且m為0-5。在式(i)的一些實施方案中,一個或者多個g本體與l、y(如果l不存在),或者與另一個g(例如,一個或者超過一個另外的g)共價鍵合。g在多次出現時可為全部相同的、全部獨特地不同的或者二者的組合。在式(ii)的一些實施方案中,一個或者多個e本體(至多m個本體)與哌甲酯的哌啶環中的氮或者與另一個e共價鍵合。e在多次出現時可為全部相同的、全部獨特地不同的或者二者的組合。在式(i)的一些優選實施方案中,x為o。在式(i)的一些優選實施方案中,y不存在或者選自o或者n。在式(i)的一些另外優選實施方案中,y為n。在式(i)的其它優選實施方案中,l選自:其中對于每個重復亞單元,r7、r8、r9、r10獨立地選自氫、烯基、烷氧基、烷基、炔基、芳基、取代的芳基、烷基芳基、環烯基、環烷基、環炔基、雜烷基、雜芳基,或者雜環基。優選地,對于每個重復亞單元,r7和r9獨立地選自氫、烷基、烷氧基、芳基或者取代的芳基,以及r8和r10優選為氫;q為1-10,優選為1-5;o和p為0-10,優選為0-2;以及q為nh或者o。在式(i)的一些另外優選實施方案中,l選自:其中q=1-6;在式(i)的其它優選實施方案中,g選自含氧酸、叔胺或者聚(乙二醇)衍生物。在式(i)的一些實施方案中,g為通過式(iii)和(iv)一般定義的叔胺:其中對于每個重復亞單元,r17獨立地選自o、s、se、nr21或者cr22r23;r14、r15、r16、r20、r21獨立地選自烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基羰基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、環烯基、環烯基烷基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基,或者聚乙二醇基團;r20也可不存在;r18、r19、r22、r23彼此獨立地并且對于(r17的)每個重復亞單元而言獨立地選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基、氨基、氨基羰基、銨基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、氰基、環烯基、環烯基烷基、羧基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵素、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、硝基、氧代、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基、聚乙二醇基團或者硫醇基;以及i為0-10。在一些實施方案中,式(iv)為環尺寸為3-10個原子的雜環,其中至少一個原子為氮原子并且至少一個原子為碳原子,并且所述環可為含有任何化學上可行的數目和組合的單鍵、雙鍵或者三鍵的脂族環或者所述環可為芳族環。在其它實施方案中,g經它的叔氮(參見式(iii)和(iv))或者經它的取代基中的一個的氨基、羥基或者羧基官能團與l共價鍵合。在式(i)的一些優選實施方案中,叔胺通過式(v)(式(iv)的子集)定義,其中:r18、r22和r23如對于式(iv)所定義。式(v)的一些另外優選實施方案通過式(vi)、(vii)和(viii)定義:在式(v)的這些實施方案中,g為羧基吡啶衍生物,優選為任選經酯鍵或者酰胺鍵與第二部分g2鍵合的煙酸。在一些實施方案中,g2優選為醇或者含氧酸,更優選為氨基酸。在式(viii)的這些實施方案中,r26選自氫、烯基、烯基氨基羰基、烷氧基、烷氧基羰基、烷基、烷基氨基、烷基氨基羰基、烷基銨基、烷基羰基、烷基羰基氨基、烷基羰基氧基、烷基亞磺酰基、烷基磺酰基、烷基硫基、炔基、炔基氨基羰基、氨基羰基、芳基、取代的芳基、芳基烯基、芳基烷氧基、芳基烷基、芳基炔基、芳基氨基、芳基氨基羰基、芳基銨基、芳基偶氮基、芳基羰基、芳基羰基氨基、芳基羰基氧基、芳基環烷基、芳基氧基、芳基氧基烷基、芳基亞磺酰基、芳基亞磺酰基烷基、芳基磺酰基、芳基磺酰基氨基、芳基硫基、芳基硫基烷基、環烯基、環烯基烷基、環烷基、環烷基烷基、環烷基氨基、環烷基氧基、環炔基、環雜烷基、環雜烷基烷基、鹵代烷氧基、鹵代烷基、雜芳基、雜芳基烯基、雜芳基烷基、雜芳基氨基、雜芳基羰基、雜芳基羰基氨基、雜芳基氧代、雜芳基氧基、雜芳基亞磺酰基、雜芳基磺酰基、雜芳基硫基、羥基、聚環烯基、聚環烯基烷基、聚環烷基、聚環烷基烷基,或者聚乙二醇基團。在式(viii)的一些實施方案中,r26優選為氫或者烷基。在式(i)的其它實施方案中,聚(乙二醇)衍生物通過式(ix)一般定義:其中r24為h或者nh2;r25為h、nh2或者co2h;q不存在或者為o;j和l為0-5;以及k為1-100。在式(i)的一些優選實施方案中,聚(乙二醇)衍生物為:其中k為1-100,優選為1-50或者1-10。在式(ii)的一些優選實施方案中,e為含氧酸,優選為氨基酸。含氧酸本發明技術的含氧酸(即,含氧酸(oxyacids)、含氧酸(oxoacids)、含氧酸(oxy-acids)、含氧酸(oxiacids)、含氧酸(oxacids))是含有氧、至少一種其它元素和至少一個與氧鍵合的氫的一類化合物,并且其通過失去一個或者多個正氫離子(質子)產生共軛堿。可將含氧酸歸類為有機酸或者無機酸和它們的衍生物。有機酸包括羧酸。羧酸在自然界中分布廣泛(天然存在),但是羧酸也可為非天然的(合成的)。可將羧酸基于它們的分子結構或者分子式歸類為很多種類,并且許多不同的種類可重疊。不希望將范圍限制為一個分類,可將本發明技術的羧酸分為以下類別:脂族羧酸、芳基羧酸、二羧酸、多元羧酸,和氨基酸類。適用于本發明技術的脂族羧酸包括但不限于,例如,飽和的、單不飽和的、多不飽和的、炔屬的、取代的(例如,烷基、羥基、甲氧基、鹵代等)、含有雜原子的或者含有環的羧酸。飽和羧酸的適合的實例包括但不限于例如,甲酸、乙酸、丙酸、丁酸、戊酸、己酸、庚酸、辛酸、2-丙基戊酸、壬酸、癸酸、十二烷酸、十四烷酸、十六烷酸、十七烷酸、十八烷酸,或者二十烷酸。適用于實踐本發明技術的單不飽和羧酸包括但不限于例如,4-癸烯酸、9-癸烯酸、5-月桂烯酸、4-十二烯酸、9-十四烯酸、5-十四烯酸、4-十四烯酸、9-十六烯酸、6-十六烯酸、6-十八烯酸,或者9-十八烯酸。適用于本發明技術的多不飽和羧酸包括但不限于例如,山梨酸、十八碳二烯酸、十八碳三烯酸、十八碳四烯酸、二十碳三烯酸、二十碳四烯酸、二十碳五烯酸、二十二碳五烯酸,或者二十二碳六烯酸。適用于本發明技術的炔羧酸包括但不限于十八碳炔酸、十八碳烯炔酸、6,9-十八碳烯炔酸、十七碳烯炔酸、十三碳四烯二炔酸、十三碳二烯三炔酸、十八碳二烯二炔酸、十七碳二烯二炔酸、十八碳二烯二炔酸、十八碳烯二炔酸,或者十八碳烯三炔酸。適用于實踐本發明技術的取代的羧酸包括但不限于例如,甲基丙酸、異戊酸、甲基十六烷酸、8-甲基-6-壬烯酸、甲基十八烷酸、三甲基二十八烷酸、三甲基二十四碳烯酸、七甲基三十碳烷酸、四甲基十六烷酸、四甲基十五碳烷酸、乳酸、甘油酸、羥乙酸、蘇糖酸、3-羥基丙酸、羥基十八碳三烯酸、羥基十八烯酸、羥基二十四烷酸、2-羥基丁酸、3-羥基丁酸、4-羥基丁酸、4-羥基戊酸、羥基十八碳二烯二炔酸、羥基十八碳二烯酸、10-羥基癸酸、羥基癸烯酸、羥基二十碳烯酸、羥基二十碳二烯酸、羥基十六烷酸、二羥基二十四碳烯酸、二羥基二十二酸、羥基二十二酸、三羥基十八烷酸、三羥基十六烷酸、三羥基二十碳六烯酸、三羥基二十碳五烯酸、2-甲氧基-5-十六烯酸、2-甲氧基十六烷酸、7-甲氧基-4-十四烯酸、9-甲氧基十五碳烷酸、11-甲氧基十七烷酸、3-甲氧基二十二酸、二乙酰氧基二十二酸、2-乙酰氧基二十二酸、2-乙酰氧基二十四烷酸、2-乙酰氧基二十六酸、9-氧代壬酸、氧代癸酸、氧代十二烯酸、羥基氧代癸烯酸、10-氧代-8-癸烯酸、氟代十八烯酸、氟代癸酸、氟代十四烷酸、氟代十六烷酸、氟代十八碳二烯酸、氯代羥基十六烷酸、氯代羥基十八烷酸、二氯代十八烷酸、3-溴-2-壬烯酸、9,10-二溴十八烷酸、9,10,12,13-四溴十八烷酸、10-硝基-9,12-十八碳二烯酸、12-硝基-9,12-十八碳二烯酸、9-硝基-9-十八烯酸、9-氧代-2-癸烯酸、9-氧代-13-十八烯酸、氧代十八碳三烯酸、15-氧代-18-二十四碳烯酸、17-氧代-20-二十六碳烯酸,或者19-氧代-22-二十八碳烯酸。含有雜原子的羧酸的適合的實例包括但不限于例如,9-(1,3-壬二烯氧基)-8-壬烯酸、9-(1,3,6-壬三烯氧基)-8-壬烯酸、12-(1-己烯氧基)-9,11-二十二碳二烯酸、12-(1,3-己二烯氧基)-9,11-二十二碳二烯酸、2-十二烷基硫烷基乙酸、2-十四烷基硫烷基乙酸、3-十四烷基硫烷基丙-2-烯酸,或者3-十四烷基硫烷基丙酸。含有環的羧酸的適合的實例包括但不限于例如,10-(2-己基環丙基)癸酸、3-(2-[6-溴-3,5-壬二烯基環丙基)丙酸、9-(2-十六烷基亞環丙基)壬-5-烯酸、8-(2-辛基-1-環丙烯基)辛酸、7-(2-辛基-1-環丙烯基)庚酸、9,10-環氧十八烷酸、9,10-環氧12-十八烯酸、12,13-環氧-9-十八烯酸、14,15-環氧-11-二十碳烯酸、11-(2-環戊烯-1-基)十一酸、13-(2-環戊烯-1-基)十三酸、13-(2-環戊烯基)-6-十三碳烯酸、11-環己基十一酸、13-環己基十三酸、7-(3,4-二甲基-5-戊基呋喃-2-基)庚酸、9-(4-甲基-5-戊基呋喃-2-基)壬酸、4-[5]-梯烷-丁酸、6-[5]-梯烷-己酸,或者6-[3]-梯烷-己酸。在本發明技術中適用于結合哌甲酯、其衍生物或者它們的組合的芳基羧酸包括例如,含有至少一個與芳環連接的羧基的化合物。本發明技術的適合的芳基羧酸可包括但不限于例如:(a)芳基羧酸,其中所述羧酸基與芳基部分直接連接,其包括但不限于苯甲酸類或者雜芳基羧酸類;(b)芳基羧酸,其中所述羧酸基被一個碳從芳基部分隔開,其包括但不限于支化的苯基丙酸,或者苯基乙酸的其它衍生物;或者(c)芳基羧酸,其中所述羧酸基被兩個碳從芳基部分隔開,其包括但不限于芐基乙酸類、其取代的衍生物或者肉桂酸類似物。本發明技術的一些實施方案提供與哌甲酯、其衍生物或者它們的組合結合的類別(a)、(b)或者(c)的芳基羧酸。本發明技術的一些實施方案提供與哌甲酯、其衍生物或者它們的組合結合的類別(a)的芳基羧酸,其中所述類別(a)的芳基羧酸為苯甲酸類、雜芳基羧酸類或者它們的衍生物。苯甲酸類本發明技術的一些實施方案提供哌甲酯、其衍生物或者它們的組合和至少一種苯甲酸類的至少一種綴合物。適合的常用苯甲酸類包括但不限于例如,苯甲酸,或者羥基苯甲酸類(例如,水楊酸類似物)。用于本發明技術的苯甲酸類的一般結構在式(x)中示出:其中x、y和z可獨立地選自包括h、o、s或者-(ch2)x-的代表性基團;r1、r2和r3可獨立地選自例如任何以下基團:h、烷基、烷氧基、芳基、取代的芳基、烯基、炔基、鹵素、鹵代烷基、烷基芳基、芳基烷基、雜環基、芳基烷氧基、環烷基、環烯基或者環炔基;o、p、q可獨立地為0或者1;以及x為整數1-10。苯甲酸類是自然界中常見的并且可以以它們的游離形式、作為鹽,或者作為酯和酰胺存在。在食品和藥品工業中也使用許多苯甲酸類似物。一些更豐富的苯甲酸類是具有羥基的衍生物。羥基官能團可以以它的游離形式存在或者用另一個化學部分封端,所述化學部分優選但不限于甲基或者乙酰基。苯環可具有另外的取代基。適合的苯甲酸類包括但不限于例如,苯甲酸,或者羥基苯甲酸類(例如,水楊酸類似物)。適用于本發明技術的羥基苯甲酸類的實例包括但不限于例如,苯甲酸、水楊酸、乙酰基水楊酸(阿司匹林)、3-羥基苯甲酸、4-羥基苯甲酸、6-甲基水楊酸、鄰,間,對-甲基水楊酸、槚如酸、4,5-二甲基水楊酸、鄰,間,對-百里酸、二氟尼柳、鄰,間,對-茴香酸、2,3-二羥基苯甲酸(2,3-dhb)、α,β,γ-雷瑣酸、原兒茶酸、龍膽酸、胡椒基酸、3-甲氧基水楊酸、4-甲氧基水楊酸、5-甲氧基水楊酸、6-甲氧基水楊酸、3-羥基-2-甲氧基苯甲酸、4-羥基-2-甲氧基苯甲酸、5-羥基-2-甲氧基苯甲酸、香草酸、異香草酸、5-羥基-3-甲氧基苯甲酸、2,3-二甲氧基苯甲酸、2,4-二甲氧基苯甲酸、2,5-二甲氧基苯甲酸、2,6-二甲氧基苯甲酸、藜蘆酸(3,4-二甲氧基苯甲酸)、3,5-二甲氧基苯甲酸、沒食子酸、2,3,4-三羥基苯甲酸、2,3,6-三羥基苯甲酸、2,4,5-三羥基苯甲酸、3-o-甲基沒食子酸(3-omga)、4-o-甲基沒食子酸(4-omga)、3,4-o-二甲基沒食子酸、丁香酸,或者3,4,5-三甲氧基苯甲酸。適用于實踐本發明技術的羥基苯甲酸類的一些結構可參見圖1。雜芳基羧酸類在其它實施方案中,本發明技術提供前藥組合物,其包含哌甲酯、其衍生物或者它們的組合和一種或者多種芳基或者雜芳基羧酸類的至少一種綴合物。適合地,常見天然產物和代謝物的雜原子是氮。雜芳基羧酸類及其衍生物的一般結構闡述于式(xi)、(xii)和(xiii):其中x、y和z可獨立地選自包括h、o、s或者-(ch2)x-的代表性基團;r1、r2和r3可獨立地選自任何以下基團:h、烷基、烷氧基、芳基、取代的芳基、烯基、炔基、鹵素、鹵代烷基、烷基芳基、芳基烷基、雜環基、芳基烷氧基、環烷基、環烯基或者環炔基;o、p、q可獨立地選自0或者1;以及x為整數1-10。氮雜環化合物在自然界中常見并且牽涉在植物和動物中的數種生物功能中。適用于實踐本發明技術的雜芳基羧酸類的實例包括但不限于例如,吡啶衍生物,其中的一些在煙酸酯和色氨酸代謝中發揮重要作用。在這些化合物中,苯環的一個碳被氮原子替代。除了羧基,這組化合物還可具有另外的取代基,優選但不限于羥基。適用于本發明技術的雜芳基羧酸類的實例包括但不限于煙酸(尼克酸)、異煙酸、吡啶-2-甲酸、3-羥基吡啶-2-甲酸、6-羥基煙酸、檸嗪酸、2,6-二羥基煙酸、犬尿烯酸、黃尿烯酸、6-羥基犬尿烯酸、8-甲氧基犬尿烯酸、7,8-二羥基犬尿烯酸,或者7,8-二氫-7,8-二羥基犬尿烯酸。適用于實踐本發明技術的雜芳基羧酸類的一些結構可參見圖2。芳基羧酸本發明技術的一些實施方案提供與哌甲酯、其衍生物或者它們的組合結合的類別(b)的芳基羧酸,其中具有被一個碳從芳基部分隔開的羧基的適合的羧酸包括但不限于例如,支化苯基丙酸(即,2-甲基-2-苯基乙酸類)或者苯基乙酸類的其它衍生物,例如,具有下式(xiv)中所述通式的化合物。在一些實施方案中,羧酸為苯基乙酸類、支化苯基丙酸類、未支化苯基丙酸類(芐基乙酸類)、苯基丙烯酸類(肉桂酸類)、其鹽、其衍生物,或者它們的組合。這些化合物的適合的實例包括但不限于某些類型的nsaid(非甾體抗炎藥)如洛芬類(profens),或者酪氨酸代謝物(例如對羥基苯基丙酮酸類)等。本發明技術的苯基丙酸或者苯基乙酸類的其它衍生物的一般結構示于式(xiv):其中x、y和z可獨立地選自包括h、o、s或者-(ch2)x-的代表性基團;r1、r2和r3可獨立地選自任何以下基團:h、烷基、烷氧基、芳基、取代的芳基、烯基、炔基、鹵素、鹵代烷基、烷基芳基、芳基烷基、雜環基、芳基烷氧基、環烷基、環烯基或者環炔基;o、p、q可獨立地為0或者1;alk為烷基鏈-(ch2)n-,n為0或者1;x為整數1-10;以及r6選自h、oh或者羰基。苯基乙酸類苯基乙酸類包括天然產物、代謝物和藥物的多個子集。一個這種藥物子集為“洛芬類”,其為一種類型的nsaid和某些苯基丙酸的衍生物(即,2-甲基-2-苯基乙酸類似物)。一些其它苯基乙酸類在苯基丙氨酸和酪氨酸代謝中具有重要功能。本發明技術的適合的苯基乙酸類包括但不限于苯基乙酸(氫化阿托酸)、2-羥基苯基乙酸、3-羥基苯基乙酸、4-羥基苯基乙酸、高原兒茶酸、尿黑酸、2,6-二羥基苯基乙酸、高香草酸、高異香草酸、高藜蘆酸、阿托酸、d,l-托品酸、雙氯芬酸、d,l-扁桃酸、3,4-二羥基-d,l-扁桃酸、香草基-d,l-扁桃酸、異香草基-d,l-扁桃酸、布洛芬、非諾洛芬、卡洛芬、氟比洛芬、酮洛芬,或者萘普生。適用于實踐本發明技術的苯基乙酸類的一些結構可參見圖3。芐基乙酸類和肉桂酸類在本發明技術的一些實施方案中,使類別(c)的芳基羧酸與哌甲酯、其衍生物或者它們的組合結合,其中所述類別(c)的芳基羧酸包括但不限于例如,芐基乙酸類、其取代的衍生物或者肉桂酸類似物,例如具有下面的通式(xv)和(xvi)的化合物:其中x、y和z可獨立地選自包括h、o、s或者-(ch2)x-的代表性基團;r1、r2和r3可獨立地選自任何以下基團:h、烷基、烷氧基、芳基、取代的芳基、烯基、炔基、鹵素、鹵代烷基、烷基芳基、芳基烷基、雜環基、芳基烷氧基、環烷基、環烯基或者環炔基;o、p、q可獨立地為0或者1;x為1-10的整數;r4為h或者oh;以及r5為h、oh或者羰基。兩類化合物以天然產物或者代謝物(例如,苯基丙氨酸代謝)的形式在自然界中豐富。羧基可與芳環直接連接或者被烷基或者烯基鏈隔開。用于本發明技術的烷基或者烯基的鏈長應該優選不超過兩個未支化碳,但是不限制潛在側鏈或者另外的官能團上的原子數目。本發明技術也包括僅含碳的芳基和具有雜原子的芳基(雜芳基)。與羧基官能團直接連接或者通過烷基或者烯基鏈連接的芳基或者雜芳基應該優選為6元環,并且應該優選不含雜原子或者含有一個雜原子。本領域技術人員應承認的是,另外的取代的或者未取代的芳族或者脂族環可與該6元芳基或者雜芳基部分稠合。芐基乙酸類在羧基官能團和苯環之間通過亞乙基限定。烷基鏈和芳基部分可具有例如取代基,優選為羥基。這種類型的一些化合物可在苯基丙氨酸代謝中發現。適用于實踐本發明技術的芐基乙酸類的實例包括但不限于例如,芐基乙酸、草木犀酸、3-羥基苯基丙酸、4-羥基苯基丙酸、2,3-二羥基苯基丙酸、d,l-苯基乳酸、鄰,間,對-羥基-d,l-苯基乳酸,或者苯基丙酮酸。適用于實踐本發明技術的芐基乙酸類的一些結構可參見圖4。肉桂酸(3-苯基丙烯酸)是芐基乙酸的不飽和類似物,其在植物和水果中無所不在。肉桂酸類以兩種異構體形式出現:順式(z)和反式(e)。在本發明技術中使用的肉桂酸類可為異構體形式,但是優選為反式構型。類似于芐基乙酸類,肉桂酸的衍生物在分子的烯基或者芳基部分上可為取代的。優選取代基為羥基和甲氧基。某些肉桂酸類在苯基丙氨酸代謝中發揮重要作用。用于本發明技術的一些適合的肉桂酸類包括但不限于例如,肉桂酸、鄰,間,對-香豆酸、2,3-二羥基肉桂酸、2,6-二羥基肉桂酸、咖啡酸、阿魏酸、異阿魏酸、5-羥基阿魏酸、芥子酸,或者2-羥基-3-苯基丙烯酸。適用于實踐本發明技術的肉桂酸類的結構可參見圖5。二羧酸和三羧酸類在一些實施方案中,可使哌甲酯、其衍生物或者它們的組合與一種或者多種二羧酸或者三羧酸類結合。二羧酸類是具有兩個羧基的化合物,通式為hooc-r-cooh,其中r可為烷基、烯基、炔基或者芳基,或者它們的衍生物。二羧酸類可具有直碳鏈或者支化碳鏈。碳鏈長度可為短的或者長的。多元羧酸是具有三個或者更多個羧基的羧酸。適用于實踐本發明技術的二羧酸和三羧酸類的實例包括但不限于例如,草酸、丙二酸、琥珀酸、戊二酸、己二酸、庚二酸、辛二酸、壬二酸、癸二酸、巴西基酸、它普酸、蘋果酸、酒石酸、二羥基丙酮二酸、α-羥基戊二酸、甲基丙二酸、美格魯托、二氨基庚二酸、氨基甲酰基天冬氨酸、富馬酸、馬來酸、甲基富馬酸、3-甲基戊烯二酸、愈傷酸、鄰苯二甲酸、間苯二甲酸、對苯二甲酸、吡啶二羧酸、檸檬酸、異檸檬酸、丙三酸,或者苯均三酸。適用于實踐本發明技術的二羧酸類的一些結構可參見圖6,以及適用于實踐本發明技術的三羧酸類的一些結構可參見圖7。無機含氧酸在本發明技術的一些實施方案中,使至少一種哌甲酯、其衍生物或者它們的組合與至少一種無機含氧酸或者其有機或者無機衍生物結合。本發明技術的無機含氧酸含有-oh基團(例如,磷酸)或者它們可為無機含氧酸的有機或者無機衍生物(例如,膦酸類、二磷酸類)。無機含氧酸和它們的衍生物的一些適合的實例包括但不限于磷酸類、膦酸類、次膦酸類、氨基磷酸類、氨基亞磷酸類、二磷酸類、三磷酸類、二膦酸類、硫代磷酸類、二硫代磷酸類、亞磷酸類、硫酸類、磺酸類、氨基磺酸類、亞硫酸類、硫代硫酸類、硫代亞硫酸類、亞磺酸類、硝酸類、亞硝酸類、硼酸類(borate)、烴基硼酸類(boronate)、次氯酸類、碳酸類,或者氨基甲酸類。用于實踐本發明技術的一些無機含氧酸的一般結構可參見圖8,以及用于實踐本發明技術的無機含氧酸的一些有機或者無機衍生物的結構可參見圖9。本發明技術的優選實施方案包括一種或者多種無機含氧酸,其為磷酸酯。更優選的實施方案包括這樣的無機含氧酸:磷酸單酯,甚至更優選為磷酸。本發明技術的另外優選的含氧酸包括脂肪酸、羥基羧酸、氨基酸、任選酯化的磷酸和任選酯化的二羧酸類。本發明技術的更優選的含氧酸為c2-24羧酸、芳基羧酸、氨基己酸、磷酸、標準氨基酸類和非標準氨基酸類。氨基酸類氨基酸類是生命的最重要結構單元之一。它們構成蛋白質、肽和許多次級代謝物的結構亞單元。除了組成蛋白質主鏈的22種標準(蛋白原的)氨基酸類之外,還存在數百種其它天然(非標準)氨基酸類,其以游離形式或者作為天然產物中的組分被發現。在本發明的前藥的一些實施方案中使用的氨基酸類包括天然氨基酸類、合成(非天然的,非自然的)氨基酸類,和它們的衍生物。標準氨基酸類目前具有22種已知的標準或者蛋白原的氨基酸類,其組成蛋白質的單體單元并在遺傳密碼中編碼。標準氨基酸類包括丙氨酸、精氨酸、天冬酰胺、天冬氨酸、半胱氨酸、谷氨酸、谷氨酰胺、甘氨酸、組氨酸、異亮氨酸、亮氨酸、賴氨酸、甲硫氨酸、苯基丙氨酸、脯氨酸、吡咯賴氨酸、硒代胱氨酸、絲氨酸、蘇氨酸、色氨酸、酪氨酸和纈氨酸。這些標準氨基酸類具有圖10中所示的一般結構,其中r表示α-碳上的側鏈。非標準氨基酸類非標準氨基酸類可在通過化學修飾已經合并在蛋白質中的標準氨基酸類而產生的蛋白質中發現。該組也包括沒有在蛋白質中發現,但是仍以游離形式或者與其它分子本體結合地存在于活的生物體中的氨基酸類。非標準氨基酸類主要作為標準氨基酸類的代謝途徑中的中間體出現并不通過遺傳密碼編碼。非標準氨基酸類的實例包括但不限于鳥氨酸、高精氨酸、瓜氨酸、高瓜氨酸、高絲氨酸、茶氨酸、γ-氨基丁酸、6-氨基己酸、肌氨酸、肉堿、2-氨基己二酸、泛酸、牛磺酸、亞牛磺酸、羊毛硫氨酸、硫代半胱氨酸、胱硫醚,高半胱氨酸、β-氨基酸類如β-丙氨酸、β-氨基異丁酸、β-亮氨酸、β-賴氨酸、β-精氨酸、β-酪氨酸、β-苯基丙氨酸、異絲氨酸、β-谷氨酸、β-酪氨酸、β-多巴(3,4-二羥基-l-苯基丙氨酸)、α,α-二取代的氨基酸如2-氨基異丁酸、異纈氨酸、二-n-乙基甘氨酸、n-甲基酸如n-甲基-丙氨酸、l-甲基色氨酸、羥基-氨基酸類如4-羥基脯氨酸、5-羥基賴氨酸、3-羥基亮氨酸、4-羥基異亮氨酸、5-羥基-l-色氨酸、環狀氨基酸如1-氨基環丙基-1-羧酸、氮雜環丁烷-2-羧酸和哌可酸。可在本發明的前藥的一些實施方案中使用的適合的非標準氨基酸類的一些結構在圖11中示出。合成氨基酸類合成氨基酸類非天然存在,而是合成制備。實例包括但不限于烯丙基甘氨酸、環己基甘氨酸、n-(4-羥基苯基)甘氨酸、n-(氯乙酰基)甘氨酸酯、2-(三氟甲基)-苯基丙氨酸、4-(羥基甲基)-苯基丙氨酸、4-氨基-苯基丙氨酸、2-氯苯基甘氨酸、3-胍基丙酸、3,4-脫氫-脯氨酸、2,3-二氨基苯甲酸、2-氨基-3-氯苯甲酸、2-氨基-5-氟苯甲酸、別-異亮氨酸、叔-亮氨酸、3-苯基絲氨酸、異絲氨酸、3-氨基戊酸、2-氨基-辛二酸、4-氯-β-苯基丙氨酸、β-高脯氨酸、β-高丙氨酸、3-氨基-3-(3-甲氧基苯基)丙酸、n-異丁酰基-半胱氨酸、3-氨基-酪氨酸、5-甲基-色氨酸、2,3-二氨基丙酸、5-氨基戊酸,和4-(二甲基氨基)肉桂酸。可在本發明的前藥的一些實施方案中使用的適合的合成氨基酸類的一些結構在圖12中示出。連接體在本發明技術的一些實施方案中,可使哌甲酯、其衍生物或者它們的組合與一種或者多種有機或者無機含氧酸經一個或者多個連接體結合。本發明技術的連接體部分(其使一種或者多種有機或者無機含氧酸與哌甲酯、其衍生物或者它們的組合連接)優選為至少一個(酰基氧基)烷基氧基或者其衍生物,其具有以下通式:-c(o)o-x-o-其中x選自包括任選取代的烷基、任選取代的芳基、任選取代的烷基芳基、任選取代的雜烷基、任選取代的雜芳基、任選取代的雜環基、任選取代的烯基、任選取代的炔基、任選取代的環烷基、任選取代的環烯基、任選取代的環炔基或者任選取代的烷氧基取代基的代表性基團。本發明技術的優選實施方案包括這樣的連接體:其中x為至少一個脂族基團。更優選的實施方案包括這樣的連接體:其中x為至少一個烷基。更加優選的實施方案為(酰基氧基)甲基氧基、(酰基氧基)乙基氧基,或者(酰基氧基)甲基(甲基)氧基連接體。給藥、制劑和優點本發明技術的前藥或者綴合物組合物可口服給藥,并且在給藥后,在體內水解后釋放活性哌甲酯、其衍生物或者它們的組合。不希望被任何特定理論束縛,本發明技術的與哌甲酯、其衍生物或者它們的組合結合的含氧酸是天然存在的代謝物、藥學活性化合物或者其模擬物或者其衍生物。據信,本發明技術的前藥或者綴合物可被生理系統容易地識別出,從而導致水解和哌甲酯的釋放。本發明技術的前藥本身被認為沒有或者具有有限的藥理學活性,并因此可遵循不同于母體藥物(即,哌甲酯)的代謝途徑。不被任何理論束縛,據信,通過選擇適合的連接體和含氧酸(“配體”),可控制哌甲酯向體循環中的釋放,甚至當前藥經不同于口服給藥的途徑給藥時。在一個實施方案中,至少一種本發明技術的經結合的哌甲酯、其衍生物或者它們的組合被認為意料不到地釋放哌甲酯、其衍生物或者它們的組合,其類似于游離或者未修飾的哌甲酯。在另一可選實施方案中,至少一種本發明技術的經結合的哌甲酯、其衍生物或者它們的組合被認為意料不到地以受控或者持續的形式釋放。已經意料不到地發現,在本發明技術的一些實施方案中,與未結合的哌甲酯相比,本申請的前藥或者綴合物提供提高的生物利用度。在一些實施方案中,與未結合的哌甲酯相比,本發明技術的前藥或者綴合物意料不到地提供提高的水溶性。在一些實施方案中,本發明技術的前藥或者組合物的水溶性是未結合的哌甲酯的至少約1.2倍或者至少約1.5倍。在一些實施方案中,本發明技術的前藥或者組合物具有至少約1.7倍、至少約2.0倍、至少約2.2倍、至少約2.5倍、至少約3.0倍、至少約4.0×或者至少約5倍的未結合的哌甲酯的水溶性,并包括其中或者較高的任何倍數,其具有大于未結合的哌甲酯的水溶性。不被任何特定理論束縛,水溶性的提高可允許所述綴合物以與未結合的哌甲酯相比而言較高濃度、劑量強度或者較高劑量負載能力形成某些劑型。在一些實施方案中,這些劑型包括但不限于需要水溶性的形式,其包括但不限于液體和口服薄膜或者條片。在另一實施方案中,至少一種本發明技術的前藥或者綴合物被認為與未修飾的哌甲酯相比而言意料不到地具有提高的吸收。在又一實施方案中,至少一種本發明技術的前藥或者綴合物被認為與未結合的哌甲酯相比而言意料不到地具有提高的生物利用度。在一些實施方案中,所述綴合物能夠酶促或者水解活化或者轉化成活性形式。在一個實施方案中,本申請所述的組合物或者前藥將釋放哌甲酯、它的活性代謝物和/或衍生物和它們的組合,從而當與等摩爾劑量的游離或者未結合的哌甲酯相比時,導致哌甲酯、它的活性代謝物和/或衍生物和它們的組合的提高的峰值血漿濃度和/或暴露。不被任何特定理論束縛,據信,這可允許當與未修飾的哌甲酯相比時給藥較低劑量并得到相等或者改善的治療效果,但是具有較少和/或較不嚴重的副作用,由此改善藥物的安全性分布。哌甲酯的常見副作用是神經質、煩躁、焦慮,和失眠或者嗜睡。其它常見副作用為腹痛、體重減輕、超敏反應、惡心、眩暈、心悸、頭痛、運動障礙、血壓、脈搏變化、心動過速、咽痛,和心律不整。在另一實施方案中,相對于未修飾的哌甲酯而言提高的吸收,或者相對于游離哌甲酯而言改善的水溶性可提供較好的哌甲酯生物利用度,其涉及較高的曲線下面積(auc)或者具有較高的循環血漿濃度。在一個實施方案中,通過例如改變體內的哌甲酯和它的代謝物如惰性利他林酸的量和/或比率,至少一種本發明技術的前藥或者綴合物將改變哌甲酯、其衍生物或者它們的組合的代謝分布。例如,所述至少一種前藥或者綴合物將降低由未修飾的哌甲酯產生的代謝物(包括活性的、惰性的、毒性的或者非毒性的代謝物)的數目和/或量。不希望被任何特定理論束縛,據信,這種代謝變化可潛在地減輕某些副作用并改善哌甲酯的安全性分布。在另一實施方案中,本發明技術的前藥或者綴合物將意料不到地產生在哌甲酯血漿濃度方面降低的患者間差異性。不被任何特定理論束縛,可假定,哌甲酯血漿濃度的患者間差異性的降低可由于提高的生物利用度或者改變的代謝途徑或者二者的組合。在另一實施方案中,與未修飾的哌甲酯相比,本發明技術的前藥將改變釋放的哌甲酯的代謝途徑。據信,這種新的代謝可降低患者間差異性和/或降低與未結合的哌甲酯或者任何它的代謝物相關的副作用。在另一實施方案中,至少一種本發明技術的前藥或者綴合物可包含外消旋d-和l-哌甲酯,其優選在體內水解成d-哌甲酯,并因此遞送更多治療活性的d-異構體。不希望被任何特定理論束縛,這可降低由l-哌甲酯和/或它的代謝物導致的潛在的副作用。在另一實施方案中,當以等摩爾劑量口服給藥時,至少一種本發明技術的前藥或者綴合物被認為意料不到地產生高于由未結合的哌甲酯、其衍生物或者它們的組合產生的cmax值的釋放的哌甲酯、其衍生物或者它們的組合的cmax值。在另一實施方案中,當以等摩爾劑量口服給藥時,至少一種前藥或者綴合物被認為令人驚訝地產生高于由未結合的哌甲酯產生的auc值的釋放的哌甲酯、其衍生物或者它們的組合的auc值。在又一實施方案中,當以等摩爾劑量口服給藥時,至少一種前藥或者綴合物被認為令人驚訝地產生高于由未結合的哌甲酯產生的cmax和auc值的釋放的哌甲酯的cmax和auc值。在一些實施方案中,當以等摩爾劑量口服給藥時,auc為未結合的哌甲酯的auc的約110%或者更大,例如約110%至約260%,可選擇地約120%至約260%,可選擇地約110%至約250%,包括但不限于約110%、約130%、約150%、約170%、約190%、約210%、約230%、約250%或者其中的任何量,增量為約0.5%、約1%、約2%、約2.5%、約5%、約10%,或者約20%。在一些實施方案中,當以等摩爾劑量口服給藥時,cmax為未結合的哌甲酯的cmax的約110%或者更大,例如約110%至約260%,可選擇地約120%至約260%,可選擇地約110%至約250%,包括但不限于約110%、約130%、約150%、約170%、約190%、約210%、約230%、約250%或者其中的任何量,增量為約0.5%、約1%、約2%、約2.5%、約5%、約10%,或者約20%。在另一實施方案中,當以等摩爾劑量給藥時,所述至少一種前藥或者綴合物被認為意料不到地產生長于由未結合的哌甲酯產生的t最大值的釋放的哌甲酯的t最大值。在另一實施方案中,當以等摩爾劑量給藥時,所述至少一種前藥或者綴合物被認為令人驚訝地產生類似于由未結合的哌甲酯產生的t最大值的釋放的哌甲酯的t最大值。在一些實施方案中,當以等摩爾劑量鼻內或者靜脈內給藥時,所述auc為未結合的哌甲酯的auc的約50%或者更小,例如約50%至約0.1%,可選擇地約25%至約0.1%,可選擇地約50%至約1%,包括但不限于約50%、約40%、約30%、約20%、約10%、約1%或者其中的任何量,增量為約0.5%、約1%、約2%、約2.5%、約5%或者約10%。哌甲酯是成癮的并易于物質濫用,因為它與可卡因和苯丙胺的藥理學相似性。已經報導,口服濫用導致幻覺、偏執、欣快,和妄想障礙。口服濫用可隨后升級至靜脈內和鼻內濫用。欣快已經在靜脈內給藥哌甲酯后報導。當鼻內給藥時發現,效果類似于苯丙胺的鼻內使用。在本發明技術的一些可選實施方案中,本發明技術的化合物、前藥、組合物和/或方法被認為提供降低的過量可能性、降低的濫用可能性和/或改善哌甲酯、其衍生物或者它們的組合在毒性或者次優釋放分布方面的特征。在本發明技術的一些可選實施方案中,當通過給藥的注射或者鼻內途徑給藥時,本發明技術的一些組合物可優選不具有藥理學活性或者具有大量降低的藥理學活性。但是,它們仍然口服可生物利用。不希望限制于下面的理論,據信,過量保護可發生,這是由于在口服給藥后所述綴合物暴露于不同的酶和/或代謝途徑,由此相對于暴露于循環中的酶或者鼻中的粘膜(這限制哌甲酯、其衍生物或者它們的組合從所述綴合物釋放的能力),本發明技術的綴合物暴露于腸和首過代謝。因此,在一些可選實施方案中,通過限制可選給藥途徑的效力,提供耐濫用性。再次,不希望被任何特定理論束縛,生物利用度可為在口服給藥后化學連接(即,共價連接)水解的結果。在至少一個可選實施方案中,經非口服途徑,本發明技術的前藥預期不水解或者以降低的速度或者以有限的程度水解。結果,當注射或者鼻吸時,與通過這些途徑給藥的游離哌甲酯相比,本發明技術的前藥被認為不產生高的釋放的哌甲酯的血漿或者血液濃度。在一些可選實施方案中,可以預期的是,至少一些包含一種或者多種哌甲酯、其衍生物或者它們的組合的前藥的本發明技術的組合物對通過在非法使用期間經常使用的腸胃外給藥途徑如靜脈內“注射”或者鼻內“嗅吸”的濫用耐受。在至少一個預期的可選實施方案中,當本發明技術的組合物通過腸胃外途徑遞送時,哌甲酯、其衍生物或者它們的組合的釋放被降低。在一些其它預期的可選實施方案中,通過例如磨碎或者碾碎固體形式的方法,物理處理本發明技術的綴合物不能使哌甲酯、其衍生物或者它們的組合從所述結合的哌甲酯、其衍生物或者它們的組合釋放,因為它們被認為包含共價結合的哌甲酯、其衍生物或者它們的組合。而且,本發明技術的一些可選綴合物預期在潛在藥物濫用者可用于“提取”分子的活性部分(例如,通過所述綴合物進行沸騰,或者酸性或者堿性溶液處理)的條件下對化學水解呈現耐性。在一些可選實施方案中,優選地,一些含有本發明技術的前藥或者綴合物的組合物在通過注射或者鼻內給藥途徑給藥時沒有藥理學活性或者具有大量降低的藥理學活性。但是,它們仍然口服可生物利用。例如,在一個可選實施方案中,在碾碎用于遞送治療性組分(即,活性成分/藥物)的片劑、膠囊劑或者其它口服劑型后,至少一種本發明技術的前藥或者綴合物預期令人驚訝地保持它的效力和濫用耐性,這被認為是由于固有釋放分布是組合物的性質,而非制劑的性質。相反,用于控制哌甲酯釋放的常規的延長釋放制劑在碾碎后立即經歷至多所有哌甲酯內容物的釋放。當注射或者嗅吸碾碎的片劑的內容物時,大劑量的哌甲酯產生成癮者追求的“快感”效果。本發明技術提供基于刺激物的治療方法和劑型,用于需要刺激cns的某些障礙,例如,注意力缺陷伴多動癥(adhd)、注意力缺陷障礙(add)、自閉癥譜群障礙(autisticspectrumdisorder)、孤獨癥、阿斯佩各障礙(asperger’sdisorder)、全身性發育障礙、睡眠障礙、肥胖癥、抑郁癥、雙相型障礙、進食障礙、慢性疲勞綜合征、精神分裂癥、重度抑郁癥、發作性睡病,或者自閉癥譜群障礙。盡管不希望被任何特定理論束縛,但是據信,與現有的刺激物治療方法和劑型相比,用本發明技術的組合物治療上述的這種cns病癥導致提高的生物利用度。在一個優選實施方案中,至少一種本發明技術的前藥或者組合物用于治療注意力缺陷伴多動癥(adhd)。在一些實施方案中,至少一種本發明技術的組合物或者前藥可在一種或者多種治療具有至少一種需要刺激一種或者多種患者的中樞神經系統的疾病、障礙或者病癥的所述患者的方法中使用,所述方法包括口服給藥藥學有效量的至少一種組合物或者前藥。在一些實施方案中,至少一種本發明技術的組合物或者前藥可在一種或者多種治療一種或者多種患者的方法中使用,所述患者具有至少一種通過控制、預防、限制或者抑制神經遞質攝取/再攝取或者激素攝取/再攝取而介導的疾病、障礙或者病癥,所述方法包括向至少一種患者給藥藥學有效量的至少一種前藥或者組合物。在一些實施方案中,所述神經遞質為5-羥色胺、多巴胺或者去甲腎上腺素。在一些實施方案中,所述激素為兒茶酚胺。至少一些包含哌甲酯、其衍生物或者它們的組合的前藥的本發明技術的組合物也可用于治療刺激物(可卡因、甲基苯丙胺)濫用和成癮,用于改善戰場警覺性,和/或用于打擊疲勞。至少一種本發明技術的前藥或者綴合物可配制成口服給藥的劑型。這些劑型包括但不限于片劑、膠囊劑、小膠囊劑、錠劑、糖錠、粉劑、混懸劑、糖漿劑、溶液劑、口服薄膜(otf)、口服條片、吸入混配物或者栓劑。優選的口服給藥形式為膠囊劑、片劑、溶液劑和otf。本發明技術的適合的配制媒介物包括但不限于水、磷酸鹽緩沖鹽水(pbs)、10%tween水溶液,和50%peg-400水溶液。固體劑型可任選包含以下的賦形劑類型:抗粘附劑、粘合劑、包衣、崩解劑、填充劑、矯味劑和著色劑、助流劑、潤滑劑、防腐劑、吸附劑和甜味劑。本發明技術的口服制劑也可包含在水性液體或者非水性液體中的溶液劑或者混懸劑中。制劑也可為乳劑,例如水包油液體乳劑或者油包水液體乳劑。所述油可通過以下方法給藥:將純化的和殺菌的液體添加至制備的腸制劑,然后將腸制劑置于不能吞咽的患者的喂食管中。軟凝膠或者軟明膠膠囊劑可例如通過以下方法制備:將制劑分散在適當的媒介物(常使用植物油)中,形成高粘度混合物。然后將這種混合物用基于凝膠的膜,使用軟凝膠工業中的技術人員已知的技術和機械進行包封。然后將如此形成的單個單位干燥至恒重。可咀嚼片劑例如可通過以下方法制備:將制劑與賦形劑混合,所述賦形劑設計成形成相對軟的矯味的片劑劑型,所述相對軟的矯味的片劑劑型意圖被咀嚼而非吞咽。可使用常規片劑機械和操作,例如,直接壓縮和造粒,即,或者在壓縮之前預壓。在藥物固體劑型制備中涉及的那些個體精通所使用的方法和機械,因為可咀嚼劑型是藥物工業中的非常普通的劑型。包衣片劑例如可通過以下方法制備:使用諸如旋轉鍋包衣方法或者空氣懸浮方法的技術包衣片劑,以在片劑上沉積連續膜層。壓縮片劑例如可通過以下方法制備:將制劑與賦形劑混合,所述賦形劑用于將粘合性質結合至崩解性質。使用本領域技術人員已知的方法和機械,將混合物直接壓縮,或者造粒,然后壓縮。然后將所得壓縮片劑劑量單位根據市場需要包裝,例如,包裝在單位劑量、卷、散裝瓶、泡罩包裝等中。本發明技術也涵蓋生物可接受的載體的使用,所述生物可接受的載體可由很多種材料制備。非限制性地,這種材料包括稀釋劑、粘合劑和膠粘劑、潤滑劑、增塑劑、崩解劑、著色劑、填充物質、矯味劑、甜味劑和雜料如緩沖劑和吸附劑,以制備特定的加入藥物的組合物。粘合劑可選自很多種材料,例如羥基丙基甲基纖維素、乙基纖維素,或者其它適合的纖維素衍生物、聚維酮、丙烯酸的和甲基丙烯酸的共聚物、藥用釉料、樹膠、乳衍生物如乳清、淀粉和衍生物,以及本領域技術人員已知的其它常規粘合劑。示例性非限制性溶劑為水、乙醇、異丙醇、二氯甲烷或者其混合物和它們的組合。示例性非限制性填充物質包括糖、乳糖、明膠、淀粉,和二氧化硅。應理解的是,除了上面特別提及的成分之外,本發明技術的制劑可包括其它適合的試劑如矯味劑、防腐劑和抗氧化劑。這種抗氧化劑為食物可接受的,并且可包括維生素e、胡蘿卜素、bht或者其它抗氧化劑。混合物可包含的其它化合物例如為藥物惰性成分,例如,用于片劑或者膠囊劑的固體和液體稀釋劑如乳糖、右旋糖、蔗糖、纖維素、淀粉或者磷酸鈣,用于軟膠囊劑的橄欖油或者油酸乙酯,和用于混懸劑或者乳劑的水或者植物油;潤滑劑如硅石、滑石、硬脂酸、硬脂酸鎂或者硬脂酸鈣和/或聚乙二醇;膠凝劑如膠狀粘土;增稠劑如黃蓍樹膠或者藻酸鈉;粘合劑如淀粉、阿拉伯膠、明膠、甲基纖維素、羧甲基纖維素或者聚乙烯吡咯烷酮;崩解劑如淀粉、藻酸、藻酸鹽或者淀粉羥乙酸鈉;泡騰混合物;染料;甜味劑;濕潤劑如卵磷脂、聚山梨酯或者硫酸月桂基酯(laurylsulfates);以及其它治療上可接受的輔助成分如濕潤劑、防腐劑、緩沖劑和抗氧化劑,其為用于這種制劑的已知添加劑。為了口服給藥,含有稀釋劑、分散劑和/或表面活性劑的細粉劑或者顆粒劑可以以飲劑、水或者糖漿劑、干燥狀態的膠囊劑或者囊劑、非水性混懸劑(其中可包含助懸劑),或者在水或者糖漿中的混懸劑存在。在希望的情況下,可包含矯味劑、防腐劑、助懸劑、增稠劑或者乳化劑。用于口服給藥的液體分散體可為糖漿劑、乳劑或者混懸劑。糖漿劑可例如含有蔗糖或者包含甘油和/或甘露醇和/或山梨醇的蔗糖作為載體。具體地,作為載體,用于糖尿病患者的糖漿劑可僅含不代謝成葡萄糖或者僅很少量地代謝成葡萄糖的產物,例如山梨醇。混懸劑和乳劑可含有載體,例如天然樹膠、瓊脂、藻酸鈉、果膠、甲基纖維素、羧甲基纖維素或者聚乙烯醇。哌甲酯以多種劑型和以多種劑量強度,作為d-和l-蘇-哌甲酯的外消旋混合物或者作為單一d-蘇-異構體市售(表1)。推薦的日劑量取決于劑型、活性成分(單一異構體或者外消旋混合物)和單個患者滴定。表1.市售哌甲酯劑型和劑量強度的實例。本發明技術的前藥的劑量與未結合的哌甲酯的劑量相比可較高或者較低,取決于它們的分子量、作為全部綴合物或者綴合物鹽的一部分的哌甲酯的相應的重量百分數和它們的生物利用度(關于釋放的哌甲酯)。因此,劑量與游離哌甲酯的劑量相比可較高或者較低。劑量可基于哌甲酯鹽酸鹽的劑量強度(其每劑量為例如,但不限于,約2.5mg至約54mg)計算。從哌甲酯鹽酸鹽至哌甲酯前藥的劑量轉化可使用下面的方程式實施:mph=哌甲酯mw=分子量fba=解決在未修飾的哌甲酯和本發明技術的前藥之間的生物利用度差異的校正因數。此校正因數對于每種前藥是特異性的。本發明技術的結合的哌甲酯或者前藥的適合的劑量包括但不限于包含與未結合的哌甲酯的量等摩爾的結合的哌甲酯的量的制劑,約0.5mg或者更高,可選擇地約2.5mg或者更高,可選擇地約5.0mg或者更高,可選擇地約7.5mg或者更高,可選擇地約10mg或者更高,可選擇地約20mg或者更高,可選擇地約30mg或者更高,可選擇地約40mg或者更高,可選擇地約50mg或者更高,可選擇地約60mg或者更高,可選擇地約70mg或者更高,可選擇地約80mg或者更高,可選擇地約90mg或者更高,可選擇地約100mg或者更高,并包含其任何額外增量,例如,約0.1、約0.2、約0.25、約0.3、約0.4、約0.5、約0.6、約0.7、約0.75、約0.8、約0.9或者約1.0mg及其相乘因數(例如,約×1、約×2、約×2.5、約×5、約×10、約×100等)。本發明技術還包括包含目前批準的哌甲酯制劑(參見表1)的劑量制劑,其中劑量可使用通過哌甲酯鹽酸鹽的量測定的上述方程式計算。本發明技術提供作為單一療法或者作為組合療法配制的劑型。在一些實施方案中,與未結合的哌甲酯相比,哌甲酯和含氧酸結合以形成前藥具有一個或者多個優點,包括但不限于減少的或者改善的副作用分布、形成較少的潛在毒性代謝物、形成較少的惰性代謝物、改善的水溶性、減少的藥物濫用可能性和/或在血漿濃度方面減少的患者間差異性。合成方案在一些實施方案中,可使一個或者多個保護基團與可干擾與哌甲酯偶聯的任何另外的反應性官能團連接。取決于官能團類型和反應條件,可使用任何適合的保護基團。適用于本發明技術的一些保護基團包括但不限于乙酰基(ac)、叔丁氧基羰基(boc)、芐基氧基羰基(cbz)、對甲氧基芐基羰基(moz)、9-芴基甲基氧基羰基(fmoc)、芐基(bn)、對甲氧基芐基(pmb)、3,4-二甲氧基芐基(dmpm)、對甲氧基苯基(pmp)、甲苯磺酰基(ts),或者酰胺基團(如乙酰胺基團、鄰苯二甲酰胺基團等)。在其它實施方案中,在本發明哌甲酯的前藥的合成方案中的任何步驟可需要堿。適合的堿包括但不限于4-甲基嗎啉(nmm)、4-(二甲基氨基)吡啶(dmap)、n,n-二異丙基乙基胺、二(三甲基甲硅烷基)氨基鋰、二異丙基氨基鋰(lda)、任何堿金屬叔丁氧化物(例如,叔丁醇鉀)、任何堿金屬氫化物(例如,氫化鈉)、任何堿金屬烷氧化物(例如,甲醇鈉)、三乙胺或者任何其它叔胺。在本發明哌甲酯的前藥的合成方案中的任何步驟可用于任何反應的適合的溶劑包括但不限于丙酮、乙腈、丁醇、氯仿、二氯甲烷、二甲基甲酰胺(dmf)、二甲基亞砜(dmso)、二噁烷、乙醇、乙酸乙酯、乙醚、庚烷、己烷、甲醇、甲基叔丁基醚(mtbe)、異丙醇、乙酸異丙酯、二異丙基醚、四氫呋喃、甲苯、二甲苯或者水。在一些實施方案中,可使用酸除去某些保護基團。適合的酸包括但不限于鹽酸、氫溴酸、氫氟酸、氫碘酸、硫酸、磷酸、三氟乙酸、乙酸、檸檬酸、甲磺酸、對甲苯磺酸和硝酸。對于某些其它保護基團,可使用催化氫化,例如,在氫氣存在下的鈀/炭。在一個實施方案中,使含氧酸與哌甲酯連接的一般合成包括以下反應。向哌甲酯的氨基甲酸碘甲酯(1-1.5mmol)在甲苯(25-50ml)中的溶液添加相應的含氧酸的銀鹽(3當量)。取決于含氧酸,將反應混合物從80℃加熱至回流并保持3小時。隨后,過濾固體并濃縮濾液。將殘留物通過柱色譜純化,得到連接的含氧酸-哌甲酯綴合物。取決于含氧酸,所述綴合物為最終產物或者需要脫保護。例如,保護磷酸酯綴合物的芐基通過以下方法除去:在甲醇中使用氫氣氣球用10%pd/c氫化2小時。過濾催化劑,將濾液濃縮并干燥,得到最終脫保護的綴合物。在一些實施方案中,所述前藥為親水的并因此比未結合的哌甲酯更易溶于水。在一些實施方案中,用于合成具有烷基或者芳基(3)的哌甲酯(mph)的氨基甲酸酯衍生物的一般操作如下:在室溫向哌甲酯鹽酸鹽(mph·hcl)(1mmol)和三乙胺(tea)(4mmol)在二氯甲烷(dcm)(8ml)中的溶液滴加氯甲酸酯2(2mmol)在dcm(2ml)中的溶液。在4-6小時后,將反應混合物用水(1ml)淬滅并攪拌15分鐘。減壓蒸發溶劑。將殘留物溶解在乙酸乙酯(etoac)(50ml)中并用5%碳酸氫鈉水溶液(nahco3)(2×40ml)和鹽水(1×40ml)洗滌。將有機相在硫酸鈉(na2so4)下干燥并真空濃縮。將油狀殘留物通過硅膠色譜或者制備性hplc純化。在其它實施方案中,4-氟苯酚-co-mph(3b)的合成如下:在室溫向mph·hcl(0.25g,0.93mmol)和tea(0.52ml,3.7mmol)在dcm(8ml)中的溶液滴加氯甲酸4-氟苯基酯(0.33g,1.86mmol)在dcm(3ml)中的溶液。在室溫將反應混合物攪拌6小時,然后用水(1ml)淬滅。減壓蒸發溶劑。將殘留物溶解在etoac(50ml)中并用5%nahco3水溶液(2×40ml)和鹽水(1×40ml)洗滌。將有機相在na2so4下干燥并真空濃縮。將油狀殘留物通過制備性hplc純化,得到3b(0.35g)。在一些實施方案中,用于合成具有羥基羧酸(8)的mph的氨基甲酸酯衍生物的一般操作如下:向經保護的羥基酸4(1mmol)在dcm(8ml)中的溶液添加tea(2.5mmol),并將溶液冷卻至0℃。在0℃滴加氯甲酸4-硝基苯基酯(5,1mmol)在dcm(2ml)中的溶液。在添加后,使反應混合物緩慢達到室溫并留置過夜。將溶劑蒸發并真空干燥,得到碳酸酯衍生物6。將化合物6溶解在二甲基甲酰胺(dmf)中并向此溶液添加tea(3mmol)和mph·hcl(1.05mmol)。將混合物在75℃加熱8小時。減壓除去溶劑。將殘留物溶解在etoac(60ml)中并用5%nahco3水溶液(2×40ml)和鹽水(1×40ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到8,其通過制備性hplc純化。在其它實施方案中,mph-co-l-乳酸酯(8b,a=-ch(ch3)-)的合成如下:向乳酸芐基酯4(a=-ch(ch3)-;0.39g,2mmol)在dcm(8ml)中的溶液添加tea(0.69ml,5mmol),并將溶液冷卻至0℃。在0℃滴加氯甲酸4-硝基苯基酯5(0.436g,2.1mmol)在dcm(3ml)中的溶液。隨后,使反應混合物緩慢達到室溫并留置過夜。將溶劑真空蒸發并干燥,得到碳酸酯衍生物6(a=-ch(ch3)-)。將化合物6溶解在dmf(12ml)中并向溶液添加tea(0.84ml,6mmol)和mph·hcl(0.604g,2.23mmol)。在65℃將混合物加熱20小時。減壓除去溶劑。將殘留物溶解在etoac(40ml)中并用5%nahco3水溶液(2×30ml)和鹽水(1×30ml)洗滌。將有機相用na2so4干燥,蒸發至干并通過制備性hplc純化,得到8b(0.62g)。在其它實施方案中,用于合成具有羥基羧酸連接體(11)的mph的氨基酸衍生物的一般操作如下:向8(1mmol)、h-aa-otbu(aa=氨基酸)(9,1.1mmol)、n-羥基琥珀酰亞胺(nhs)(1.1mmol)在thf(8ml)中的溶液添加tea(2mmol),并將混合物攪拌10分鐘。隨后,添加n,n'-二環己基碳二亞胺(dcc)(1.1.mmol)在thf(2ml)中的溶液,并將混合物在室溫攪拌過夜。過濾反應混合物,并將濾液蒸發至干,得到經保護的衍生物10,其通過制備性hplc純化。將化合物10溶解在4nhcl/二噁烷溶液(8ml)中,并將溶液在室溫攪拌6小時。將溶液在真空下蒸發,與乙酸異丙酯共蒸發并干燥,得到11。在一些實施方案中,mph-co-乳酰基-lys(11a;a=-ch(ch3)-,r=-(ch2)4nh2)的合成如下:向8b(0.12g,0.34mmol)、h-lys(boc)-otbu·hcl9(0.145g,0.37mmol)、nhs(0.044g,0.37mmol)在thf(8ml)中的溶液添加tea(0.15ml,1.02mmol)并將混合物攪拌10分鐘。隨后,添加dcc(0.076g,0.37mmol)在thf(2ml)中的溶液并將混合物在室溫攪拌過夜。過濾反應混合物,并將濾液蒸發至干。將粗產物通過制備性hplc純化,得到10a(0.14g)。將化合物10a(a=-ch(ch3)-,r=-(ch2)4nh2)(0.135g)溶解在4nhcl/二噁烷(8ml)中,并將溶液在室溫攪拌6小時。將溶液真空蒸發,與乙酸異丙酯(ipac)共蒸發并干燥,得到11a(0.12g)。在其它實施方案中,mph-co-乳酰基-ala(11b;a=-ch(ch3)-,r=-ch3)的合成如下:向8b(0.12g,0.34mmol)、h-ala-otbu·hcl9(0.0.065g,0.36mmol)、nhs(0.044g,0.37mmol)在thf(8ml)中的溶液添加tea(0.15ml,1.02mmol)并將混合物攪拌10分鐘。隨后,添加dcc(0.075g,0.36mmol)在thf(2ml)中的溶液,并將反應混合物在室溫攪拌過夜。過濾懸浮液,并將濾液蒸發至干。將粗產物通過制備性hplc純化,得到10b(a=-ch(ch3)-,r=-ch3)(0.095g)。將化合物10b(a=-ch(ch3)-,r=-ch3)(0.09g)溶解在4nhcl/二噁烷(8ml)中,并將溶液在室溫攪拌4小時。將溶液真空蒸發,與乙酸異丙酯(ipac)共蒸發并干燥,得到11b(0.085g)。在其它實施方案中,用于合成具有氨基醇(15)的mph的氨基甲酸酯衍生物的一般操作如下:向氨基醇12(1mmol)在dcm(8ml)中的溶液添加tea(2.5mmol)并將溶液冷卻至0℃。在0℃滴加氯甲酸4-硝基苯基酯(5,1mmol)在dcm中的溶液。隨后,使反應混合物緩慢達到室溫并在室溫留置過夜。將溶劑真空蒸發并干燥,得到碳酸酯衍生物13。將化合物13溶解在dmf中并向此溶液添加tea(3mmol)和mph·hcl(1.05mmol)。將混合物在65℃加熱15小時。減壓除去溶劑。將殘留物溶解在etoac(40ml)中并用5%nahco3水溶液(2×30ml)和鹽水(1×30ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到14,其通過制備性hplc純化。將化合物14溶解在4nhcl/二噁烷中,并將溶液在氬氣下攪拌3-6h,取決于氨基酸衍生物。將溶劑蒸發,與ipac共蒸發并干燥,得到15。在其它實施方案中,所述酪胺-co-mph(19)的合成如下:向boc-酪胺16(1mmol)在dcm(8ml)中的溶液添加tea(2.5mmol)并將溶液冷卻至0℃。在0℃滴加氯甲酸4-硝基苯基酯(5,1mmol)在dcm中的溶液。隨后,除去冰浴并將反應混合物在室溫攪拌4小時。將溶劑在真空下蒸發并干燥,得到碳酸酯衍生物17。將化合物17溶解在dmf中并向此溶液添加tea(3mmol)和mph·hcl(1.05mmol)。將混合物在65℃加熱15小時。減壓除去溶劑。將殘留物溶解在etoac(40ml)中并用5%nahco3水溶液(2×30ml)和鹽水(1×30ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到18,其通過制備性hplc純化。將化合物18用4nhcl/二噁烷脫保護,得到19(0.38g)。在一些實施方案中,琥珀酸-酪胺-co-mph(20)的合成如下:向19(0.1g,0.23mmol)和tea(0.095ml,0.69mmol)在thf(8ml)中的溶液添加琥珀酸酐(0.025g,0.25mmol)并將反應混合物在室溫攪拌3小時。減壓蒸發溶劑并將殘留物溶解在etoac(50ml)中。將etoac相用1%硫酸氫鈉水溶液(nahso4)(50ml)、鹽水(50ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到20(0.11g),為白色固體。在其它實施方案中,具有氨基醇連接體(23和25)的mph的羧酸衍生物的合成的一般操作如下:向15(1mmol)在thf中的溶液添加tea(2.5mmol)和boc-aa-osu(aa=氨基酸)(21,1.05mmol)并將溶液在室溫攪拌3小時。真空蒸發溶劑。將殘留物溶解在etoac(50ml)中并用5%nahco3水溶液(2×30ml)和鹽水(1×40ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到22。在純化后,將化合物21溶解在4nhcl/二噁烷中并在室溫攪拌3-6小時。蒸發溶劑,將殘留物與ipac共蒸發并干燥,得到23。在一些實施方案中,lys-丙氨酸醇-co-mph(23;a=-ch2ch(ch3)-,r1=-(ch2)4nh2)的合成如下:向15b(0.09g,0.24mmol)在thf中的溶液添加tea(2.5mmol)和boc-lys(boc)-osu21(0.113g,0.25mmol)并將溶液在室溫攪拌3小時。真空蒸發溶劑。將殘留物溶解在etoac(50ml)中并用5%nahco3水溶液(2×30ml)和鹽水(1×40ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到22(a=-ch2ch(ch3)-,r1=-(ch2)4nh2)。在純化后,將化合物22(0.135g)溶解在4nhcl/二噁烷中并在室溫攪拌2小時。蒸發溶劑,將殘留物與ipac共蒸發并干燥,得到23(0.13g)。在其它實施方案中,煙酸-乙醇胺-co-mph(25a;r2=3-吡啶基)的合成如下:向15a(0.1g,0.28mmol)和tea(0.15ml,1.12mmol)在dcm(8ml)中的溶液添加煙酰氯(0.055g,0.31mmol)。在室溫攪拌2h后,用水(1ml)淬滅反應混合物并將溶劑蒸發至干。將殘留物溶解在etoac(60ml)中并用5%nahco3水溶液(2×50ml)和鹽水(1×50ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到煙酸衍生物25a(0.13g)。在一些實施方案中,琥珀酸-乙醇胺-co-mph(25b;r2=-(ch2)2co2h)的合成如下:向15a(0.11g,0.31mmol)和tea(0.13ml,0.9mmol)在thf(8ml)中的溶液添加琥珀酸酐(0.034g,0.34mmol)并將反應混合物在室溫攪拌3小時。用水淬滅反應混合物并減壓蒸發溶劑。將殘留物溶解在etoac(50ml)中并用1%nahso4水溶液(2×40ml)、鹽水(50ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到25b(0.12g),為固體。在其它實施方案中,甘油-co-mph(29)的合成如下:將1,2-異亞丙基甘油26(0.265g,2mmol)和tea(0.55ml,4mmol)在dcm(8ml)中的溶液冷卻至0℃。隨后,滴加氯甲酸4-硝基苯基酯5(0.425g,2mmol)在dcm中的溶液。除去冰浴并將反應混合物在室溫攪拌5小時。真空蒸發溶劑并干燥,得到碳酸酯衍生物27。將化合物27溶解在dmf中并向此溶液添加tea(0.69ml,5mmol)和mph·hcl(0.502g,1.85mmol)。將混合物在70℃加熱15小時。減壓除去溶劑。將殘留物溶解在etoac(70ml)中并用5%nahco3水溶液(2×50ml)和鹽水(1×50ml)洗滌。將有機部分用na2so4干燥并蒸發至干,在通過制備性hplc純化后得到氨基甲酸酯衍生物28(0.61g)。將異亞丙基衍生物28(0.6g)溶解在甲醇(meoh)(20ml)中并向此溶液添加甲苯磺酸一水合物(tsoh·h2o)(0.035g)。在室溫攪拌3小時后,用5%nahco3水溶液(1ml)淬滅反應混合物并將溶劑蒸發至干。將殘留物溶解在etoac(70ml)中并用5%nahco3水溶液(2×50ml)和鹽水(1×50ml)洗滌。將有機相用na2so4干燥并蒸發至干,得到甘油衍生物29(0.46g)。在其它實施方案中,具有聚(乙二醇)衍生物的mph的氨基甲酸酯綴合物(32)的合成如下:在一些實施方案中,me-peg-co-mph(32a)的合成如下:在室溫向me-peg(聚(乙二醇)甲基醚)30(1mmol)和tea(2mmol)在dcm(8ml)中的溶液滴加氯甲酸4-硝基苯基酯5(1.05mmol)在dcm(3ml)中的溶液。將溶液在室溫攪拌過夜。真空蒸發溶劑并干燥,得到碳酸酯衍生物31。將化合物31溶解在dmf中并向此溶液添加tea(3mmol)和mph·hcl(1.05mmol)。將混合物在70℃加熱15小時。減壓除去溶劑。將油狀殘留物通過制備性hplc純化,得到32a,為油狀物。在其它實施方案中,me-(och2ch2)3-oco-mph(32b;n=3)的合成如下:在室溫向me-peg30(n=3;0.165g,1mmol)和tea(0.3ml,2mmol)在dcm(8ml)中的溶液滴加氯甲酸4-硝基苯基酯5(0.212g,1.05mmol)在dcm(3ml)中的溶液。將溶液在室溫攪拌過夜。真空蒸發溶劑并干燥,得到碳酸酯衍生物31(n=3)。將化合物31溶解在dmf中并向此溶液添加tea(0.42ml,3mmol)和mph·hcl(0.273g,1.05mmol)。將混合物在75℃加熱6小時。減壓除去溶劑。將油狀殘留物通過制備性hplc純化,得到32b(n=3)(0.24g),為油狀物。在一些實施方案中,h2n-peg-co-mph(34)的合成如下:向o-[2-(boc-氨基)乙基]-o′-(2-羧基乙基)聚乙二醇(boc-nh-peg-co2h)33(0.12g,0.26mmol)、mph·hcl(0.93g,0.35mmol)、1-羥基苯并三唑(hobt)(0.035g,0.26mmol)和tea(0.11ml,0.78mmol)在dmf(6ml)中的溶液滴加dcc(0.056g,0.27mmol)溶液。將反應混合物在室溫攪拌2天。過濾懸浮液并將濾液真空蒸發至干。將殘留物純化并用4nhcl/二噁烷脫保護,得到酰胺衍生物34(0.13g),為油狀物。在其它實施方案中,me-peg-nh-琥珀酰基-丙氨酸醇-co-mph(36)的合成如下:向15b(0.075g,0.2mmol)和tea(0.085ml,0.6mmol)在thf(8ml)中的溶液添加o-[(n-琥珀酰亞氨基)琥珀酰基-氨基乙基]-o′-甲基聚乙二醇(me-peg-suc-osu)35(平均mp=750,0.15g,0.2mmol)并將反應混合物在室溫攪拌2天。減壓蒸發溶劑并通過制備性hplc純化殘留物,得到36,為油狀物。在一些實施方案中,6-氨基己酸-ch2oco-mph(40)的合成如下:a.boc-6-氨基己酸銀鹽的合成:將boc-6-氨基己酸(0.85g,3.68mmol)添加至水(4ml)并在冰浴中冷卻。在恒定攪拌下向此懸浮液添加1nnaoh,直到溶液的ph約為7并且混合物變為澄清溶液。向此溶液緩慢添加硝酸銀(0.63g,3.68mmol)的水(2ml)溶液。將所得析出物過濾并用水洗滌。將固體用五氧化二磷真空干燥,得到白色固體(1.09g)(收率,88%)。b.2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸氯甲基酯(37)的合成:將哌甲酯鹽酸鹽(1)(2.70g,10mmol)懸浮在dcm(75ml)中并在冰浴中冷卻。添加4-二甲基氨基吡啶(dmap)(4.887g,40mmol),并將所得混合物攪拌10分鐘。緩慢添加氯甲酸氯甲基酯(3.224g,25mmol)的dcm(10ml)溶液。除去冰浴并將反應混合物在室溫攪拌5小時。添加乙酸乙酯(250ml),然后添加水(20ml),以淬滅反應混合物。將乙酸乙酯層分離并用1nhcl(40ml)和鹽水(2×40ml)洗滌并用無水硫酸鈉干燥。蒸發溶劑并通過硅膠柱色譜(己烷:etoac,3:1)純化殘留物,得到37,為無色油狀物(2.60g)(收率,80%)。c.2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸碘甲基酯(38)的合成:將37(0.28g,0.86mmol)和碘化鈉(0.387g,2.58mmol)在丙酮(6ml)中的混合物攪拌過夜。蒸發丙酮。將殘留物溶解在乙酸乙酯(80ml)中并用飽和硫酸氫鈉(30ml)和鹽水(30ml)洗滌并用無水硫酸鈉干燥。蒸發溶劑并真空干燥殘留物,得到38,為糖漿劑(0.263g)(收率,73%)。d.boc-6-氨基己酸-ch2oco-mph(39a)的合成:將38(0.43g,1.03mol)和boc-6-氨基己酸銀鹽(1.05g,3.09mmol)在甲苯(30ml)中的混合物回流3小時。過濾固體并將濾液濃縮至干。將粗殘留物通過制備性hplc純化,得到39a,為吸濕固體(0.375g)(收率,70%)。e.6-氨基己酸-ch2oco-mph(40)的合成:在室溫將化合物39a(0.21g,0.40mmol)與4nhcl/二噁烷(5-6ml)一起攪拌2小時。將溶劑濃縮至干,得到40,為吸濕固體(0.166g)(收率,91%)。在其它實施方案中,乳酸-ch2oco-mph(39b)的合成如下:將化合物38(0.428g,1.03mmol)和乳酸銀(0.61g,3.09mmol)在30ml甲苯中的混合物在80-90℃加熱3小時。過濾固體并將濾液濃縮至干。將粗殘留物通過制備性hplc純化,得到39b,為漿狀物(0.28g)(收率,64%)。在一些實施方案中,用于合成哌甲酯-1-羧酸(6-氨基己酰氧基)甲基酯綴合物的氨基酸和肽衍生物(42)的一般操作如下:在n-甲基嗎啉(nmm)(3當量)的存在下在thf中,在室溫將40的鹽酸鹽(1當量)用boc保護的氨基酸或者肽的琥珀酰亞氨基酯(1.05當量)處理2-12小時。將反應混合物濃縮至干,將粗殘留物吸收在etoac中并用飽和碳酸氫鹽、氯化銨溶液和鹽水洗滌。將有機層用無水硫酸鈉干燥并濃縮至干,得到boc保護的氨基酸或者肽衍生物41。在室溫將boc保護的衍生物41使用4nhcl/二噁烷脫保護2-3小時。將溶劑蒸發至干,得到氨基酸或者肽衍生物的鹽酸鹽42。在其它實施方案中,val-6-氨基己酸-ch2oco-mph(42a)的合成如下:a.合成boc-val-6-氨基己酸-ch2oco-mph(41a):將化合物40(0.08g,0.175mmol)吸收在無水thf(10ml)中。添加nmm(0.06ml,0.525mmol)和boc保護的琥珀酰亞氨基酯(0.06g,0.184mmol)并將反應混合物在室溫攪拌2小時。將溶劑濃縮至干并將粗產物吸收在乙酸乙酯(100ml)中,用飽和碳酸氫鹽(40ml)、氯化銨溶液(40ml)和鹽水(40ml)各洗滌一次。將有機層用無水硫酸鈉干燥并濃縮至干,得到41a(0.084g)(收率,77%)。b.合成val-6-氨基己酸-ch2oco-mph(42a):將化合物41a(0.084g,0.14mmol)溶解在4nhcl/二噁烷(4-5ml)中并在室溫攪拌2小時。將二噁烷濃縮至干,得到42a(0.078g)(收率,100%)。在其它實施方案中,用于合成哌甲酯的氨基酸和肽綴合物的一般操作(44)如下:將哌甲酯鹽酸鹽(1當量)吸收在無水dmf中。添加boc保護的氨基酸或者肽(1.05當量)、dcc(1.05當量)、hobt(1.1當量)和tea(2.5當量)。將混合物在室溫攪拌過夜。真空蒸發dmf并將殘留物溶解在乙酸乙酯中。將有機層用1%硫酸氫鈉和鹽水洗滌。將有機層濃縮至干,得到boc保護的綴合物。boc基團通過以下方法脫保護:在室溫用4nhcl/二噁烷處理2-3小時。將二噁烷蒸發至干,得到哌甲酯的氨基酸或者肽的衍生物(44)。在一些實施方案中,ala-mph(44a)的合成如下:a.合成boc-ala-mph(43a):將哌甲酯鹽酸鹽(0.274g,1.02mmol)吸收在無水dmf(10ml)中。添加boc-ala-oh(0.20g,1.07mmol)、tea(0.35ml,2.54mmol)、hobt(0.15g,1.11mmol)和dcc(0.22g,1.07mmol)。將反應混合物在室溫攪拌過夜。將dmf蒸發至干并將殘留物吸收在etoac(200ml)中,并用1%硫酸氫鈉(60ml)和鹽水(60ml)各洗滌一次。將有機層用無水硫酸鈉干燥并濃縮至干,得到43a(0.37g)(收率,90%)。b.合成ala-mph·hcl(44a):將化合物43a(0.37g)吸收在4nhcl/二噁烷(8ml)中并在室溫攪拌2小時。將二噁烷蒸發至干,得到44a(0.31g)(收率,100%)。在其它實施方案中,用于合成包含或者不含連接體的哌甲酯的1,3-二甘油酯衍生物(羧酸的鏈長優選為c14或者更長)的一般操作如下:1,3-二甘油酯(45)的羥基可用氯甲酸對硝基苯基酯活化。然后可將活化的1,3-二甘油酯46在tea的存在下在dmf中用哌甲酯鹽酸鹽處理,得到相應的氨基甲酸酯衍生物47。1,3-二甘油酯的實例包括但不限于1,3-二棕櫚酸甘油基酯、1,3-二硬脂酸甘油基酯或者1-棕櫚酰基-3-硬脂酰基-甘油。在一些實施方案中,具有羥基羧酸連接體的mph的1,3-二甘油酯衍生物(48)的合成如下:具有游離末端羧酸基團的哌甲酯和連接體的氨基甲酸酯也可與1,3-二甘油酯衍生物連接。例如,使用dcc和dmap,在dcm中,可使具有羥基羧酸的哌甲酯氨基甲酸酯綴合物與1,3-二甘油酯偶聯,得到相應的脂肪酸甘油衍生物48。1,3-二甘油酯的實例包括但不限于1,3-二棕櫚酸甘油基酯、1,3-二硬脂酸甘油基酯或者1-棕櫚酰基-3-硬脂酰基-甘油。在其它實施方案中,用于合成具有-c(o)och2o-連接體的哌甲酯綴合物的一般操作如下:向哌甲酯的氨基甲酸碘甲基酯38(1-1.5mmol)在甲苯(25-50ml)中的溶液添加酸的銀鹽(3當量)。將混合物從80℃加熱至回流并保持3小時,取決于酸的銀鹽。在反應結束后,過濾固體并濃縮濾液。將殘留物通過柱純化,得到所述綴合物。所述綴合物為最終產物或者需要脫保護。在這些操作中的所有保護基團為芐基,但是也可使用其它保護基團。使用氫氣球,將在甲醇中的綴合物用10%pd/c氫化2小時。過濾催化劑。將濾液濃縮并干燥,得到最終綴合物49。在一些實施方案中,磷酸-ch2oco-mph(49a)(其結構在下面示出)的合成如下在步驟a、b和c中:a.合成磷酸銀二芐基酯:將磷酸二芐基酯(2.78g,10mmol)的水(40ml)溶液在冰浴中冷卻。隨后,添加1nnaoh,同時振搖燒瓶,直到溶液的ph約為7。固體幾乎完全溶解。然后緩慢添加硝酸銀(1.89g,11mmol)的水(20ml)溶液。在添加后,將所的固體通過過濾收集并用水洗滌。將固體用五氧化二磷真空干燥,得到磷酸銀二芐基酯(3.18g)(收率,82.5%),為白色固體。b.合成(bno)2-磷酸-ch2oco-mph:將2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸碘甲基酯38(0.260g,0.62mmol)和磷酸銀二芐基酯(0.719g,1.87mmol)的甲苯(20ml)溶液回流1.5小時。過濾固體。濃縮濾液并將殘留物通過硅膠柱色譜(己烷:etoac,3:1至1:1)純化,得到經保護的綴合物(0.27g)(收率,76.3%),為無色油狀物。c.合成磷酸-ch2oco-mph(49a):使用氫氣球,將2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸(二(芐基氧基)磷酰基氧基)甲基酯(0.267g,0.47mmol)的甲醇(8ml)溶液在10%pd/c(干燥,90mg)下氫化2小時。通過硅藻土過濾催化劑。將濾液蒸發至干,得到49a(0.136g)(收率,74.6%),為白色無定形固體。在一些實施方案中,煙酸-ch2oco-mph·hcl(49b)(其結構在下面示出)的合成如下在步驟a和b中:a.合成煙酸-ch2oco-mph,其結構在下面示出:將2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸碘甲基酯38(0.457g,1.10mmol)和煙酸銀(0.755g,3.28mmol)的甲苯(20ml)溶液回流2小時。過濾固體。濃縮濾液并通過硅膠柱色譜(己烷:etoac,2:1至1:1)純化殘留物,得到游離堿形式的49b(0.256g)(收率,56.7%),為無色油狀物。b.合成煙酸-ch2oco-mph·hcl(49b):用1.25nhcl/meoh(0.75ml,0.93mmol)處理煙酸(2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羰基氧基)甲基酯(0.256g,0.62mmol)的丙酮(8ml)溶液。在室溫蒸發溶劑。將所得殘留物與丙酮(2×3ml)共蒸發,然后溶解在丙酮(0.8ml)中并添加乙醚(20ml)。通過用刮鏟刮擦,固體逐漸形成并通過過濾收集,得到49b(0.180g)(收率,64.6%)。在其它實施方案中,異煙酸-ch2oco-mph·hcl(49c)(其結構在下面示出)的合成如下在步驟a和b中:a.合成異煙酸-ch2oco-mph,其結構在下面示出:在90℃將2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸碘甲基酯38(0.555g,1.33mmol)和異煙酸銀(0.918g,3.99mmol)的甲苯(50ml)溶液加熱1.5小時。通過硅藻土過濾固體。濃縮濾液并通過硅膠柱色譜(己烷:etoac,1.2:1至1:1)純化殘留物,得到游離堿形式的49c(0.286g)(收率,52.1%),為漿狀物。b.合成異煙酸-ch2oco-mph·hcl(49c):用1.25nhcl/meoh(1ml,1.25mmol)處理異煙酸(2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羰基氧基)甲基酯(0.286g,0.62mmol)的甲醇(4ml)溶液。在室溫蒸發溶劑。將殘留物與甲醇(2×5ml)共蒸發并添加丙酮(4ml)。逐漸形成固體并蒸發丙酮。將固體收集并用乙醚(4×2ml)洗滌,得到49c(0.228g)(收率,73.2%),為灰白色固體。在其它實施方案中,棕櫚酸酯-ch2oco-mph(49d)(其結構在下面示出)的合成如下:在95℃將2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸碘甲基酯38(0.472g,1.13mmol)和棕櫚酸銀(1.233g,3.39mmol)的甲苯(50ml)溶液加熱1小時。過濾固體。濃縮濾液并通過硅膠柱色譜(己烷:etoac,5:1)純化殘留物,得到49d(0.48g)(收率,77.8%),為白色固體。在一些實施方案中,沒食子酸-ch2oco-mph(49e)(其結構在下面示出)的合成如下:在85℃將2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸碘甲基酯38(0.477g,1.14mmol)和3,4,5-三(芐基氧基)苯甲酸銀(1.877g,3.43mmol)的甲苯(50ml)溶液加熱1小時。通過硅藻土過濾固體。濃縮濾液并通過硅膠柱色譜(己烷:etoac,3:1)純化殘留物,得到0.55g無定形固體,將其在10%pd/c(干燥,150mg)下在甲醇(25ml)中用氫氣球氫化2小時。通過硅藻土過濾催化劑。將濾液蒸發至干,得到49e(0.315g)(收率,60.1%),為無定形固體。在其它實施方案中,磷酸-(對-水楊酸)-ch2oco-mph(49f)(其結構在下面示出)的合成如下:在90℃將2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羧酸碘甲基酯38(0.47g,1.13mmol)和4-(二(芐基氧基)磷酰基氧基)苯甲酸銀(1.01g,2mmol)的甲苯(50ml)溶液加熱1小時。通過硅藻土過濾固體。濃縮濾液并通過硅膠柱色譜(己烷:etoac,3:1-2:1)純化殘留物,得到0.45g無色油狀物,將其在10%pd/c(干燥,100mg)下在甲醇(15ml)中用氫氣球氫化1小時。通過硅藻土過濾催化劑。蒸發濾液,得到49f(0.326g)(收率,56.8%),為無定形固體。在一些實施方案中,用于合成哌甲酯的吡啶鎓型綴合物的一般操作如下:r1=h,-co2et,-conh2,-co2tbu,-co-gly-ala-otbu,-co-val-otbu,-co-asp(otbu)-otbur2=-co-gly-ala,-co-val,-co-asp,-co2h在70℃將哌甲酯的氨基甲酸氯甲基酯37(1-1.5mmol)和吡啶或者吡啶衍生物50(1-7mmol)在乙腈(6-10ml)中加熱3.5小時至48小時。在反應結束后,蒸發溶劑。純化殘留物,得到所述綴合物。所述綴合物為最終產物或者需要脫保護。用于這些反應的所有保護基團為叔丁基,其用4nhcl/二噁烷除去,但是也可使用其它保護基團。在其它實施方案中,mph-co2ch2-吡啶氯化物(51a)(其結構在下面示出)的合成如下:在70℃將哌甲酯的氨基甲酸氯甲基酯37(0.326g,1mmol)和吡啶(0.566ml,7mmol)的乙腈(6ml)溶液加熱3.5小時。將溶劑蒸發,然后與甲苯(2×5ml)共蒸發。將所得殘留物溶解在dcm(1ml)中并添加叔丁基甲基醚(tbme)(15ml)。將乳狀液體傾出。將殘留物真空干燥,得到51a(0.404g)(收率,99.8%),為無定形固體。在其它實施方案中,mph-co2ch2-煙酰基-oet氯化物(51b)(其結構在下面示出)的合成如下:在70℃將哌甲酯的氨基甲酸氯甲基酯37(0.326g,1mmol)和煙酸乙基酯(0.453g,3mmol)的乙腈(6ml)溶液加熱24小時。蒸發溶劑。將殘留物溶解在dcm(1.5ml)中并添加tbme(40ml)。固體形成并傾出液體。將上面的操作重復兩次。將所得殘留物真空干燥,得到51b(0.325g)(收率,68.1%),為灰白色固體。在一些實施方案中,mph-co2ch2-煙酰胺氯化物(51c)(其結構在下面示出)的合成如下:在70℃將哌甲酯的氨基甲酸氯甲基酯37(0.326g,1mmol)和煙酰胺(0.122g,1mmol)的乙腈(6ml)溶液加熱26小時。蒸發溶劑并向所得殘留物添加etoac(40ml)。通過用刮鏟刮擦,固體逐漸形成并通過過濾收集。將固體用etoac(3×3ml)進一步洗滌并真空干燥,得到51c(0.298g)(收率,66.5%),為灰白色固體。在一些實施方案中,mph-co2ch2-煙酰基-otbu氯化物(51d)(其結構在下面示出)的合成如下:在70℃將哌甲酯的氨基甲酸氯甲基酯37(0.489g,1.5mmol)和煙酸叔丁基酯(0.806g,4.5mmol)的乙腈(10ml)溶液加熱7小時。蒸發溶劑。向殘留物的dcm(1ml)溶液添加tbme(40ml)。將液體傾出并將殘留物溶解在dcm(1ml)中,然后添加tbme(30ml)。將所得固體收集,用tbme(3×4ml)洗滌并真空干燥,得到51d(0.325g)(收率,47.4%),為灰白色固體。在其它實施方案中,mph-co2ch2-煙酰基-gly-ala氯化物(52a)(其結構在下面示出)的合成如下在步驟a、b和c中:a.合成2-(2-(煙酰氨基)乙酰氨基)丙酸叔丁基酯(50e),其結構在下面示出:向h-gly-ala-otbu(0.85g,4.2mmol)的dcm(30ml)溶液添加et3n(1.17ml,8.4mmol)。在冰浴中,逐份添加煙酰氯鹽酸鹽(0.748g,4.2mmol)(4次,歷時20分鐘)。在添加后,在低于5℃將混合物攪拌1小時。添加水(30ml)淬滅反應混合物,然后添加dcm(50ml)。將dcm層用5%nahco3和鹽水(各30ml)進一步洗滌,并用na2so4干燥。蒸發溶劑并通過硅膠柱色譜(6%meoh/dcm)純化殘留物,得到50e(0.881g)(收率,68.3%),為無定形固體。b.合成mph-co2ch2-煙酰基-gly-ala-otbu氯化物(51e),其結構在下面示出:在70℃將哌甲酯的氨基甲酸氯甲基酯37(0.489g,1.5mmol)和2-(2-(煙酰氨基)乙酰氨基)丙酸叔丁基酯50e(0.461g,1.5mmol)的乙腈(10ml)溶液加熱24小時。蒸發溶劑。將殘留物溶解在dcm(1.5ml)中并添加tbme(25ml)。固體形成并傾出液體。將上面的操作重復四次。將固體收集,用tbme(3×2ml)洗滌并真空干燥,得到51e(0.576g)(收率,60.7%),為灰白色固體。c.合成mph-co2ch2-煙酰基-gly-ala氯化物(52a):向51e(0.367g,0.58mmol)的dcm(1ml)溶液添加4mhcl/二噁烷(5ml)。將混合物攪拌2小時。蒸發溶劑。將殘留物溶解在dcm(2ml)中并添加tbme(25ml)。將所得固體收集,用tbme(2×1ml)洗滌并真空干燥,得到52e(0.322g)(收率,96.1%),為固體。在其它實施方案中,mph-co2ch2-煙酰基-val氯化物(52b)(其結構在下面示出)的合成如下在步驟a、b和c中:a.合成3-甲基-2-(煙酰氨基)丁酸叔丁基酯(50f),其結構在下面示出:50f通過與50e相同的操作制備并通過硅膠柱色譜(3%meoh/dcm)純化,得到50f(0.882g,3mmol規模)(收率,98.4%),為漿狀物。b.合成mph-co2ch2-煙酰基-val-otbu氯化物(51f),其結構在下面示出:在70℃將哌甲酯的氨基甲酸氯甲基酯37(0.489g,1.5mmol)和3-甲基-2-(煙酰氨基)丁酸叔丁基酯50f(0.278g,1mmol)的乙腈(10ml)溶液加熱40小時。蒸發溶劑。向殘留物的tbme(5ml)溶液添加己烷(10ml)。將所得固體收集,用tbme/己烷(1:1,6×3ml)洗滌并真空干燥,得到51f(0.464g)(收率,76.8%)。c.合成mph-co2ch2-煙酰基-val氯化物(52b):向51f(0.302g,0.5mmol)的dcm(1ml)溶液添加4nhcl/二噁烷(5ml)。將混合物攪拌5小時。蒸發溶劑。將殘留物溶解在dcm(1.5ml)中并添加tbme(25ml)。將所得固體收集,用tbme(4×2ml)洗滌并真空干燥,得到52b(0.329g)(收率,100%),為固體。在其它實施方案中,mph-co2ch2-煙酰基-gly-asp氯化物(52c)(其結構在下面示出)的合成如下在步驟a、b和c中:a.合成2-(煙酰氨基)琥珀酸二-叔丁基酯(50g),其結構在下面示出:50g通過與50e相同的操作制備。b.合成mph-co2ch2-煙酰基-asp(otbu)-otbu氯化物(51g),其結構在下面示出:在70℃將哌甲酯的氨基甲酸氯甲基酯37(0.489g,1.5mmol)和2-(煙酰氨基)琥珀酸二-叔丁基酯50g(0.35g,1mmol)的乙腈(10ml)溶液加熱24小時。蒸發溶劑。通過硅膠柱色譜(7%meoh/dcm,然后11%meoh/dcm)純化殘留物,得到51g(0.452g)(收率,66.8%),為無定形固體。c.合成mph-co2ch2-煙酰基-asp氯化物(52c):將51g(0.45g,0.67mmol)的4nhcl/二噁烷(5ml)溶液攪拌3小時。蒸發溶劑。將殘留物與dcm(4×5ml)共蒸發,然后溶解在dcm(4ml)中并添加tbme(25ml)。將所得固體收集,用tbme(4×2ml)洗滌并真空干燥,得到52c(0.357g)(收率,95.1%),為固體。在其它實施方案中,mph-co2ch2-煙酸酯氯化物(52d)(其結構在下面示出)的合成如下:將3-(叔丁氧基羰基)-1-((2-(2-甲氧基-2-氧代-1-苯基乙基)哌啶-1-羰基氧基)甲基)吡啶鎓氯化物51d(0.202g,0.4mmol)的4nhcl/二噁烷(5ml)溶液攪拌24小時。蒸發溶劑。將殘留物溶解在dcm(1ml)中并添加tbme(20ml)。將所得固體收集,用tbme(3×1ml)洗滌并真空干燥,得到52d(0.172g)(收率,95.8%),為固體。在一些實施方案中,磷酸-(對-水楊酸)-mph(56)(其結構在下面示出)的合成如下在步驟a、b、c和d中:a.合成bno-對-水楊酸酯-mph(53),其結構在下面示出:將哌甲酯鹽酸鹽(2.698g,10mmol)、4-芐基氧基苯甲酸(2.282g,10mmol)和hobt·h2o(1.532g,10mmol)的thf(60ml)溶液添加至et3n(3.07ml,22mmol),然后添加1-乙基-3-(3-二甲基氨基丙基)碳二亞胺)鹽酸鹽(edci)(2.109g,11mmol)。將混合物攪拌4天。添加etoac(200ml),并將混合物用水(30ml)、5%hoac(50ml)和鹽水(40ml)洗滌。用na2so4干燥etoac層。蒸發溶劑并將殘留物從etoac(12ml)結晶。將固體通過過濾收集并用冷etoac(3×4ml)洗滌,得到53(3.48g)(收率,78.5%),為白色固體。b.合成對-水楊酸酯-mph(54),其結構在下面示出:將53(3.48g,7.85mmol)在10%pd/c(濕,700mg)下在meoh(10ml)和etoac(100ml)中用氫氣球氫化15小時。通過硅藻土過濾催化劑。蒸發濾液,得到54(2.94g),為無定形固體。c.合成(bno)2-磷酸-(對-水楊酸)-mph(55),其結構在下面示出:向54(0.7g,1.98mmol)的dcm(20ml)溶液添加二異丙基氨基亞磷酸二芐基酯(dibenzyldiisopropylphosphoramidite)(0.752g,2.178mmol),然后添加1n-四唑的乙腈溶液(0.45m,4.84ml,2.178mmol)。將混合物攪拌3小時。隨后,添加0.6ml70%tert-buooh/水并攪拌20分鐘。蒸發溶劑。將殘留物的etoac(100ml)溶液用水和鹽水(各30ml)洗滌并用na2so4干燥。蒸發溶劑并通過硅膠柱色譜純化殘留物(etoac:己烷,1.2:1),得到55(0.99g)(收率,81.5%),為漿狀物。d.合成磷酸-(對-水楊酸)-mph(56),其結構在下面示出:將55(0.99g,1.61mmol)在10%pd/c(濕,300mg)下在甲醇(20ml)中用氫氣球氫化3小時。通過硅藻土過濾催化劑。蒸發濾液,得到56(0.675g)(收率,96.5%),為無定形固體。在一些實施方案中,gly-(對-水楊酸)-mph(58)的合成如下在步驟a和b中:a.合成boc-gly-(對-水楊酸)-mph(57),其結構在下面示出:向54(0.353g,1mmol)、boc-gly-oh(0.175g,1mmol)和hobt·h2o(0.153g,1mmol)的thf(10ml)溶液添加et3n(0.15ml,1.1mmol),然后添加edci(0.211g,11mmol)。將混合物攪拌15小時。然后添加另外0.4mmolboc-gly-oh并添加edci,并將混合物再攪拌3小時。添加etoac(100ml),并將混合物用水(2×30ml)和鹽水(30ml)洗滌。用na2so4干燥etoac層。蒸發溶劑并通過硅膠柱色譜(2%meoh/dcm)純化殘留物,得到57(0.452g)(收率,88.5%),為無定形固體。b.合成gly-(對-水楊酸)-mph(58):向57(0.45g,0.88mmol)的dcm(1ml)溶液添加4mhcl/二噁烷(5ml)。將混合物攪拌1小時。蒸發溶劑。將殘留物與dcm(3×5ml)共蒸發,然后溶解在dcm(2ml)中。添加etoac(10ml)和tbme(10ml)。將所得固體收集,用etoac/tbme(1:1,3×2ml)洗滌并真空干燥,得到58(0.329g)(收率,83.5%),為白色固體。藥物試劑盒在一些實施方案中,本發明技術提供藥物試劑盒,其包含本發明技術的前藥或者組合物,所述本發明技術的前藥或者組合物與未結合的哌甲酯相比具有增加的水溶性。在一些實施方案中,在包裝中的特定量的單個劑量含有藥學有效量的本發明技術的前藥或者綴合物。在一些其它實施方案中,試劑盒包含口服薄膜或者條片,所述口服薄膜或者條片包含本發明技術的前藥或者綴合物。本發明技術提供藥物試劑盒,其用于治療或者預防患者中的adhd、add或者戒斷癥狀。患者可為人或者動物患者。適合的人類患者包括兒童患者、老人(老年)患者,和常規患者。試劑盒包含在包裝中的特定量的單個劑量,其含有藥學有效量的至少一種本發明技術的哌甲酯綴合物。試劑盒還可包含試劑盒的使用說明書。單個劑量的特定量可含有約1至約100單個劑量,可選擇地約1至約60單個劑量,可選擇地約10至約30單個劑量,包括約1、約2、約5、約10、約15、約20、約25、約30、約35、約40、約45、約50、約55、約60、約70、約80、約100,并包含其任意額外增量,例如,約1、約2、約5、約10及其相乘因數(例如,約×1、約×2、約×2.5、約×5、約×10、約×100等)。通過參考以下實施例,將更好地理解本申請描述的技術及其優點。提供這些實施例以描述本發明技術的具體實施方案。提供的這些具體實施例不意圖限制本發明技術的范圍和主旨。本領域技術人員應理解的是,本申請所述技術的全部范圍涵蓋本說明書所附的權利要求所限定的主題,和這些權利要求的任何改變、修飾,或者等同物。實施例實施例1:哌甲酯和含氧酸的綴合物的口服藥代動力學(pk)分布的比較本發明技術的示例性前藥綴合物如上所述合成。在大鼠中,在口服給藥后,將從煙酸-ch2oco-mph、磷酸-ch2oco-mph、沒食子酸-ch2oco-mph、乳酸-ch2oco-mph、mph-co2ch2-煙酰基-asp、mph-co2ch2-煙酰基-val、mph-co2ch2-煙酰基-gly-ala、val-6-氨基己酸-ch2oco-mph、mph-co2ch2-煙酰胺、6-氨基己酸-ch2oco-mph、mph-co2ch2-煙酰基-otbu、mph-co2ch2-煙酸酯、mph-co2ch2-煙酰基-oet、mph-co2ch2-吡啶、異煙酸-ch2oco-mph和磷酸-(對-水楊酸)-ch2oco-mph釋放的哌甲酯的口服血漿濃度與未結合的哌甲酯進行比較。向大鼠給藥相當于2mg/kg哌甲酯游離堿的經結合的前藥的口服溶液,并與未結合的哌甲酯鹽酸鹽的等摩爾溶液比較。通過lc-ms/ms測量隨時間推移哌甲酯的血漿濃度。圖13-30示出通過不同哌甲酯綴合物實現的不同pk曲線并與未結合形式比較,以及所有特定藥代動力學參數數據在表2-4中提供。哌甲酯從前藥的釋放取決于與哌甲酯連接的連接體和含氧酸而改變。與未結合的哌甲酯鹽酸鹽相比,通過曲線下面積測量的從前藥釋放的哌甲酯的量的變化為0-185%-auc。用于pk實驗的給藥媒介物如下:圖13-10%tween水溶液。圖14和15-水。圖16–綴合物在50%peg-400水溶液中;對照物:水。圖17-50%peg-400水溶液。圖18-10%tween水溶液。圖19-27-水。圖28和29-磷酸鹽緩沖鹽水(pbs)。圖30-10%tween水溶液。表2在大鼠中經口服強飼法給藥的哌甲酯的前藥的pk參數a用于從三個研究的組合數據計算的磷酸-ch2oco-mph和用于從六個研究的組合數據計算的哌甲酯鹽酸鹽的pk參數。b用于從一個研究的數據計算的沒食子酸-ch2oco-mph和用于從六個研究的組合數據計算的哌甲酯鹽酸鹽的pk參數。表3.在大鼠中鼻內給藥的哌甲酯的前藥的pk參數表4.在大鼠中靜脈內給藥的哌甲酯的前藥的pk參數實施例2:本發明技術的哌甲酯綴合物的水溶性磷酸-ch2oco-哌甲酯和未結合的哌甲酯的水溶性在環境溫度測定,以及結果在表5中。表5.具有含氧酸的哌甲酯綴合物的水溶性化合物在水中的溶解度磷酸-ch2oco-哌甲酯432mg/ml哌甲酯鹽酸鹽169mg/ml未結合的哌甲酯鹽酸鹽的結果與在文獻中發現的溶解度數據(191mg/ml,在32℃)一致。磷酸-ch2oco-哌甲酯綴合物的水溶性是未結合形式的水溶性的約2.5倍。在本說明書中,單數的使用包括復數,除非明確指明。現在以全面、清楚、簡明和準確的術語描述了本申請所述技術,以使本領域任何技術人員能夠實踐本發明。應理解的是,前文描述了本發明技術的優選實施方案,以及可對其進行修飾而不脫離所附權利要求闡述的本發明的主旨或者范圍。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1