一種美洲型豬繁殖與呼吸綜合征病毒的熒光RT?RPA特異性檢測的制作方法
本發明涉及分子生物學和病毒檢測鑒定技術領域,具體涉及一種美洲型豬繁殖與呼吸綜合征病毒的熒光RT-RPA特異性檢測方法、其相應的引物和探針組合以及包含該引物和探針組合的試劑盒。
背景技術:
豬繁殖與呼吸綜合征(Porcine reproductive and respiratory syndrome,PRRS)主要引起懷孕母豬的繁殖障礙和所有日齡豬的呼吸道癥狀,被認為是影響世界養殖業最重要的傳染病之一。引起該病的病原是豬繁殖與呼吸綜合征病毒(PRRSV),是一種具有囊膜的單股正鏈RNA病毒,屬于尼多病毒目,動脈炎病毒科,動脈炎病毒屬。PRRSV于1987年首次分離于北美,然后于1990年分離于西歐。目前,PRRSV遍布全球,成為造成經濟損失最嚴重的豬病之一。根據PRRSV基因和抗原差異,目前將之分為兩個基因型,即歐洲型(基因1型)和美洲型(基因2型)。
我國自1986年首次分離到PRRSV以來,目前該病毒已經遍及全國,并且部分地區豬群的感染率達到90%。2006年,以Nsp2基因出現30個不連續氨基酸缺失為特征的高致病性PRRSV在我國的爆發,對我國養豬業造成了巨大的經濟損失。2006年6月到9月,高致病性PRRSV造成約2,120,000頭豬感染,400,000頭豬死亡,而2007年1月到7月,造成約143,221頭豬的感染,39,455頭豬死亡。截至目前,我國豬群主要流行美洲型PRRSV,并且經典毒株(C-PRRSV)和高致病性毒株(HP-PRRSV)同時存在。隨著我國大型養豬場和集約化養殖模式的發展,對豬病的現場、快速診斷將極大有益于豬場疫病控制,尤其是大型養豬場多位于邊遠地區的情況下。
上述事實清晰表明,對PRRSV的快速、現場診斷極大有益于我國豬場中PRRS的防控。傳統的PRRSV檢測技術,主要是病毒分離、免疫組化和免疫熒光技術,費時費力,對檢測人員技術要求較高,靈敏性低,無法滿足目前快速檢測的需要。
目前對PRRSV的實驗室分子診斷技術主要包括RT-PCR、同時檢測美洲型和歐洲型PRRSV、特異性檢測HP-PRRSV和同時檢測C-PRRSV和HP-PRRSV的熒光RT-PCR,以及特異性針對美洲型PRRSV的RT-LAMP方法。但是,PRRSV快速進化和基因變異使得建立長期有效的RT-PCR方法異常復雜,設計保持足夠敏感性的LAMP引物異常困難,從而導致假陰性檢測結果。同時,RT-PCR和RT-LAMP試劑需要冷鏈運輸、價格高昂的設備和經驗豐富的技術人員,從而難以應用于現場檢測。因此,需要建立一種能夠用于PRRSV現場檢測的操作簡單、快速、準確和成本較低的檢測方法。
技術實現要素:
為了解決上述問題,本發明建立了一種能夠用于現場檢測,操作簡單、快速、特異性強、靈敏性高的PRRSV熒光RT-RPA檢測方法、其相應的引物和探針組合以及包含該引物和探針組合的試劑盒。
本發明采用如下技術方案:
一種用于美洲型豬繁殖與呼吸綜合征病毒的熒光RT-RPA特異性檢測的引物和exo探針組合,其關鍵技術在于,其正向引物序列如SEQ ID No.1所示;反向引物序列如SEQ ID No.2所示;exo探針序列如SEQ ID No.3所示。
一種美洲型豬繁殖與呼吸綜合征病毒熒光RT-RPA特異性檢測的方法,其關鍵技術在于,提取待測樣品的RNA為模板,利用上述的引物及exo探針組合進行擴增及實時熒光檢測。
檢測方法中,向50μL實時RT-RPA反應體系中加入濃度均為10μM的正向引物和反向引物各2.1μL;濃度為10μM的exo探針0.6μL;RNA模板1μL;擴增程序為:使用RPA擴增儀于42℃下反應20分鐘,并在擴增過程中實時收集檢測熒光信號。
一種用于美洲型豬繁殖與呼吸綜合征病毒熒光RT-RPA特異性檢測的試劑盒,其關鍵技術在于,該試劑盒包含上述的引物和exo探針組合。
本發明的有益效果在于:本發明根據美洲型PRRSV ORF7保守序列設計引物和exo探針,基于能夠實現等溫擴增且收集熒光信號的設備,建立了能夠用于現場檢測,操作簡單、快速、特異性強、靈敏性高的PRRSV熒光RT-RPA檢測方法。
附圖說明
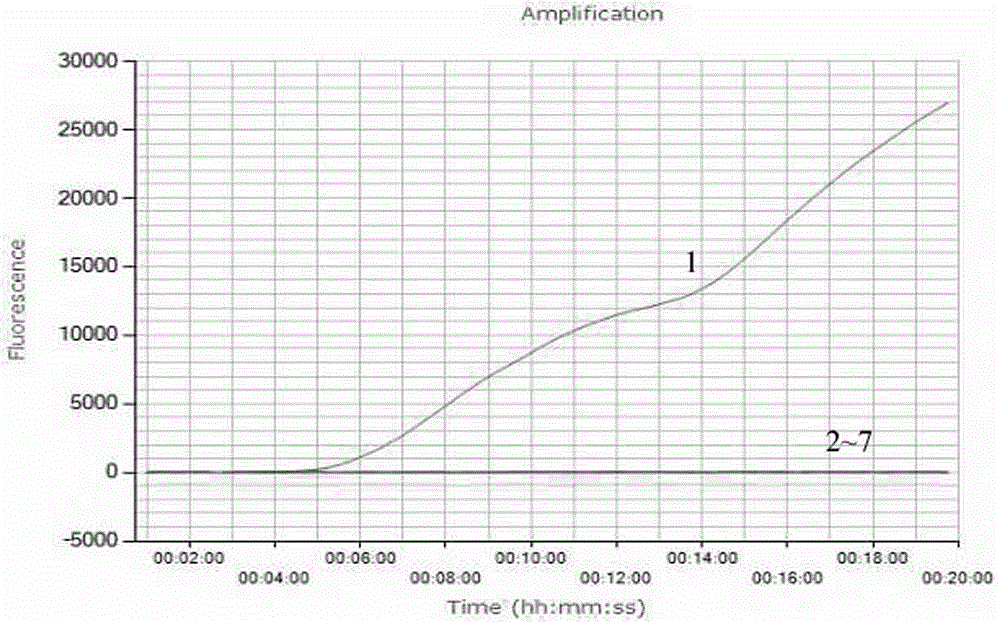
圖1 PRRSV熒光RT-RPA方法的特異性檢測I。
圖1中,1:PRRSV(JXA1-R);2:FMDV;3:CSFV;4:PRV;5:PPV;6:PCV-2;7:豬基因組DNA。
圖2 PRRSV熒光RT-RPA方法的特異性檢測II。
圖2中,1:JXA1-R;2:VR-2332;3:HuN4-F112;4:TJM-F92;5:R98;6:Ch-1R;7:豬基因組DNA。
圖3 PRRSV熒光RT-RPA方法的敏感性檢測結果。
圖4 PRRSV real-time RT-PCR方法的敏感性檢測結果。
圖3和圖4中,1:106copies RNA;2:105copies RNA;3:104copies RNA;4:103copies RNA;5:102copies RNA;6:101copies RNA;7:100copies RNA。
具體實施方式
下面結合實施例對本發明進行詳細說明。本發明保護范圍不限于實施例,本領域技術人員在權利要求限定的范圍內做出任何改動也屬于本發明保護的范圍。
下述各實施例中,未注明具體條件的實驗方法,按照通常的常規條件或一起和試劑盒制造廠商所建議的條件。
下述各實施例中,需要的材料和設備如下。
病毒株與臨床樣品
6株PRRSV毒株,均來自商業化弱毒疫苗,其中3株C-PRRSV毒株,VR-2332、CH-1R和R98,分別來自德國勃林格殷格翰公司、維科生物技術開發公司和瑞普(保定)生物藥業有限公司;3株HP-PRRSV毒株,JXA1-R、HuN4-F112和TJM-F92,分別來自普萊柯生物工程股份有限公司、維科生物技術開發公司和青島易邦生物工程有限公司。
豬瘟病毒(Classical swine fever virus,CSFV,AV1412),來自瑞普(保定)生物藥業有限公司商業化弱毒疫苗;O型口蹄疫病毒(Foot-and-Mouth Disease virus,FMDV,TypeO),來自蘭州獸醫研究所商業化液相阻斷ELISA試劑盒;偽狂犬病毒(Pseudorabies virus,PRV)、豬細小病毒(Porcine parvovirus,PPV)和豬圓環病毒2型(Porcine circovirus-2,PCV-2),均為本實驗室保存。
60份臨床樣品,包括淋巴結、肺臟、脾臟和肝臟,均來自河北省不同養豬場。取10mg樣品在1mL無菌PBS中研磨處理,4℃,3000g離心10min收集上清用于病毒RNA/DNA提取。
主要試劑和設備
TwistAmpTM RT exo kit,購自英國TwistDx公司;病毒DNA/RNA提取試劑盒、DNA純化回收試劑盒均購自天根生化科技(北京)有限公司;One Step PrimeScript RT-PCR Kit、NdeI酶、PrimeScriptTMⅡ1st strand cDNA Synthesis Kit均購自寶生物工程(大連)有限公司;pGEM-T-EASY載體、Ribo MAXTM Large Scale RNA Production System-T7均購自美國Promega公司。
等溫擴增熒光檢測儀(OptigeneⅢ,型號Genie III),英國Optigene公司;實時熒光定量PCR儀(ABI 7500),美國ABI公司;EPS梯度PCR儀,為美國Eppendorf公司產品;核酸蛋白測定儀(Nanodrop ND-2000),為美國Thermo公司產品。
實施例1引物及exo探針的設計
參考GenBank中美洲型PRRSV ORF7序列(EF112445),選擇特異性保守區域,設計RPA引物和exo探針,目的片段大小為178bp。引物和exo探針的序列見SEQ ID No.1、SEQ ID No.2和SEQ ID No.3,如表1。
表1引物及exo探針序列
實施例2熒光實時RT-RPA檢測PRRSV
(一)病毒DNA/RNA提取
按照病毒DNA/RNA提取試劑盒說明,提取病毒株和臨床樣品上清液中核酸,并使用核酸蛋白測定儀(Nanodrop ND-2000)測定提取病毒核酸的濃度。所有提取的病毒RNA或DNA保存于-80℃,備用。
(二)實時RT-RPA反應體系及條件
使用TwistAmpTM RT exo kit配制50μL實時RT-RPA反應體系。擴增反應的50μL反應體系中加入濃度10μM的正向引物序列(RPA-Forward)2.1μL(終濃度420nM),濃度10μM的反向引物序列(RPA-Reverse)2.1μL(終濃度420nM),濃度10μM的exo探針(RPA-Probe)0.6μL(終濃度120nM),Buffer 29.5μL,蒸餾水12.2μL,混勻后轉入含有聚合酶、重組酶、單鏈結合蛋白和外切核酸酶III等凍干制劑的0.2mL反應管中,將1μLRNA模板、2.5μL濃度為280mM的MgAc(終濃度14mM)加入該反應管中。將反應管蓋緊后瞬時離心并渦旋后,放入Genie III中,42℃反應20min。在擴增過程實時收集檢測熒光信號,目的基因擴增后熒光信號會明顯增加。
實施例3特異性
以C-PRRSV,HP-PRRSV,CSFV,FMDV,PRV,PPV和PCV-2的病毒RNA或DNA,通過實施例2的方法進行實時熒光RT-RPA檢測,確定是否出現特異性擴增曲線。結果如圖1和圖2所示。
結果表明C-PRRSV毒株(VR-2332,R98and CH-1R)和HP-PRRSV毒株(JXA1-R,HuN4-F112and TJM-F92)均出現特異性擴增曲線(見圖2),而其他病毒則沒有出現擴增(見圖1),說明該方法具有良好的特異性,能過實現對不同C-PRRSV毒株和HP-PRRSV的特異性檢測,而不能擴增豬場常見的其他病原。這對于我國豬場中C-PRRSV和HP-PRRSV同時存在的現實具有重要意義。
需要說明的是,在本發明建立的針對美洲型PRRSV的熒光RT-RPA方法中,在反應即將結束時出現了熒光的急劇升高(見圖1和圖2)。其原因在于,在TwistAmpTM RT exo反應中,聚合酶和外切核酸酶III處于競爭關系,當反應即將結束,能量耗盡時,外切核酸酶III占據主導地位,進而導致exo探針的大量切割而出現熒光的突然升高。
實施例4敏感性
(I)PRRSV體外轉錄RNA的制備
以JXA1-R病毒RNA作為模板,以表2中N-forward和N-Reverse為引物進行RT-PCR,獲得433bpRT-PCR產物,涵蓋了PRRSV 3’端ORF7和3’非編碼區的部分區域。使用DNA純化回收試劑盒回收純化433bpRT-PCR產物,將之克隆到pGEM-T Easy載體中,并轉化入感受態細胞DH5α,獲得重組質粒pGEM-T-PRRSV-N。
表2N-forward和N-Reverse引物序列
使用Nde I將pGEM-T-PRRSV-N線性化,使用Wizard SV Gel and PCR純化試劑盒進行純化回收后,使用RiboMAX Large Scale RNA Production System-T7進行體外轉錄。室溫下采用100μL體系:T7Transcription 5X Buffer 20μL,rNTPs(25mM ATP,CTP,GTP,UTP)30μL,linear DNA template(5–10??g total)plus Nuclease-Free Water 40μL,Enzyme Mix(T7)10μL,輕輕充分混勻,37℃反應2-4h。使用RNase-Free DNase I處理RNA,20-25℃孵育10min,以除去殘留的DNA,純化RNA。
所有體外轉錄PRRSV RNA經瓊脂糖凝膠電泳確定大小均為433bp左右,并使用Nanodrop ND-2000測定濃度,通過公式計算拷貝數:拷貝數(copies/μL)=[RNA濃度(g/μL)/(RNA堿基數×340)]×6.02×1023,并10倍系列稀釋至1.0copies/μL。
(II)敏感性分析
將體外轉錄病毒RNA進行10倍倍比稀釋,使其濃度在106-100拷貝/μL之間,106-100拷貝/μL系列濃度的體外轉錄PRRSV RNA以1μL作為模板進行實時RT-RPA反應,確定該方法的最低檢測濃度。與OIE參考方法進行比較。
OIE參考方法,即在ABI7500上進行美洲型PRRSV的熒光RT-PCR檢測。熒光RT-PCR檢測方法所用引物及序列如表3所示。在反應體系配制中,使用One Step PrimeScript RT-PCR Kit代替原方法中使用的反轉錄酶、DNA聚合酶、dNTP混合液等試劑,其他試劑濃度不變。反應條件為:42℃5min;95℃10s;95℃5s,60℃34s,40個循環。
結果表明,熒光RT-RPA最低可以檢測到102拷貝病毒RNA(見圖3),同OIE推薦熒光RT-PCR方法一致(見圖4)。熒光RT-RPA對106-102拷貝病毒RNA的檢測時間是5-15min,而熒光RT-PCR的檢測Ct值是21-37,所需時間則為40-60min。
表3熒光RT-PCR所用引物及序列
實施例5對臨床樣品的檢測
采用OIE推薦熒光RT-PCR方法及本發明實施例2中的熒光RT-RPA方法進行測試。在60份臨床實際樣品中,熒光RT-RPA對PRRSV的陽性檢出率為86.6%(52/60),而熒光RT-PCR的陽性檢出率則為83.3%(50/60)(結果見表4)。對于陽性樣品的檢測時間,熒光RT-RPA為3-16min,而熒光RT-PCR則為1h左右。這說明,本發明建立的熒光RT-RPA的檢測效果要優于熒光RT-PCR,就檢測時間而言,熒光RT-RPA為3-16min,遠遠小于熒光RT-PCR所需要的30-60min。
表4熒光RT-RPA和熒光RT-PCR對臨床樣品的檢測結果比較
綜合上述各實施例,本發明建立了一種特異性快速檢測美洲型PRRSV的熒光RT-RPA方法。聚合酶重組酶擴增(Recombinase polymerase amplification,RPA)是一種基于等溫擴增的分子檢測技術。RPA已經被廣泛應用于疫病病原的檢測。相對于普通PCR和熒光PCR,RPA具有以下優勢:1、RPA試劑以凍干粉形式存在,在運輸和保存過程中不需要冷鏈,可以在25℃下存放12周,45℃下存放3周;2、RPA能夠在5-20min內獲得檢測結果,遠遠快于PCR方法(一般需要60min以上);3、RPA所用的引物和探針可以耐受5-9個堿基的錯配,而對檢測結果沒有影響,從而可以耐受檢測對象的一定程度上的突變,而熒光PCR所用的探針的突變能夠造成檢測的失敗;4、RPA對常見的PCR抑制劑具有一定的耐受性,并且可以不同的生物樣品(如血清、糞便、尿液、血漿、動物組織、鼻拭子等),從而降低了對樣品的制備需求;5、RPA具有多種結果呈現形式,可以通過瓊脂糖凝膠電泳、實時熒光檢測或試紙條形式進行結果判定;6、RPA屬于等溫擴增,無需復雜的升降溫控制。
目前,核酸等溫擴增技術由于其操作簡單、快速和成本低的特點,成為PCR檢測技術的代替者。相比較于其他等溫擴增技術,RPA無需在反應開始時升溫解鏈模板DNA,一直處于等溫過程中實現對靶基因的指數擴增。由于RPA的簡便性(簡單的操作)、多樣性(用于核酸檢測的不同商業化試劑盒)和快速(5-20min),RPA可能是最適于傳染病田間和現場檢測的方法。目前針對PRRSV的檢測,也建立了多個RT-LAMP方法。不同于RT-RPA,在RT-LAMP方法建立過程中需要設計特異性強、性能良好的4-6引物,這對于易于變異的PRRSV來說,是非常困難的。同時LAMP對引物堿基錯配的耐受性尚不明確。另外,上述建立的RT-LAMP方法反應時間均為40-50min,遠遠長于RT-RPA反應時間。
RPA屬于等溫擴增技術,除了可以應用于環境設備良好的實驗室外,還可以被廣泛應用于不發達地區實驗室,甚至是現場檢測。本研究中所使用檢測設備的小巧、輕便、便攜,結合熒光RT-RPA操作的簡便性、試劑無需冷鏈保存的特點,所建立的熒光RT-RPA方法具有田間應用的巨大優勢和潛力,可以應用于現場診斷和田間監測,特別是豬場所在的偏遠地區。
總之,本發明建立了一種基于exo探針的能夠有效檢測C-PRRSV和HP-PRRSV的熒光RT-RPA方法。綜合反應敏感性和檢測時間而言,該方法要優于OIE推薦的熒光RT-PCR方法。本發明建立針對PRRSV熒光RT-RPA方法的便攜性好(Genie III,規格:25cm×16.5cm×8.5cm,重量:1.75kg),能夠使之在疫病發生現場、口岸和檢疫一線使用,對于我國PRRSV的防控具有重要意義。
根據上述的實施例對本發明作了詳細描述。需說明的是,以上的實施例僅為了舉例說明發明而已。在不偏離本發明的精神和實質的前提下,本領域技術人員可以設計出本發明的多種替換方案和改進方案,其均應被理解為在本發明的保護范圍之內。
SEQUENCE LISTING
<110> 河北出入境檢驗檢疫局檢驗檢疫技術中心
<120> 一種美洲型豬繁殖與呼吸綜合征病毒的熒光RT-RPA特異性檢測
<130> /
<160> 3
<170> PatentIn version 3.3
<210> 1
<211> 30
<212> DNA
<213> 人工序列
<400> 1
CGGAGAAGCC CCATTTCCCT CTAGCGACTG 30
<210> 2
<211> 30
<212> DNA
<213> 人工序列
<400> 2
TGCGTCGGCA AACTAAACTC CACAGTGTAA 30
<210> 3
<211> 50
<212> DNA
<213> 人工序列
<400> 3
CAATTGTGTC TGTCGTCGAT CCAGACTGCC TTCATCAGGG CGCTGGAACC 50
- 還沒有人留言評論。精彩留言會獲得點贊!