一種新型具有高平面性的含萘結構功能二胺單體及其合成方法和應用與流程
本發明專利申請是分案申請。原案的申請號是cn201510095103.5,申請日是2015年3月4日,發明名稱是:具有高平面性的含萘結構功能二胺單體及其合成方法和應用。
本發明涉及材料科學領域,特別是一種具有高平面性的含萘結構功能二胺單體及其合成方法,該二胺單體可用于合成如聚酰胺、聚酰亞胺、聚酰胺酰亞胺和聚酯酰亞胺等高性能、功能化聚合物。
技術背景
有機電致發光器件(oled)彰顯了全固態、主動發光、高發光效率、高亮度、高對比度、超薄、功耗低、無視角限制、響應速度快、工作溫度范圍寬、加工工藝簡單、節能環保等諸多優點,被認為是理想、具發展前景的取代液晶顯示器的新一代信息顯示技術,是未來30年世界信息產業發展的重點。并且,oled可實現柔性顯示是其獨有特點之一,柔性oled也被譽為“夢幻顯示器”。oled產業化的關鍵問題在于如何“擴尺寸、降成本、增壽命、提色彩”,只有徹底解決了這幾個問題,oled才能真正開啟第三代顯示革命之門。其中,使用壽命的長短是制約oled廣泛應用的最大挑戰之一,影響oled使用壽命的主要原因是電極材料和發光材料對氧、水、雜質都非常敏感,很容易被污染從而導致器件性能的下降,從而降低發光效率,縮短使用壽命。為了保證產品的發光效率并延長其使用壽命,器件在封裝時一定要隔絕氧和水。因此必須選用阻隔性能十分優異的柔性襯底材料對器件進行封裝,才能滿足產品壽命的嚴格要求,這使得研發新的封裝技術和封裝材料成為柔性oled產業發展的一大熱點。
oled的柔性顯示就要求柔性封裝,此類封裝材料的特點就是在發生很大彎曲變形的同時可以保證材料的有效使用,目前常用的柔性顯示器件的襯底封裝材料有超薄玻璃,金屬箔片和聚合物薄膜。玻璃具有優良的耐化學穩定性,能很好的阻隔水和氧,但是其韌性差、很脆,只有厚度達到一定的薄度才能具有一定的韌性,但大面積的玻璃薄化技術很難實現。沒有缺陷的金屬箔片是不允許水分子和氧氣透過的,并且它可以承受很高的加工溫度,但是金屬箔片不透光,并且表面平整性不好,不能承受多重彎曲、易產生針孔,這大大影響了其在柔性oled方面的應用。與超薄玻璃和金屬箔片相比,柔性聚合物薄膜具有質量更輕、柔韌性更好、成本更低、容易加工成型等優點,并且部分聚合物薄膜還具有優異的機械性能、光學性能、熱穩定性、化學穩定性和阻隔性能等,這些優勢使得聚合物薄膜成為制備柔性oled的關鍵材料。
目前,可用的柔性聚合物封裝材料有聚偏二氯乙烯(pvdc),乙烯-乙烯醇共聚物(evoh),聚酰胺(pa),聚乙烯醇(pva),聚酰亞胺(pi)及聚對苯二甲酸乙二醇酯(pet)和聚萘二甲酸乙二醇酯(pen)代表的熱塑性聚酯等。然而,柔性聚合物封裝材料的溫度特性(200℃的使用溫度)和阻隔性(水蒸氣透過率低于10-6g/m2/day,氧透過率低于10-5cm3/m2/day)是實現柔性oled需要克服的關鍵問題之一,而目前尚未報道具有該性能的聚合物。開發新型高阻隔聚合物材料是解決這一問題的辦法之一。通過對分子結構進行有針對性的設計來開發新型聚合物材料,不僅能夠改善聚合物薄膜的阻隔性能,還能達到提高聚合物綜合性能的目的。本發明通過在聚合物中引入具有剛性平面結構的萘環,設計合成一系列具有平面性的二胺單體,以其為單體可以制備得到分子鏈間相互作用力強、分子鏈堆砌緊密、自由體積小的聚合物(聚酰胺、聚酰亞胺、聚酰胺酰亞胺和聚酯酰亞胺等),從而獲得阻隔性能優異、綜合性能良好的柔性聚合物封裝材料。
技術實現要素:
本發明的目的是提供一種以萘結構為中心的、具有高平面性的新型功能二胺單體,可用于合成聚酰胺、聚酰亞胺、聚酰胺酰亞胺和聚酯酰亞胺等高性能、功能化聚合物。
本發明的另一目的在于提供上述具有高平面性的含萘結構功能二胺單體的合成方法。
本發明的目的是這樣實現的:具有高平面性的含萘結構功能二胺單體,其結構通式為:
其中,ar1選自下列結構式中的任何一種:
ar2選自下列結構式基團中的任何一種:
ar3選自下列結構式基團中的任何一種:
ar4選自下列結構式基團中的任何一種:
ar5選自下列結構式基團中的任何一種:
本發明另一目的是提供上述具有平面結構的含萘功能二胺單體的合成方法,該方法的反應過程為:1.(a1)、利用二鹵代萘通過格式反應生成萘基格式試劑;(a2)、利用步驟(a1)所得萘基格式試劑與二鹵代物通過kumada偶聯反應生成具有萘結構且含有兩個鹵原子的單體,或利用步驟(a1)所得萘基格式試劑與帶有鹵原子的單硝基化合物通過取代反應生成二硝基單體;(a3)、利用步驟(a2)所得到的具有兩個鹵原子的含萘單體,通過suzuki反應,得到具有平面結構的二胺單體,獲得如權利要求1結構通式如ⅰ或ⅱ所示的新型二胺化合物,或者將步驟(a2)中得到的二硝基單體還原成二胺,獲得如權利要求1結構通式如ⅰ或ⅱ所示的新型二胺化合物,此外,還可以將二鹵代萘和帶硼酸的單胺通過一步suzuki反應直接獲得權利要求1結構通式如ⅰ或ⅱ所示的新型二胺化合物。2.(b1)、利用二氯亞砜或草酰氯等通過酰氯化反應將萘二酸轉化成萘二酰氯,(b2)、利用步驟(b1)所得的化合物上的酰氯基團與帶鹵原子的單胺化合物通過酰胺化反應,得到含酰胺結構且帶有兩個鹵原子化合物,或者利用步驟(b1)所得的化合物上的酰氯基團與帶有胺基的單硝基化合物通過酰胺化反應,得到含有酰胺結構的二鹵代物,(b3)、將步驟(b2)所得到的含酰胺結構的二鹵代物與芳基硼酸通過suzuki反應獲得如權利要求1結構通式如iii或ⅳ所示的新型二胺化合物,或者將步驟(b2)所得到的含有酰胺結構的二硝基單體還原成二胺,獲得如權利要求1結構通式如iii或ⅳ所示的新型二胺化合物。3.(c1)、利用二氯亞砜或草酰氯等通過酰氯化反應將萘二酸轉化成萘二酰氯,(c2)、利用步驟(c1)所得的化合物上的酰氯基團與含羥基的單硝基化合物通過酯化反應,得到含有酯鍵的二硝基單體,或者直接通過萘二酸與含羥基的單硝基化合物通過酯化反應得到含有酯鍵的二硝基單體,(c3)、將步驟(c2)所得到的含有酯鍵的二硝基單體還原成二胺,獲得如權利要求1結構通式如ⅴ或ⅵ所示的新型二胺化合物。4.(d1)、利用萘二酚與含鹵原子的單硝基化合物反應生成含醚鍵的二硝基單體,(d2)、將步驟(d1)所得到的含有醚鍵的二硝基單體還原成二胺,獲得如權利要求1結構通式如ⅶ或ⅷ所示的新型二胺化合物。5.(e1)利用含兩個酰氯基團或兩個羧酸基團的化合物直接與萘二胺通過酰胺化反應獲得如權利要求1結構通式如ⅸ、ⅹ或xi所示的新型二胺化合物。其中所涉及到的重要中間體的結構通式如下:
本發明的二胺單體,由于其最低能態的3d空間結構具有高平面性,以其為單體可以制備得到分子鏈堆砌緊密,分子鏈間的相互作用力強,自由體積小的聚合物,能夠賦予聚合物良好的阻隔性能。本發明二胺單體的合成方法工藝簡單,純化容易,因而適于工業生產。本發明所公開的二胺單體可用于合成聚酰胺、聚酰亞胺、聚酰胺酰亞胺和聚酯酰亞胺等高性能、功能化聚合物。
附圖說明
圖1:實施例1~5所得單體的紅外光譜圖,其中:a~e分別為實施例1~5所得二胺的紅外光譜圖,從紅外光譜圖可以看到,在3480-3380cm-1的范圍內出現了-nh2-的特征吸收峰,在3000cm-1處出現了ar-h的特征吸收頻率,1730cm-1處出現了酯羰基的特征吸收峰,1653cm-1處出現了酰胺羰基的特征吸收峰,1617cm-1,和1503cm-1處出現了特征的苯環骨架伸縮振動吸收峰,1278cm-1附近的吸收峰為ar-h的變形振動吸收峰,1198cm-1處出現了醚鍵的特征吸收峰,1172cm-1處出現了酯基的特征吸收峰,827cm-1處為對位二取代ar-h的特征吸收頻率,這些都說明所合成的產物都具有芳香二胺的特征結構。
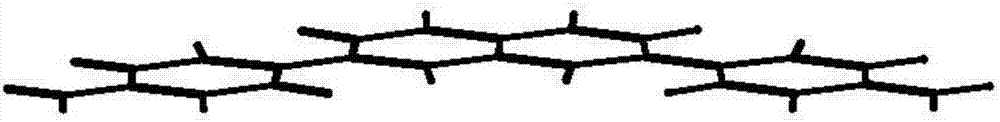
圖2:4,4'-(naphthalene-2,7-diyl)dianiline的最低能態的3d圖
圖3:bis(4-aminobenzyl)naphthalene-2,6-dicarboxylate的最低能態的3d圖
圖4:n2,n6-bis(4-((4-aminophenyl)amino)phenyl)naphthalene-2,6-dicarboxamide的最低能態的3d圖
圖5:4,4'-(((naphthalene-2,7-diylbis(oxy))bis(butane-4,1-diyl))bis(oxy))dianiline的最低能態的3d圖
圖6:n1,n4-bis(5-aminonaphthalen-1-yl)terephthalamide的最低能態的3d圖
具體實施方式
下面給出實例以對本發明作更詳細的說明,有必要指出的是以下實施例不能解釋為對發明保護范圍的限制,該領域的技術熟練人員根據上述發明內容對本發明作出的一些非本質的改進和調整,仍應屬于本發明的保護范圍。
實施例1
4,4'-(naphthalene-2,7-diyl)dianiline的合成:
將8.579g(0.03mol)2,7-二溴代萘、11.272g(0.065mol)對氨基苯硼酸鹽酸鹽加入到500ml三口瓶中,加入400ml四氫呋喃,再加入2mol/l的碳酸鉀溶液97.5ml和適量的aliquat336,磁力攪拌并通氬氣,油浴加熱至75℃后加入0.100g四三苯基膦鈀,回流反應24h。將反應液倒入水中,有大量沉淀析出。用漏斗抽濾,減壓蒸去溶劑。產物以二氯甲烷為流動相,硅膠為固定相作柱色譜提純,收集產物并旋干得到橙紅色固體,在60℃真空干燥24h,產率為80%。化合物的紅外光譜圖如圖1所示,采用chemoffice計算它的最低能態,所得結果如圖2所示。
實施例2
bis(4-aminobenzyl)naphthalene-2,6-dicarboxylate的合成:
(1)合成中間體naphthalene-2,6-dicarbonyldichloride
將10.810g(0.050mol)2,6-萘二羧酸加入到250ml三口燒瓶中,加入100ml除水二氯甲烷,在冰浴條件下緩慢滴加17.846g(0.150mol)二氯亞砜,在滴加3至4滴n,n-二甲基甲酰胺作為催化劑,磁力攪拌并通氬氣,升溫至75℃反應回流12h。減壓蒸去溶劑以及過量二氯亞砜,得到淡黃色固體,產率為85%。該中間體結構如下:
(2)合成中間體bis(4-nitrobenzyl)naphthalene-2,6-dicarboxylate:
將18.376g(0.12mol)4-硝基苯甲醇加入到500ml三口燒瓶中,加入200mln,n-二甲基乙酰胺,40ml三乙胺,在冰浴下緩慢加入反應(1)所得naphthalene-2,6-dicarbonyldichloride,磁力攪拌并通氬氣,升溫至100℃反應24h。將反應液倒入1000ml甲醇和水為1:1的溶液中,有大量沉淀析出。用漏斗抽濾,將抽濾所得固體在n,n-二甲基甲酰胺中重結晶,收集白色固體,在50℃真空干燥箱中干燥10h,得到19.851g白色固體,產率為81.6%。該中間體結構如下:
(3)bis(4-aminobenzyl)naphthalene-2,6-dicarboxylate的合成:
將19.453g(0.040mol)bis(4-nitrobenzyl)naphthalene-2,6-dicarboxylate加入到500ml三口瓶中,加入500ml無水乙醇,磁力攪拌并通氬氣,油浴加熱至70℃后,加入10%wt的鈀碳0.2g,并逐漸滴加35ml水合肼,回流反應24h后,將反應液用漏斗抽慮,將濾液放置在冰箱中24h結晶,抽濾后收集白色固體,在50℃真空干燥箱中干燥10h,得到產物bis(4-aminobenzyl)naphthalene-2,6-dicarboxylate15.911g,產率為91%。化合物的紅外光譜圖如圖1所示,采用chemoffice計算它的最低能態,所得結果如圖3所示。
實施例3
n2,n6-bis(4-((4-aminophenyl)amino)phenyl)naphthalene-2,6-dicarboxamide的合成:
(1)按實施例2合成中間體naphthalene-2,6-dicarbonyldichloride;
(2)合成中間體n2,n6-bis(4-aminophenyl)naphthalene-2,6-dicarboxamide:
將10.814g(0.1mol)對苯二胺溶于150mln-甲基吡咯烷酮和吡啶為4:1的溶液中,再緩慢加入5.061g(0.02mol)naphthalene-2,6-dicarbonyldichloride,在氬氣環境下加入12.420g(0.04mol)亞磷酸三苯酯,室溫攪拌2h,然后升溫至100℃反應12h,冷卻后將反應液倒入甲醇中,濾出沉淀,用甲醇充分洗滌,在n,n-二甲基甲酰胺和水中重結晶,在50℃真空干燥箱中干燥10h,得到米白色產物n2,n6-bis(4-aminophenyl)naphthalene-2,6--dicarboxamide6.739g,產率為85%。該中間體結構如下:
(3)合成中間體n2,n6-bis(4-((4-nitrophenyl)amino)phenyl)naphthalene-2,6-dicarboxamide:
將3.964g(0.01mol)n2,n6-bis(4-aminophenyl)naphthalene-2,6-dicarboxamide和6.060g(0.03mol)對溴硝基苯加入到500ml三口燒瓶中,加入150ml二甲基亞砜,磁力攪拌并通氬氣,升溫至150℃反應12h后將反應液倒入冷水中,濾出沉淀,用鹽酸和水洗滌,得到黃褐色產物n2,n6-bis(4-((4-nitrophenyl)amino)phenyl)naphthalene-2,6-dicarboxamide4.917g,產率為77%。該中間體結構如下:
(4)n2,n6-bis(4-((4-aminophenyl)amino)phenyl)naphthalene-2,6-dicarboxamide的合成:
二胺n2,n6-bis(4-((4-aminophenyl)amino)phenyl)naphthalene-2,6-dicarboxamide的合成:
實施例4
4,4'-(((naphthalene-2,7-diylbis(oxy))bis(butane-4,1-diyl))bis(oxy))dianiline的合成:
(1)合成中間體1-(4-bromobutoxy)-4-nitrobenzene:
將13.911g(0.1mol)對硝基苯酚,64.773g(0.3mol)1,4-二溴丁烷和41.463g(0.3mol)碳酸鉀加入到500ml三口瓶中,加入250mln,n-二甲基甲酰胺,磁力攪拌并通氬氣,室溫下反應24小時后將反應液倒在冰水中,用二氯甲烷對反應粗產物進行萃取。粗產物以正己烷為流動相,硅膠為固定相作柱色譜提純,收集產物并旋干溶劑得到淡黃色固體21.614g,產率為80%。該中間體結構如下:
(2)合成中間體2,7-bis(4-(4-nitrophenoxy)butoxy)naphthalene
將13.706g(0.05mol)1-(4-bromobutoxy)-4-nitrobenzene,3.203g(0.02mol)2,7-二羥基萘和8.292g(0.06mol)碳酸鉀加入到500ml三口燒瓶中,加入250mln,n-二甲基甲酰胺,磁力攪拌并通氬氣,室溫下反應24小時后將反應液倒在冰水中,用二氯甲烷對反應粗產物進行萃取。粗產物以二氯甲烷和正己烷比例1:2為流動相,硅膠為固定相作柱色譜提純,收集產物并旋干溶劑得到淡黃色固體2,7-bis(4-(4-nitrophenoxy)butoxy)naphthalene8.741g,產率為80%。該中間體結構如下:
(3)4,4'-(((naphthalene-2,7-diylbis(oxy))bis(butane-4,1-diyl))bis(oxy))dianiline的合成:
將5.466g(0.01mol)2,7-bis(4-(4-nitrophenoxy)butoxy)naphthalene加入到500ml三口瓶中,加入500ml無水乙醇,磁力攪拌并通氬氣,油浴加熱至70℃后,加入10%wt的鈀碳0.05g,并逐漸滴加10ml水合肼,回流反應24h后,將反應液用漏斗抽慮,將濾液放置在冰箱中24h結晶,抽濾后收集米白色固體,在50℃真空干燥箱中干燥10h,得到產物4,4'-(((naphthalene-2,7-diylbis(oxy))bis(butane-4,1-diyl))bis(oxy))dianiline4.912g,產率為90%。化合物的紅外光譜圖如圖1所示,采用chemoffice計算它的最低能態,所得結果如圖5所示。
實施例5
n1,n4-bis(5-aminonaphthalen-1-yl)terephthalamide的合成:
將15.820g(0.1mol)1,5-萘二胺溶于150mln-甲基吡咯烷酮和吡啶為4:1的溶液中,再緩慢加入4.06g(0.02mol)對苯二酰氯,在氬氣環境下加入12.420g(0.04mol)亞磷酸三苯酯,室溫攪拌2h,然后升溫至100℃反應12h,冷卻后將反應液倒入甲醇中,濾出沉淀,用甲醇充分洗滌,在n,n-二甲基乙酰胺和水中重結晶,在50℃真空干燥箱中干燥10h,得到褐色產物n1,n4-bis(5-aminonaphthalen-1-yl)terephthalamide6.438g,產率為72.6%。化合物的紅外光譜圖如圖1所示,采用chemoffice計算它的最低能態,所得結果如圖6所示。
- 還沒有人留言評論。精彩留言會獲得點贊!