反式法尼基硫代水楊酸的應用的制作方法
本發明屬于抗癡呆藥物領域,具體涉及一種反式法尼基硫代水楊酸(Trans Farnesyl Thiosalicylic Acid/Salirasib,FTS)在制備抗癡呆藥物中的應用。
背景技術:
癡呆已被稱為世界上當前的“流行病”之一,在發達國家被估計列為第四位最常見的死亡原因。所謂的老年性癡呆癥,最常見的為阿爾茨海默病(Alzheimer’s disease,AD)。阿爾茨海默病是一種發生在老年期及老年前期以進行性認知障礙為主要臨床表現的神經退行性疾病。隨著世界人口進入老齡化,阿爾茨海默病的發病率快速上升,幾乎每7秒鐘就有一人患病,預測到2050年將增加到11540萬人。但是,迄今仍然缺乏療效顯著和可靠、副作用少、維持療效的抗癡呆藥物。
阿爾茨海默病腦的主要特征性病理變化為大腦皮層萎縮,β-淀粉樣蛋白(Aβ)沉積,神經原纖維纏結,膽堿能神經系統損害,以及老年斑的形成。中樞膽堿能神經是構成學習記憶的重要生物學基礎。海馬的乙酰膽堿受體α7亞型(α7nACh)介導鈣離子內流參與記憶的形成。AD腦中膽堿能神經元選擇性退變。臨床病理分析發現α7nACh受體在AD患者腦中的密度明顯下降,且α7nACh受體水平降低與AD患者認知功能評分密切相關。Aβ能直接抑制α7nACh受體功能,損害突觸傳遞和可塑性,提出α7nACh受體損害是AD早期認知障礙的重要病理機制。AD腦的神經細胞死亡,導致谷氨酸NMDA受體減少和功能降低也被認為是認知功能減退的關鍵病理機制。
Ras傳導通路參與支氣管哮喘、腫瘤等疾病的發生,因此Ras信號通路被作為抗腫瘤和治療支氣管哮喘的靶標。反式法尼基硫代水楊酸(Trans Farnesyl Thiosalicylic Acid/Salirasib,FTS)是一種新型的Ras抑制劑。FTS能模擬Ras的幾基末端法尼半胱氨酸,將活化Ras從它的膜鑲嵌結構域上移去從而發揮Ras抑制功能。FTS對結合活化GTP的Ras具有明顯的選擇性抑制作用。在動物實驗中,FTS無明顯毒性或不良副作用。
技術實現要素:
解決的技術問題:本發明提供一種反式法尼基硫代水楊酸(FTS)在制備抗癡呆藥物中的應用。
技術方案:反式法尼基硫代水楊酸在制備抗癡呆藥物中的應用。。
所述反式法尼基硫代水楊酸(FTS)的結構為
FTS別名為2-[[(2E,6E)-3,7,11-三甲基-2,6,10-十二烷三烯-1-基]硫代]苯甲酸;
分子式:C22H30O2S,分子量:358.54。
有益效果:反式法尼基硫代水楊酸(FTS)對老年性癡呆,阿爾茨海默病認知障礙具有明顯的改善作用。具體的說,(1)在阿爾茨海默病模型小鼠,FTS經口腔或腹腔注射處理都能改善模型小鼠的認知功能障礙,(2)FTS能減少Aβ的神經毒性,減少神經細胞死亡,(3)FTS能恢復阿爾茨海默病模型小鼠海馬腦區的突觸傳遞效應和長時程增強誘導,(4)FTS經口腔、腹腔注射或細胞孵育能劑量依賴地增強小鼠海馬腦區的突觸傳遞效應和長時程增強誘導。(5)FTS增強神經細胞谷氨酸NMDA受體的活性;(6)FTS增強神經細胞α7nACh的活性。
附圖說明
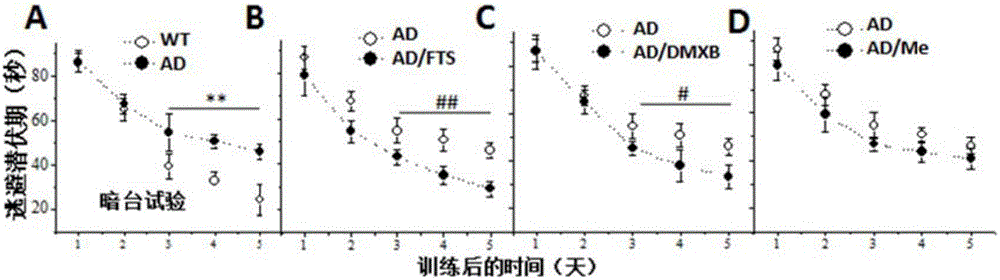
圖1為FTS連續20天進行APP/PS1小鼠腹腔注射后,,(A-D))Morris水迷宮隱蔽平臺的逃避潛伏期;
圖2為Morris水迷宮空間探索時的各象限游泳時間百分比;
圖3為“Y“迷宮的進臂交替率(%);
圖4-A為海馬CA1區的突觸傳遞功能;
圖4-B為海馬CA1區的長時程增強(LTP)誘導。*P<0.05和**P<0.01vs.野生型小鼠;#P<0.05和##P<0.01vs.APP/PS1小鼠。
圖5為FTS連續14天進行Aβ25-35小鼠腹腔注射后,(A-D)Morris水迷宮隱蔽平臺的逃避潛伏期;
圖6為Morris水迷宮空間探索時的各象限游泳時間百分比;
圖7為“Y“迷宮的進臂交替率(%);
圖8為海馬CA1區神經細胞的計數;
圖9為海馬CA1區的突觸傳遞功能和長時程增強(LTP)誘導。*P<0.05和**P<0.01vs.對照組小鼠;#P<0.05和##P<0.01vs.Aβ25-35小鼠。
圖10為FTS增強海馬腦區的突觸傳遞效應和長時程增強誘導的試驗結果圖。為2-4小時用FTS處理海馬腦片后,(A-B)海馬CA1腦區的突觸傳遞效應和海馬CA1腦區的LTP誘導。*P<0.05和**P<0.01vs.對照組。
圖11為FTS連續5天進行小鼠腹腔注射后,(A-B)海馬CA1腦區的突觸傳遞效應和海馬CA1腦區的LTP誘導。
圖12為FTS增強海馬神經細胞的谷氨酸NMDA受體活性的試驗結果圖。為2-4小時用FTS處理海馬腦片后,NMDA受體的鈣離子內向電流(INMDA)的密度曲線。*P<0.05和**P<0.01vs.對照組。
圖13為FTS連續5天進行小鼠腹腔注射后,NMDA受體的鈣離子內向電流(INMDA)的密度曲線。*P<0.05和**P<0.01vs.對照組。
圖14為FTS增強α7nACh受體活性的試驗結果圖,為2-4小時用FTS處理海馬腦片后,乙酰膽堿(ACh)誘導的α7nACh受體內向電流(IACh)的密度曲線。*P<0.05和**P<0.01vs.對照組。
圖15為FTS連續5天進行小鼠腹腔注射后,乙酰膽堿(ACh)誘導的α7nACh受體內向電流(IACh)的密度曲線。*P<0.05和**P<0.01vs.對照組。
具體實施方式
本發明結合附圖和實施例作進一步的說明,(1)在阿爾茨海默病模型小鼠,FTS經口腔或腹腔注射等途徑處理都能改善小鼠的認知功能障礙,(2)FTS能減少Aβ的神經毒性和神經細胞死亡,(3)FTS能恢復阿爾茨海默病模型小鼠海馬腦區的突觸傳遞效應和長時程增強誘導,(4)FTS經口腔或腹腔注射,細胞孵育等途徑處理能劑量依賴地增強小鼠海馬腦區的突觸傳遞效應和長時程增強誘導。(5)FTS增強神經細胞谷氨酸NMDA受體的活性;(6)FTS增強神經細胞α7nACh受體的活性。
實施例1:FTS改善APP/PS1轉基因小鼠(阿爾茨海默病模型)的認知功能和神經系統功能
實驗主要材料:
動物飼養在南京醫科大學實驗動物中心,并且維持在溫度23±2℃,濕度55±5%,12:12h光/暗循環的環境下。它們可以自由的取食物和水。
阿爾茨海默病模型小鼠
APP/PS1小鼠:10月齡雄性和雌性APPswe/PS1dE9雙轉基因型小鼠(以下簡稱,APP/PS1小鼠)從Jackson實驗室(Bar Harbor,ME,USA)購得,運用Jackson實驗室推薦的PCR方法進行基因型鑒定。
藥物和試劑
反式法尼基硫代水楊酸(Trans-farnesylthiosalicylic acid,FTS)從美國Calbiochem公司購買(Cat#344555)。FTS在5%Tween 80產生乳液或溶解于dimethyl sulfoxide(DMSO)。用生理鹽水或人工腦脊液稀釋到使用濃度(DMSO的最終濃度低于0.1%),進行腹腔注射(5mg/kg)。
α7nACh受體激動劑3-(2,4-dimethoxybenzylidene)-anabaseine(DMXB,日本大昭制藥公司提供,代號GTS-21,Taisho Pharmaceuticals,Tokushima,Japan)溶解在生理鹽水中進行腹腔注射(2mg/kg)。
NMDA受體拮抗劑鹽酸美金剛(易倍申,批號366825,規格10mg/片,丹麥靈北藥廠產品)用0.1%的DMSO配制至所需濃度(Memantine,5mg/kg)進行灌胃給藥。
實驗操作
空間認知行為的評價:
Morris水迷宮試驗:采用Morris水迷宮檢測小鼠空間學習的長期記憶功能(Aβ25-35給藥后第6-11天)。《隱蔽平臺試驗(hidden platform trial)》直徑120cm、高45cm的圓形白色水池,水深30cm,水溫保持(23±1)℃,水中加入食品添加劑深藍色粉末。將水池等分成四個象限,在池壁上標記四個象限的入水點,在第四象限正中處放一個直徑為7cm的圓形平臺,平臺頂低于水面1cm。迷宮上方安置帶有視頻拍攝系統的攝像機,以便同步記錄小鼠的游泳軌跡。訓練期間迷宮外參照物保持不變,室內保持安靜。第一次實驗前一天(Aβ25-35給藥后第5天)撤去隱蔽平臺,將小鼠放入水池中自由游泳60秒,以檢測各組小鼠間的游泳能力有無差異。前五天進行定向航行實驗,每天訓練4次,每次訓練的設定時間為90秒,訓練時將小鼠面向池壁依次從各個象限的入水點入水,觀察并記錄小鼠的登臺潛伏期(即從小鼠入水到找到水下隱蔽平臺并立于其上所需時間)。登臺潛伏期(逃避潛伏期,escape latency)反應了小鼠的學習記憶能力:登臺潛伏期越短,說明小鼠的學習記憶能力越好。如果小鼠在90秒內未找到平臺,潛伏期記為90秒。《空間探索試驗(probe trial)》第6天(Aβ25-35給藥后第11天)撤去隱蔽平臺進行空間探索實驗,小鼠從平臺所在象限的對面象限入水,記錄小鼠在60秒內的游泳軌跡,分別對小鼠在各個象限(target quadrant,opposite quadrant,adjacent right and left quadrant)的停留時間進行統計分析。對小鼠原站臺所在象限停留時間%進行分析。
“Y”迷宮試驗:短期記憶可以用Y-maze實驗來評估。Y-maze即黑色Y形三等分輻射式迷路箱,由3個支臂和一個連接區組成,三臂互相間夾角120°,每臂長38.5厘米,上寬8厘米,下寬3.5厘米,高12厘米,三個臂可任選一臂為起始臂。每只小鼠從固定一臂的末端釋放,讓小鼠自由活動8分鐘,記錄每次進臂的次序。三次連續進入不同的三個臂被定為交替進臂(如:ABC,ACB,BAC,BCA,CAB,CBA)。交替進臂率的計算為:1-(錯誤次數/總次數-2)×100%。另外,總的進臂次數也可以確定。
海馬突觸傳遞功能檢查
腦片制備:小鼠在乙醚麻醉下快速斷頭取腦,置于0–4℃冰凍人工腦脊液(artificial cerebrospinal fluid,ACSF)中2min左右備用。ACSF成分為(mM):124.0NaCl,4.5KCl,2.0CaCl2,1.0MgCl2,26.0NaHCO3,1.2NaH2PO4,10.0D-glucose。使用前通混合氣(95%O2,5%CO2)使pH值穩定在7.4。鼠腦經稍加修飾后移至振動切片機浴槽內,在0–4℃ACSF中切取包含海馬的冠狀腦片2–4片(厚度400μm)。將切好的腦片迅速轉移至持續通飽和氧混合氣的ACSF中,在室溫(22–25℃)下孵育至少60min后移至恒溫記錄浴槽,浴槽為浸潤式灌流系統,灌流速度1mL/min,溫度30±1℃,并持續通氧。記錄電極使用標準硼硅酸鹽玻璃管經P-97拉制儀拉制,沖灌2M NaCl溶液后電極阻抗為4–5MΩ。刺激電極為自制雙極鎢絲電極,直徑50μm,極間距為100–150μm,尖端裸露40–60μm。刺激電極為雙極鎢絲電極置于海馬腦片CA2或CA1區的謝弗側支處,進行順向刺激,距離刺激電極約2–3mm,其尖端位于腦片表面下50–200μm處,記錄興奮性的突觸后電位EPSP。記錄信號經放大器放大,Bridge模式,濾波5kHz,經A/D卡進行數模轉換后用Clampex軟件(Axon Inc.,USA)顯示并保存。使用SEN-3301刺激器,刺激波寬0.1ms,刺激強度約為0.1–1.0mA,刺激間隔為15秒,每4個刺激進行一次疊加平均獲得標準EPSP。每次實驗時,刺激強度從閾值開始直至誘發最大EPSP,測定輸入–輸出(input-output relationship,I/O)曲線。每一個刺激強度取5個反應,以刺激強度為橫坐標,以平均的EPSP斜率為縱坐標得到I/O曲線。根據I/O曲線,選擇最大反應的刺激強度一半作為測試刺激強度進行長時程增強實驗。長時程增強(long-term potentiation,LTP)的誘導是先用實驗刺激強度刺激腦片作為條件測試,采集20分鐘作為平均的基數值(100%),然后進行高頻條件刺激(HFS,100Hz,100次刺激共1秒),再施以高頻條件刺激前的同樣實驗測試,至少穩定記錄1小時。高頻條件刺激后如果EPSP斜率增加20%或以上,判斷為LTP的發生。
統計學分析
定量資料表示為均值±標準誤。Morris水迷宮原站臺所在象限時間%和“Y”迷宮采用雙因數和單因素方差分析。Scheffe`s檢驗測定兩組間的差異顯著性。將差異P<0.05定義為差異顯著。
試驗結果:
(1)Morris水迷宮—隱蔽平臺試驗:與野生型小鼠相比,10月齡APP/PS1小鼠的逃避潛伏期顯著延長(**P<0.01vs.野生型小鼠,n=8,圖1-A)。FTS(5mg/kg)處理(20天)能減少APP/PS1小鼠的逃避潛伏期(##P<0.01vs.APP/PS1小鼠,n=8,圖1-B)。α7nACh受體激動劑DMXB(2mg/kg)20天處理能部分改善APP/PS1小鼠的逃避潛伏期(#P<0.05vs.APP/PS1小鼠,n=8,圖1-C),而美金剛(5mg/kg)不能降低APP/PS1小鼠的逃避潛伏期(P>0.05,n=8,圖1-D)。
(2)Morris水迷宮—空間探索試驗:與野生型小鼠相比,APP/PS1小鼠在站臺象限的游泳時間顯著減少(**P<0.01vs.野生型小鼠,n=8,圖2)。FTS處理能增加APP/PS1小鼠在站臺象限的游泳時間(##P<0.01vs.APP/PS1小鼠,n=8)。DMXB能改善APP/PS1小鼠在站臺象限的游泳時間(#P<0.05vs.APP/PS1小鼠,n=8)。美金剛不能增加APP/PS1小鼠在站臺象限的游泳時間(P>0.05,n=8)。
(3)“Y“迷宮的檢測結果顯示,APP/PS1小鼠與野生型小鼠比較進臂交替率有顯著性減少(**P<0.01vs.野生型小鼠,n=8,圖3)。FTS處理能明顯增加APP/PS1小鼠的進臂交替率(##P<0.01vs.APP/PS1小鼠,n=8)。DMXB能增加APP/PS1小鼠的進臂交替率(#P<0.05vs.APP/PS1小鼠,n=8)。美金剛處理并不能明顯改善APP/PS1小鼠的進臂交替率(P>0.05,n=8)。
(4)電生理檢測結果顯示,APP/PS1小鼠的海馬CA1區的突觸傳遞斜率明顯低于野生型小鼠(**P<0.01vs.野生型小鼠,n=8,圖4-A)。FTS處理能提高APP/PS1小鼠的突觸傳遞斜率(#P<0.05&##P<0.01vs.APP/PS1小鼠,n=8)。DMXB使用能恢復APP/PS1小鼠的突觸傳遞斜率(#P<0.05vs.APP/PS1小鼠,n=8)。美金剛處理并不能明顯改善APP/PS1小鼠的突觸傳遞斜率(P>0.05,n=8)。
(5)電生理檢測結果顯示,APP/PS1小鼠的海馬CA1區的LTP不能誘導(n=8,圖4-B)。FTS處理能恢復APP/PS1小鼠的LTP誘導(n=8)。DMXB能30-40%恢復APP/PS1小鼠的LTP誘導(n=8)。而美金剛處理并不能恢復APP/PS1小鼠的LTP誘導(n=8)。
(圖中略寫符號,WT:野生型小鼠,AD:APP/PS1小鼠,Me:美金剛;PQ:站臺象限,OQ:站臺對面象限,R-AQ:站臺右側象限,L-AQ:站臺左側象限)。
結論:FTS有顯著的抗阿爾茨海默病癡呆作用。
實施例2:FTS改善Aβ25-35小鼠(阿爾茨海默病模型)的認知損害和保護神經細胞
實驗主要材料:
動物飼養在南京醫科大學實驗動物中心,并且維持在溫度23±2℃,濕度55±5%,12:12h光/暗循環的環境下。它們可以自由的取食物和水。
藥物和試劑
同實施例1。
阿爾茨海默病模型小鼠
將Aβ25-35溶于無菌雙蒸水中配成1mg/mL的溶液,置于37℃水浴箱中孵育4天,使其成為聚集態。注射前可以用生理鹽水稀釋到終濃度。Maurice等人發現,以上方法處理后可以看到兩種類型的Aβ聚集態,分別是雙折射的纖維型和球型結構[1]。小鼠經2%水合氯醛腹腔麻醉(400mg/kg)后固定于小鼠腦立體定位儀上。參照Paxinos和Watson小鼠立體定位圖譜,以前囟為參考點,在前囟后0.3mm,右側1.0mm,深度2.5mm用微量進樣器將3μl聚集態Aβ25-35(6nmol)或滅菌生理鹽水(對照組)分別于15min緩慢注射到小鼠雙側的側腦室,注射完畢后靜待5min后緩慢地拔出微量注射器,縫合皮膚。注射位置的準確性預先通過注射墨汁來確定。動物于Aβ25-35注射后第4-10天進行Morris水迷宮測試,第11天進行“Y”迷宮檢測,測得空間學習記憶能力,第12-16天進行海馬組織的病理學檢查和電生理學LTP檢測。
實驗操作
空間認知行為的評價:同實施例1。
組織學的檢測:Aβ25-35給藥后第14天,小鼠用2%水合氯醛(400mg/kg)腹腔麻醉,0.01M PBS和4%多聚甲醛灌流固定,經常規后固定、梯度酒精脫水、透明、石蠟包埋后,做5μm海馬連續冠狀石蠟切片。石蠟切片在37℃烘箱中過夜后,室溫存放。《甲苯胺藍染色》5μm石蠟切片在37℃烘箱中放1h后,脫蠟水化,ddH2O洗10min,經0.25%甲苯胺藍染色后用95%酒精分色、梯度酒精脫水、二甲苯透明、中性樹膠封片。以海馬CA1區和CA3區錐體神經細胞染色清晰為標準,光學顯微鏡下觀察腦組織病理變化(圖8的左圖)。存活的錐體細胞表現為圓形細胞體中帶有一個清晰深染的細胞核。將已固定的海馬組織用0.01M PBS沖洗,置于15%蔗糖緩沖溶液中,4℃冰箱過夜,待組織沉底后置于30%蔗糖緩沖液脫水,組織沉底后進行冰凍切片,冠狀切片厚40μm,每5張取1張得海馬連續切片,進行甲苯胺藍和TUNEL染色。利用Microbrightfield Stereo Investigator軟件計算整個海馬CA1或CA3區三維層面上的正常錐體細胞數(圖-2G的右圖)。
海馬突觸傳遞功能檢查:同實施例1。
統計學分析方法:同實施例1。
試驗結果:
(1)Morris水迷宮—隱蔽平臺試驗,與對照組相比,Aβ25-35小鼠的逃避潛伏期顯著延長(**P<0.01vs.對照組小鼠,n=8,圖5-A)。FTS(5mg/kg)處理(12天)能減少Aβ25-35小鼠的逃避潛伏期(##P<0.01vs.Aβ25-35小鼠,n=8,圖5-B)。DMXB(2mg/kg)能改善Aβ25-35小鼠的逃避潛伏期(#P<0.05vs.Aβ25-35小鼠,n=8,圖5-C)。但是,美金剛處理幾乎不能降低Aβ25-35小鼠的逃避潛伏期(#P<0.05vs.Aβ25-35小鼠,n=8,圖5-D)。
(2)Morris水迷宮—空間探索試驗:與野生型小鼠相比,Aβ25-35小鼠在站臺象限的游泳時間顯著減少(**P<0.01vs.對照組小鼠,n=8,圖6)。FTS處理能增加Aβ25-35小鼠在站臺象限的游泳時間(##P<0.01vs.Aβ25-35小鼠,n=8)。DMXB能部分改善Aβ25-35小鼠在站臺象限的游泳時間(#P<0.05vs.Aβ25-35小鼠,n=8),但是美金剛處理并不能改善Aβ25-35小鼠在站臺象限的游泳時間(P>0.05,n=8)。
(3)“Y“迷宮的檢測結果顯示,Aβ25-35小鼠與對照組比較進臂交替率有顯著性減少(**P<0.01vs.對照組小鼠,n=8,圖7)。FTS處理處理能明顯增加Aβ25-35小鼠的進臂交替率(##P<0.01vs.Aβ25-35小鼠,n=8)。DMXB能部分改善Aβ25-35小鼠的進臂交替率(#P<0.05vs.Aβ25-35小鼠,n=8)。美金剛不能改善Aβ25-35小鼠的進臂交替率(P>0.05,n=8)。
(4)海馬細胞計算結果顯示,與對照組相比Aβ25-35小鼠海馬CA1區錐體細胞數量明顯減少(*P<0.05vs.對照組小鼠,n=8,圖8)。FTS處理能明顯減少Aβ25-35小鼠海馬CA1區錐體細胞的丟失(#P<0.05vs.Aβ25-35小鼠,n=8)。DMXB或美金剛并不能減少Aβ25-35小鼠的錐體細胞的丟失(P>0.05,n=8)。
(5)電生理檢測結果顯示,Aβ25-35小鼠的海馬CA1區不能誘導LTP(n=8,圖9)。FTS處理能恢復Aβ25-35小鼠的LTP誘導(n=8)。DMXB能部分恢復Aβ25-35小鼠的LTP誘導(n=8)。但是,美金剛不能改善Aβ25-35小鼠的LTP誘導(n=8)。
(圖中略寫符號,control:對照組小鼠,Aβ:Aβ25-35小鼠,Me:美金剛;PQ:站臺象限,OQ:站臺對面象限,R-AQ:站臺右側象限,L-AQ:站臺左側象限)。
結論:FTS具有神經保護作用和抗阿爾茨海默病癡呆的作用。
實施例3:FTS增強小鼠海馬腦區的突觸傳遞效應和長時程增強誘導。
實驗主要材料:
3月齡的ICR小鼠購自南京醫科大學實驗動物中心。動物飼養在南京醫科大學實驗動物中心,并且維持在溫度23±2℃,濕度55±5%,12:12h光/暗循環的環境下。它們可以自由的取食食物和水。
藥物和試劑
同實施例1。FTS在5%Tween 80產生乳液或溶解于dimethyl sulfoxide(DMSO)。用生理鹽水或人工腦脊液(mM:124.0NaCl,4.5KCl,2.0CaCl2,1.0MgCl2,26.0NaHCO3,1.2NaH2PO4,10.0D-glucose)稀釋到使用濃度(DMSO的最終濃度低于0.1%),進行腹腔注射(5mg/kg)或腦片孵育(5-15μM)。
海馬突觸傳遞功能檢查:同實施例1。
統計學分析方法:同實施例1。
試驗結果:
(1)用FTS(5-15μM)進行2-4小時的海馬腦片孵育能劑量依賴地增強海馬CA1腦區的EPSP斜率(*P<0.05和**P<0.01vs.對照組小鼠,n=10;圖10-A)。
(2)用FTS(10μM)進行2-4小時的海馬腦片孵育,海馬CA1腦區的高頻條件刺激(100Hz,100次刺激)誘導LTP的幅值明顯增加(圖10-B)。
(3)為FTS(5mg/kg)連續5天進行小鼠腹腔注射后,海馬CA1腦區的EPSP斜率明顯增大(**P<0.01vs.對照組小鼠,n=10;圖11-A)。
(4)為FTS(5mg/kg)連續5天進行小鼠腹腔注射后,在海馬CA1腦區給予弱的高頻條件刺激(10次共0.1秒)能誘導LTP,但是在對照組小鼠不能誘導LTP(圖11-B),提示LTP誘導閾值顯著降低。
結論:FTS能提高神經回來興奮性和降低LTP誘導閾值。
實施例4:FTS能增強神經細胞的NMDA受體活性
實驗主要材料:
30-35天齡的ICR小鼠購自南京醫科大學實驗動物中心。動物飼養在南京醫科大學實驗動物中心,并且維持在溫度23±2℃,濕度55±5%,12:12h光/暗循環的環境下。它們可以自由的取食食物和水。
藥物和試劑
同實施例1。
實驗操作
電生理的檢測和分析:(1)海馬腦片制備:乙醚麻醉后快速斷頭取腦,置于0-4℃冰凍人工腦脊液中1分鐘備用。人工腦脊液使用前通混合氣(95%O2,5%CO2)使pH值穩定在7.4。鼠腦稍加修飾后移至振動切片機浴槽內,在0-4℃人工腦脊液中切取包含海馬的冠狀腦片3-6片(厚度350μm)。將切好的腦片迅速轉移至持續通混合氣的氧飽和人工腦脊液中,在28℃左右孵育至少60分鐘后移至記錄浴槽。浴槽為浸潤式灌流系統,灌流速度2mL/min,灌流液為持續通95%O2/5%CO2混合氣體的ACSF。微電極的拉制:選用長10cm,外徑為1.5mm,內徑為0.86mm標準硼硅酸鹽玻璃毛細管,在水平拉制儀上用四步拉制法拉制成記錄用微電極。充灌電極內液后電極尖端入水阻抗為4-6MΩ。電極無需拋光即可直接進行實驗。循環灌流系統:實驗中人工腦脊液用作灌流液進行循環灌流。溶液置于一定容積的刻度管中,并持續給95%O2/5%CO2混合氣,通過恒流泵的動力作用將氧飽和ACSF泵入記錄槽。溶液灌流速度由調節閥進行控制,通常為2-3mL/min,需要特殊沖洗的實驗,可將流速調至5-8mL/min,以使藥物快速而有效的作用于腦片細胞或者將殘留的藥物迅速沖洗干凈。灌流液溫度通過恒溫水浴鍋控制在28-30℃,使得記錄槽溫度維持在室溫附近。保持實驗室封閉透光,室內常溫(22-25℃),并具備較好的隔離噪音等條件。灌流系統所用的灌流管定期(兩周)更換,以免被污塘堵塞。
(2)全細胞膜片鉗記錄:實驗在室溫(22-25℃)下進行。將孵育好的腦片,轉移到記錄糟內,并用鉑金絲網固定,置于正置顯微鏡載物臺(配有40×的水鏡)上。在40×水鏡下,通過CCD(EvolutuonQE)采集圖象并可在顯示器上進行實時觀察。實驗過程中,選取腦片上CA1或CA3區胞體飽滿均勻,邊界清晰的神經元為記錄對象。在電壓鉗模式下用MP-225微型操縱儀引導充有電極內液的玻璃微電極靠近細胞,記錄電極入水前要先給予一正壓(將1mL注射器向前輕推1/10的體積),以防止電極尖端被污染。待電極靠近細胞,細胞出現小凹陷,并能觀察到電極阻抗上升3-5MΩ,釋放正壓并用給予適當負壓進行封接,同時逐步將鉗制電壓調節到–70mV,形成高阻封接(>1GΩ)。待形成穩定的封接后,給予強烈而短促的負壓打破電極尖端下的小片細胞膜,從而形成穩定的全細胞記錄模式。全細胞膜片鉗所用放大器為EPC-10,數據采集使用2.9kHz低通濾波,并在10kHz采樣。在電流記錄時,通過實時監控窗口,監測串聯電阻(Rs)的變化,防止破膜的回封引起電流動力學參數如幅度和衰減時間(decay time)的變化。其中Rs或者電容值的變化不應超過原值的20%,同時保持Rs<30M,Ra>200M。所采集數據中統計時舍去未補償的串聯電阻導致的電壓鉗誤差超過5mV的神經元數據。采樣后數據用PulseFit(HEKA公司)進行數據分析。記錄NMDA受體電流(INMDA)時,鉗制為–60mV,NMDA溶解到灌流液中,通過快速噴藥系統局部對目標神經元胞體進行加藥。同時浴槽循環灌流液中加入1μM strychnine,10μM bicuculline,10μM NBQX和0.1μM TTX。電生理結果用pClamp軟件(Axon公司)或PulseFit軟件(HEKA公司)進行數據處理。膜片鉗記錄數據分析:相關量效曲線用Hill方程進行擬合,n為Hill系數,EC50為半數有效劑量。
實驗結果
(1)海馬腦片進行FTS(10μM)4小時孵育,能增加NMDA誘導的NMDA受體內向電流(INMDA)的密度(*P<0.05和**P<0.01vs.對照組小鼠,n=10;圖12)。
(2)給與小鼠連續5天的FTS(5mg/kg)腹腔注射,能增加INMDA的密度(**P<0.01vs.對照組小鼠,n=10;圖13)。
結論:FTS能增強NMDA受體的活性。
實施例5:FTS能增強神經細胞α7nACh受體的活性
實驗主要材料:
同實施例1。
藥物和試劑
同實施例4。
實驗操作
電生理的檢測和分析:(1)同實施例4。記錄α7nACh受體電流(IACh)時,鉗制為–60mV,乙酰膽堿(ACh)溶解到灌流液中,通過快速噴藥系統局部對目標神經元胞體進行加藥。同時浴槽循環灌流液中加入1μM strychnine,10μM bicuculline,10μM NBQX和0.1μM TTX。電生理結果用pClamp軟件(Axon公司)或PulseFit軟件(HEKA公司)進行數據處理。膜片鉗記錄數據分析:相關量效曲線用Hill方程進行擬合,n為Hill系數,EC50為半數有效劑量。
實驗結果
(1)海馬腦片進行FTS(10μM)4小時孵育,能增加乙酰膽堿(ACh)誘導的α7nACh受體內向電流(IACh)的密度(*P<0.05vs.對照組小鼠,n=10;圖14)。
(2)給與小鼠連續5天的FTS(5mg/kg)腹腔注射,能增加IACh的密度(**P<0.01vs.對照組小鼠,n=10;圖15)。
(3)結論:FTS能增強α7nACh受體的活性。
- 還沒有人留言評論。精彩留言會獲得點贊!