HPV顆粒及其用途的制作方法
本申請是申請號為200980159856.0的中國專利申請的分案申請,原申請是2009年7月24日提交的pct國際申請pct/us2009/004299于2011年12月13日進入中國國家階段的申請。
相關申請
根據35u.s.c.§119(e),本申請要求2009年4月13日提交的美國臨時專利申請ussn61/168,914的優先權,其通過引用全文并入本文。
本發明涉及人乳頭瘤病毒樣顆粒(viruslikeparticle,vlp)及其作為治療劑的用途。
背景技術:
在世界范圍內,宮頸癌是女性主要癌癥死亡原因之一,每年奪去超過233,000名女性的生命。20世紀以前,在女性中的發生率和死亡率上,宮頸癌都是最常見的惡性疾病。在發達國家中,宮頸癌發生率的降低是重大公共健康成就之一,主要歸因于實施基于人群的篩查(population-basedscreening)以及侵入前疾病(pre-invasivedisease)的檢測和治療計劃。然而,雖然在發達國家中宮頸癌的發生率已降低,但在世界范圍內該疾病仍然是女性中第二常見的癌。
巴氏(papanicolaou,pap)涂片可檢測宮頸中的宮頸癌或癌前病變(pre-cancerouschange),其中很多與hpv相關。在實施廣泛篩查措施的發達國家中,這些pap涂片極大地降低了宮頸癌的發生率和死亡率。在篩查措施仍然十分有限的發展中國家中,宮頸癌是女性中最常報道的癌,并且其發生率持續升高。
宮頸上皮內異常(cervicalintraepithelialabnormalities)的所有現有治療(包括冷凍療法(cryotherapy)、激光消融(laserablation)、子宮頸錐切除(excisionalconization)和環形電切術(loopelectrosurgicalexcisionprocedure,leep))都是侵入性的手術過程,常導致明顯的副反應,包括分泌物過多、感染、出血、痙攣、子宮頸機能不全(cervicalincompetence),可導致流產、宮頸完整性喪失和無法懷孕。此外,這些過程必須在門診場所中進行,這增加了治療的成本。
子宮頸上皮內瘤形成(cin,cervicalintraepithelialneoplasia)是指宮頸癌的侵入前病理中間階段。在子宮頸的細胞涂片或組織活檢中觀察到的異常表現代表了子宮頸內皮細胞分化程度的改變。這種細胞發育異常分為三個不同嚴重程度的組:cini是指局限于內皮的基部1/3的輕微發育異常;cinii是指局限于內皮的基部2/3的病變;ciniii是指涵蓋大于內皮厚度2/3的細胞發育異常。
在美國,每年約350萬女性會有異常的pap涂片試驗。這些女性中約120萬患有鱗狀上皮內病變(squamousintraepitheliallesion,sil),其中的200,000至300,000人屬于晚期。在拉丁美洲,嚴重cin的發生率超過美國發生率的3倍。表1提供了世界范圍內hpv感染和cin流行程度的總結。
表1:世界范圍內hpv和cin的發病率
hpv感染在性活躍的個體中流行。具有多個性伴侶的女性獲得hpv的機會并因而獲得hpv相關子宮頸感染的機會更高。高風險hpv類型的感染增加了女性罹患宮頸癌的可能性。在hpv感染的女性中篩查和隨后治療癌前宮頸病癥對宮頸癌的預防高度有效。然而,當前的治療常需手術介入并且需要替代性的治療選擇。
技術實現要素:
本發明的一些方面涉及基于hpv的顆粒及其用于治療疾病和/或遞送治療劑的用途。在一些實施方案中,本發明的組合物和方法可用于治療粘膜疾病(例如,粘膜組織(例如粘膜內皮細胞)的疾病和/或感染)。
在一些實施方案中,本發明的一些方面涉及經修飾的基于hpv的顆粒,所述顆粒能將治療劑遞送到粘膜組織(例如,表面施用)。在一些實施方案中,所述治療劑可為抗病毒劑。所述抗病毒劑可用于治療病毒感染,例如,人乳頭瘤病毒、皰疹病毒或靶向粘膜組織的其他病毒。在一些實施方案中,所述治療劑可為抗癌劑。所述抗癌劑可用于治療例如宮頸癌或任何其他粘膜組織的癌癥。在一些實施方案中,本發明提供了用于治療人乳頭瘤病毒(humanpapillomavirus,hpv)感染的方法和用于治療對象中的hpv相關疾病(包括但不限于宮頸癌)的方法。然而,應當理解,本發明的經修飾病毒顆粒可用于遞送其他類型的治療劑和/或醫療劑(例如,成像劑或造影劑)。
在一些實施方案中,本發明的顆粒可局部遞送(例如,以乳膏、泡沫、噴霧劑、氣霧劑或其他適于表面遞送(topicaldelivery)的形式)至任何粘膜組織(例如,子宮頸、鼻、口腔或其他粘膜組織)。然而,本發明的一些方面不限于表面遞送,經修飾顆粒可皮下、靜脈內、胃腸外和/或通過任何其他適合的遞送途徑遞送。
本文中提供的方法包括將通過基于病毒樣顆粒(vlp)遞送系統遞送的一種或多種治療劑施用于對象。在某些實施方案中,所述基于vlp的遞送系統包含人乳頭瘤病毒樣納米顆粒。在一些實施方案中,hpv納米顆粒包含病毒l1蛋白。在一些實施方案中,hpv納米顆粒包含病毒l1蛋白和病毒l2蛋白。在一些實施方案中,所述l1和/或l2蛋白可為野生型病毒蛋白。在一些實施方案中,l1和/或l2蛋白可通過突變和/或插入/缺失而改變。在某些實施方案中,包含l1和/或l2的hpv納米顆粒的暴露于表面的環中的氨基酸發生突變、缺失和/或插入。在某些實施方案中,暴露于表面的環中的氨基酸的突變、缺失和/或插入導致hpv納米顆粒的免疫原性的改變。在某些實施方案中,免疫原性可以這樣的方式改變,使得某些血清型的hpv納米顆粒不再被對抗這種血清型的抗體所識別。在這些實施方案中,所述改變的hpv納米顆粒在具有所述血清型特異性抗體的宿主中是免疫沉默的。
因此,在一些實施方案中,可將本發明的基于hpv的顆粒進行修飾以使其具有降低或改變的免疫原性。可選擇這樣的顆粒遞送給具有中和性抗hpv應答的患者。在一些實施方案中,出于治療目的將一系列具有不同血清型的基于hpv的顆粒施用給對象,以降低中和性免疫應答對任一種所述血清型的作用。例如,可將第一血清型用于第一對象施用組(例如1、2、3、4、5、5-10或更多)。隨后,可將第二血清型用于第二施用組(例如1、2、3、4、5、5-10或更多)以降低對象針對所述第一血清型產生的中和免疫應答的影響。應當理解的是,其他施用組可涉及第三、第四、第五等血清型。不同的血清型可為天然血清型、嵌合血清型、其他突變血清型,或其任何組合。應當理解的是,可將該系列或順序施用用于特定化合物(例如每一種不同血清型中的同一個)或一系列不同的化合物在數月和/或數年時間段內的長期施用(例如,治療)。
在一些實施方案中,可以如下的方式向病毒衣殼蛋白l1和/或l2中引入氨基酸的突變、缺失和/或插入,使得所得的hpv納米顆粒不失去向所述靶細胞遞送治療劑的能力。在一些實施方案中,所述hpv納米顆粒未失去將核酸(例如,sirna或shrna)轉移進靶細胞的能力。
在一些實施方案中,可改變免疫原性以使某些血清型的hpv納米顆粒誘導產生交叉特異性中和性抗體的免疫應答。在這些實施方案中,這樣改變所述hpv納米顆粒,以使得其在其表面上表現出多個血清特異性表位(例如,通過在表面暴露環中插入表位)或使得其表現出血清型之間更保守的表位(例如,通過在表面暴露環中插入l2蛋白的部分,或者通過將保守的表位與hpv納米顆粒的表面相連)。在一些實施方案中,在hpv感染的個體中誘導交叉特異性中和性抗體的產生,其中所述hpv感染的個體已進行過治療以消除或減少hpv感染細胞的數目。在一些實施方案中,所述hpv感染的個體已進行過治療以消除或減少hpv相關腫瘤的大小。在這些實施方案中,可誘導交叉特異性中和性抗體的產生以產生足以對治療后剩余的hpv感染細胞進行免疫監視的免疫應答。在一些實施方案中,所產生的免疫監視足以阻止新的hpv感染或hpv感染的細胞的復育(repopulation),或hpv感染的腫瘤的復發。在一些實施方案中,交叉特異性中和性抗體可有效對抗一種或多種hpv血清型。
在一些實施方案中,由基于vlp的遞送系統遞送的治療劑為核酸。核酸治療劑可以是例如sirna或shrna分子或編碼它們的質粒。其他的治療劑可以是例如小分子,如具有抗病毒或抗癌活性的小分子。
在某些實施方案中,通過基于vlp的遞送系統給具有hpv感染或hpv相關癌癥(例如宮頸癌)或病變的對象施用一種或多種治療劑,導致殺死和/或清除hpv感染細胞。hpv感染的轉化細胞被認為是引起hpv相關癌癥或病變的原因。在一些實施方案中,殺死和/或清除hpv感染的細胞導致hpv相關癌癥的部分或完全緩解。
在一些實施方案中,本文中描述的所述治療方法可在用包含治療劑的hpv納米顆粒治療之前、同時或之后,與其他治療劑(例如,抗癌劑和/或抗病毒劑)和/或免疫調節劑和/或放射治療或免疫治療聯合施用。在一些實施方案中,所述抗癌劑和/或抗病毒劑可通過hpv納米顆粒遞送。在一些實施方案中,所述hpv納米顆粒和所述抗癌劑和/或抗病毒劑可一起施用或者可分別施用,例如,在不同時間或不同施用部位或者通過不同施用途徑施用。
在一些實施方案中,根據本文中描述的方法治療的對象中大多數或全部hpv感染細胞被殺死或清除,并且在hpv感染的對象中不再檢出hpv。在另一些實施方案中,對象中一些hpv感染的細胞被殺死或清除,并且在hpv感染的對象中仍可檢出hpv。在一些實施方案中,具有hpv相關病變或癌癥的對象可發生癌癥或病變的部分或完全消退。在一些實施方案中,對象未發生病變或癌癥或病毒感染的復發。在另一些實施方案中,對象經歷病變或癌癥或病毒感染的復發。在一些實施方案中,在用包含治療劑的hpv納米顆粒治療期間和/或之后,將本文所述的治療方法與抗病毒治療進一步聯合。可給予抗病毒治療以防止例如hpv復制、病毒擴散和/或具有在首次治療后存活的或已作為新感染進入對象身體的hpv之細胞的復育。
在另一些實施方案中,在初次治療方案結束時,施用改變的hpv顆粒。所述hpv納米顆粒進行如下改變,使得其在其表面上表現出多個血清特異性表位,或其表現出血清型間更保守的表位。在一些實施方案中,施用這種改變的hpv納米顆粒可誘導針對所施用表位的局部免疫應答,例如,誘導交叉特異性中和性抗體的增加,所述抗體足以使免疫監視能夠檢測并殺死新近被hpv感染的細胞。在一些實施方案中,阻止新病毒感染和/或擴散和復育足以抑制hpv相關癌癥或病變的復發。
在某些實施方案中,本文中描述的方法包括通過不同途徑施用包含一種或多種治療劑的hpv納米顆粒。在一些實施方案中,通過表面施用來施用hpv納米顆粒。在一些實施方案中,靶向粘膜進行表面施用。例如,包含一種或多種治療劑的所述hpv納米顆粒可表面施用至內皮(例如子宮頸內皮)或其附近,或者局部施用至病變(例如子宮頸或肛門內皮癌)或其附近。
在某些實施方案中,提供包含改變的病毒衣殼的hpv納米顆粒,其中如本文描述的那樣,通過野生型氨基酸的突變、額外氨基酸的插入和/或野生型氨基酸的去除來改變所述病毒衣殼蛋白。在某些實施方案中,所述改變的hpv納米顆粒在對象中或多或少是免疫原性的,或者具有改變的免疫原性。在一些實施方案中,所述改變的hpv納米顆粒保持將治療劑遞送或轉移至靶細胞的能力。
因此,本發明的一些方面涉及用于向對象遞送一種或多種化合物的方法和組合物。在一些實施方案中,使用修飾的人乳頭瘤病毒(hpv)樣顆粒,其中所述顆粒包含一種或多種包裝在hpv樣顆粒中的異源化合物,所述顆粒包含免疫原性改變的表面蛋白。所述異源化合物為非hpv分子(例如,不是hpv基因組、不是hpv核酸和/或不是其他hpv分子的化合物)。這樣的化合物可以是治療劑或其他醫藥化合物。在一些實施方案中,所述治療劑可以是下述中的一種或多種:治療劑或醫藥劑、核酸或小分子,或者成像劑或造影劑。在一些實施方案中,所述治療劑為sirna、shrna、反義核酸,或者編碼sirna、shrna或反義核酸的核酸。在一些實施方案中,所述sirna、shrna或反義核酸靶向hpv-e6和/或hpv-e7。在一些實施方案中,所述小分子是抗病毒劑。在一些實施方案中,所述小分子是抗癌劑(例如吉西他濱)。
應當理解,本發明的方法和組合物可以與一種或多種其他藥劑(例如,抗病毒劑、抗癌劑(例如吉西他濱),或其任何組合)一起提供。
在本發明的方法和組合物的一些實施方案中,所述hpv樣顆粒包含l1蛋白,或者包含l1蛋白與l2蛋白。在本發明的方法和組合物的一些實施方案中,所述表面蛋白是具有修飾的fg環序列的修飾的l1蛋白。在一些實施方案中,所述l1蛋白具有hpv16、hpv31、hpv33、hpv34、hpv35、hpv52、hpv58、hpv73或hpv91血清型的序列,并且其中所述l1蛋白的所述fg環具有一個或多個氨基酸改變,所述改變使人對象中所述蛋白的免疫原性發生改變。在一些實施方案中,所述一個或多個氨基酸改變發生在seqidno:11的x1-x17的一個或多個位點上。在一些實施方案中,在位置x16上的氨基酸沒有改變。在一些實施方案中,seqidno:11的x1、x2、x3、x5、x6、x11和x14中的一個或多個位置被修飾。在一些實施方案中,seqidno:11的x1、x2、x3、x5、x6、x11和x14中的2-3個位置被修飾。在一些實施方案中,seqidno:11的x1、x2、x3、x5、x6、x11和x14中的4-7個位置被修飾。在一些實施方案中,seqidno:11的x1、x2、x3、x5、x6、x11和x14中的3個位置被修飾。在一些實施方案中,seqidno:11的x6、x11和x14位置被修飾。在一些實施方案中,seqidno:11的x1、x2、x3、x5、x6、x11和x14的所有位置均被修飾。在一些實施方案中,所述l1蛋白具有hpv16血清型的序列,其seqidno:11的x6、x11和x14位置分別改變為t、t和n,seqidno:11的其余位置具有hpv16血清型的特征性氨基酸。在一些實施方案中,所述l1蛋白具有hpv16血清型的序列,其在位置x1、x2、x3、x5、x6、x11和x14分別改變為f、s、t、s、t、t和n,并且seqidno:11的其余位置具有hpv16血清型的特征性氨基酸。
應當理解,在一些實施方案中,向不具有針對表面蛋白血清型的中和免疫應答的對象施用hpv樣顆粒,例如,當所述對象未針對所述表面蛋白的血清型進行過免疫時,或當所述對象未感染過與所述hpv樣顆粒中表面蛋白血清型具有相同血清型的hpv時。在一些實施方案中,在選擇供施用的hpv樣顆粒之前,對所述對象的免疫應答進行評價。
在一些實施方案中,將hpv樣顆粒施用于粘膜組織。所述粘膜組織可在本文中描述的任何位置(例如,子宮頸、泌尿生殖道、口腔等)。此外,在一些實施方案中,將hpv樣顆粒施用于表皮位置(例如,以治療表皮癌或皮膚癌或感染)。
應當理解,本發明的組合物可局部和/或通過任何其他合適的途徑施用(例如,通過注射劑、氣霧劑、噴霧劑或其他施用形式施用)。
可將本發明組合物施用于被病毒、細菌和/或其他微生物或寄生蟲感染的組織。在一些實施方案中,感染部位可被幾種不同的有機體(例如,多種病毒和/或其他微生物,例如hpv和皰疹病毒(如hsv))所感染。因此,本發明的組合物可包含廣泛靶向幾種不同有機體的化合物,或包含各自靶向不同有機體的幾種不同化合物,或者其組合。在一些實施方案中,同樣的hpv樣顆粒可包含不同的治療化合物。在一些實施方案中,組合物或治療方案可包含兩種或多種不同的hpv樣顆粒,其各自含有靶向特定感染的化合物。
可將本發明的組合物施用給對象以治療癌癥(例如,在施用部位處或其附近)。在一些實施方案中,所述癌癥可以與感染(例如,hpv或hsv感染)相關。在一些實施方案中,所述癌癥可以與感染不相關。因此,本發明的一些方面可用于治療皮膚癌(例如,非黑色素瘤皮膚癌)。
在一些實施方案中,可將本發明組合物施用給具有免疫系統缺陷的對象,以治療與免疫系統缺陷相關的病癥(例如,感染、癌癥或其他病癥)。所述免疫系統缺陷可由感染(例如,hiv感染、aids)或其他病癥(例如癌癥)所引起。
在一些實施方案中,本發明的hpv樣顆粒可與促進非特異性免疫應答(例如,在施用部位或其附近)的組合物一起施用。所述非特異性免疫應答可有助于治療感染和/或癌癥或其他病癥。在一些實施方案中,應答于施用具有不同血清型的多種hpv樣顆粒的提高的免疫應答可能是有益的。因此,本發明的一些組合物包含幾種不同的血清型。
在一些實施方案中,可通過在第一段時間給對象施用包含化合物的第一hpv樣顆粒,并在第二段時間給所述對象施用包含所述化合物的第二hpv樣顆粒,以實現組合物的長期施用,其中所述第一和第二hpv樣顆粒具有不同的血清型。可使用其他血清型進行進一步施用。在一些實施方案中,所述第一和第二hpv樣顆粒的血清型獨立地為天然或改變的血清型。在一些實施方案中,所述第一和/第二hpv樣顆粒的血清型是嵌合血清型。
在一些實施方案中,本發明的組合物或方法可包括使用hpv樣顆粒,所述顆粒通過包含融合在l1環中的l2序列而具有嵌合血清型。在一些實施方案中,所述l2序列連接在l1顆粒的表面上。在一些實施方案中,所述l2序列由hpv31l2蛋白的13至88位殘基構成。
在以下非限定性的實施例和描述中,更詳細地描述了本發明的這些和其他方面。
附圖說明
圖1顯示了hpv-16的e6和e7基因的sirna的位置。
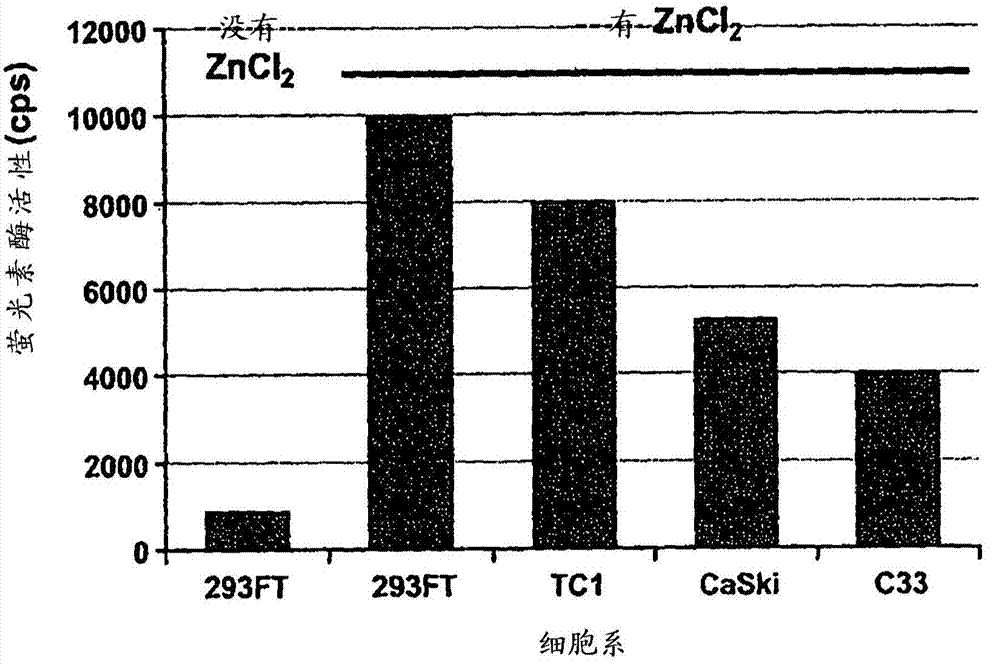
圖2顯示的條形圖表明zncl2在生產編碼螢光素酶的假病毒顆粒中的作用。在以未使用zncl2的重新組裝的假病毒顆粒轉染的293ft細胞中評價了螢光素酶基因的表達,并且在存在zncl2時產生的假病毒顆粒轉染的293ft、tc1、c33和caski細胞中評價了螢光素酶基因的表達。
圖3顯示了a)從以lacz、e6-1、e6-2、e7-1和e7-2的shrna轉染的caski細胞中提取的逆轉錄mrna。用e6和e7基因特異性引物和作為對照的甘油醛-3-磷酸脫氫酶(gapdh)引物pcr擴增了cdna。b)以lacz、e6-2、e6-1、e7-2和e7-1的shrna轉染的caski細胞(模擬組)的細胞提取物的western印跡的照片。使用p53和β-肌動蛋白抗體分析了提取物。
圖4顯示的條形圖表明了e6和e7的shrna對c33(灰色柱)、caski(黑色柱)和tc1(白色柱)細胞生長的作用。細胞(c)是以lacz、e6-1、e6-2、e7-1和e7-2的shrna轉染的。
圖5顯示的照片表明c57bl6小鼠中tc1腫瘤生長的抑制。將tc1細胞體外轉染。a)注射以單獨的vlp(底部)和e7-1假病毒顆粒(頂部)處理的tc1細胞之后獲得的腫瘤的比較。b)用shrna假病毒顆粒和shrna慢病毒(lentivirus)進行不同處理后腫瘤重量比較的定量柱形圖。
圖6顯示的圖表明腫瘤內注射對照shrna和e7-1shrna假病毒顆粒(pseudovirion,pv)后c57bl6小鼠中tc1腫瘤生長的抑制。a)第一次注射對照shrna或e7-1shrna假病毒顆粒之后腫瘤大小的(平均直徑)的演變。b)以對照shrna和e7-1shrna假病毒顆粒處理的小鼠中3周時的腫瘤重量。
圖7(a)顯示代表性的表面等離子體共振數據的圖。(b)顯示通過spr進行的由15種構象表位識別的hpv31mab間相互作用研究中構建的表位圖(epitopemap)。中和內化抗體以黑色顯示,中和細胞連接的以下劃線顯示。h31.d24抗體是非中和的(以方框顯示)。(c)以下劃線表示抑制vlp與肝素結合的aq5抗體。
圖8顯示hpv31l1蛋白的表位,所述表位通過使用細菌呈示法被非中和性mab(h31.d24)和四種中和性mab(h31.b1、h31.f7、h31.f16和h31.h12)所識別。
圖9描述附著前和附著后的假病毒顆粒的mab中和。(a)通過hpv31mab抑制hpv31假病毒進入。以hpv31mab預先孵育hpv31假病毒顆粒,并隨后加入細胞。(b)用hpv31mab抑制hpv31假病毒顆粒的內化。預先附著hpv31假病毒顆粒至細胞,并隨后添加hpv31mab。在圖的右側對使用細菌呈示方法研究的五種mab進行分組。灰色柱,中和性類型特異性mab;黑色柱,交叉中和的f7mab。
圖10描述vlp結合至hs和ecm:hpv31mab和l1c-末端缺失的作用。(a)用mab預孵育vlp之后,肝素結合的抑制。(b)用mab預孵育vlp之后,ecm結合的抑制。在圖的右側對使用細菌呈示法研究的五個mab進行分組。灰色柱:中和性類型特異性mab;黑色柱:f7交叉中和mab;空心柱:d24非中和mab。數值為抑制百分比和sd。大于50%的抑制被認為是陽性的。
圖11描述了具有或不具有c-末端缺失(d9和d31)的類型16和類型31的天然vlp(黑色柱)和變性的vlp(灰色柱)的肝素結合。
圖12描述了hpv31的fg環上被五種單克隆抗體識別的表位的位置。hpv31l1蛋白的fg環上被四種mab所識別的表位的位置。
圖13分別描述了hpv16和hpv31的fg環的序列比對,和插入hpv16fg環野生型序列中以產生嵌合體的突變(x和y)。
圖14描述的圖表顯示提取自轉染了wthpv16和嵌合體hpvx和hpvy的cos-7細胞的螢光素酶活性(計數/分鐘,cpm,countperminute)。
圖15描述的表格顯示以elisa檢測測量的來自免疫接種了hpv16、hpv31、hpvx或hpvy的小鼠的hpv16、hpv31、hpvx和hpvy特異性抗體的效價(幾何平均效價)(geometricmeantiter,gmt))。
圖16描述嵌合的vlpl1stii(a)和31l1-16l2(13-88)(b)的電鏡照片(標尺條(bar)=200nm)。
圖17描述的條形圖顯示通過elisa對嵌合的hpv16l1-stii、hpv16l1stiil2sa和hpv31l1-16l213-88vlp顆粒的抗原性的分析。使用camvir-1mab將結果針對l1反應性進行調節。結果表示為相對反應性,即用目的抗原獲得的od與用參比抗原(*)獲得的od之間的比值。使用針對構象(c)表位和streptagii或l2暴露的單克隆抗體在天然條件下分析顆粒。用h16.v5(c)、針對streptagii序列的單克隆抗體和多克隆的hpv16l2抗血清分析hpv16l1stii和hpv16l1stiil2sa。使用hpv16l1vlp和l1l231vlp為對照。使用h31.f16(c)和多克隆的hpv16l2抗血清分析hpv31l1-16l213-88vlp。結果為兩個重復的平均值。
圖18描述了l2蛋白表達的western印跡分析圖。1)純化的l2sa融合蛋白,2)與l1stiivlp相互作用后和3)與l1vlp相互作用后;在用4)編碼gfp的hpv58假病毒和5)用編碼l2的hpv58假病毒轉導轉導的cos-7細胞中。
圖19描述的圖表顯示hpv31、hpv58和hpv18中和性抗體的檢測。單個小鼠的中和效價為提供超過50%螢光素酶表達抑制的最后的倒數稀釋度。以標尺條(bar)表示幾何平均效價。
具體實施方式
本發明的一些方面涉及基于hpv顆粒的方法和組合物及其用于醫療和/或治療應用的用途。在一些實施方案中,使用基于hpv的顆粒遞送一種或多種藥劑(例如,治療劑、成像劑和/或其他醫療劑)至靶細胞或組織(例如,粘膜組織,例如粘膜組織表面)。
在一些實施方案中,本發明的一些方面涉及含有一個或多個天然hpv表面蛋白(例如,l1和/或l2蛋白)的hpv顆粒,并且其載有一種或多種醫療和/或治療劑,或其二種或更多中的組合。在一些實施方案中,本發明的一些方面涉及含有一種或多種變體表面蛋白(例如,變體l1和/或l2蛋白)的以修飾hpv為基礎的顆粒,其在對象中具有降低的或改變的免疫原性。所述修飾可為氨基酸序列的改變,以減少或避免被宿主的免疫系統所中和。在一些實施方案中,基于修飾的hpv的顆粒是含有重組hpv蛋白(例如,重組l1和/或l2蛋白)的顆粒,包括改變該蛋白在對象中(例如,在人類對象中)的免疫原性的一個或多個氨基酸改變。在一些實施方案中,基于修飾的hpv的顆粒具有改變的免疫原性,但保留了包裝并遞送分子至宿主的能力。因此,本發明的修飾的hpv顆粒可載有一種或多種藥劑(例如,代替hpv核酸)。可遞送這種顆粒至對象,而不誘導可被天然hpv顆粒所誘導的免疫應答。
本發明的一些實施方案可用于遞送一種或多種治療劑至患病組織(例如,患病的粘膜組織)。在一些實施方案中,患病的組織(例如,粘膜組織、上皮組織或上皮內組織)可為感染的組織(例如,感染了病毒,例如hpv或hsv)。在一些實施方案中,所述粘膜組織是宮頸組織并且所述疾病是發育異常或癌(例如,子宮頸發育異常(cervicaldysplasia),宮頸癌,例如與持續hpv感染相關的)。然而,在一些實施方案中,基于hpv的顆粒可被用于遞送組合物至其他組織(例如,表皮)。在一些實施方案中,基于hpv的顆粒可被用于治療hpv。然而,在一些實施方案中,基于hpv的顆粒可被用于遞送治療劑以治療其他疾病或狀況。
本發明的一些實施方案被用于遞送一種或多種成像劑或造影劑至對象。例如,可遞送量子點、金屬和/或其他成像劑。在一些實施方案中,可使用藥劑來追蹤早期階段的疾病(例如,早期階段的轉移)。在一些實施方案中,可使用放射敏感劑來增強放射治療的作用。在一些實施方案中,可遞送藥劑以誘導腫瘤細胞在其膜上表達不同的受體或糖。例如,本發明的一些方面可被用于遞送藥劑,所述藥劑促進腫瘤細胞中可增強免疫系統識別腫瘤的信號的表達(例如,可使腫瘤細胞看起來更像細菌或病毒的藥劑)。在一些實施方案中,可遞送藥劑以阻斷腫瘤細胞對糖的攝取。然而,應當理解的是,可遞送根據本發明的一些方面的任何合適的治療和/或其他醫療劑。
在一些實施方案中,本發明的一些方面涉及基于hpv的顆粒,所述顆粒被修飾以展示來自兩種或更多種不同天然hpv變體的表位。所述修飾的顆粒可用來提供針對任何兩種或更多種天然hpv變體感染的免疫。
在一些實施方案中,本發明的一些方面涉及施用一種或多種用于治療應用的不同hpv顆粒的方案。所述不同的hpv顆粒可以是不同的hpv變體、含有不同藥劑的基于hpv的顆粒和已在免疫原性方面經修飾的hpv顆粒的任何組合。
在某些實施方案中,可使用hpv納米顆粒來將一種或多種治療劑遞送至粘膜細胞(例如,hpv感染的細胞)。在另一些實施方案中,可以使用改變的hpv納米顆粒來將一種或多種治療劑遞送至靶細胞。在某些實施方案中,所述改變的hpv納米顆粒在具有血清型特異性抗體的宿主中是免疫沉默的。例如,感染了第一hpv血清型(例如,hpv-16)的對象產生出針對該血清型的抗體。在這樣的對象中,具有第一血清型(例如,基于野生型hpv16的vlp)的病毒顆粒可誘導免疫應答,所述免疫應答降低基于vlp的藥物遞送的效率。
在另一個實施方案中,可對對象針對hpv進行免疫(例如,用gardasil和cervarix)且所述對象已產生出針對第一和/或第二血清型(例如,hpv-16和hpv18)的中和性抗體。在這樣的對象中,具有所述第一和/或第二血清型的病毒顆粒(例如,基于野生型hpv-16和hpv18的vlp)可誘導免疫應答,所述免疫應答顯著降低基于vlp的藥物遞送的效率。
然而,可通過本文中所述的方法改變hpv納米顆粒,以使所述改變的hpv納米顆粒在宿主中不被所述第一血清型特異性抗體(例如,宿主中的hpv-16血清型特異性抗體)和/或宿主中所述第二血清型特異性抗體(例如,宿主中的hpv-18血清型特異性抗體)所識別。這種包含來自不同血清型的l1和/或l2蛋白的改變的hpv或hpv納米顆粒可用于治療。例如,所述改變的hpv納米顆粒或基于不同血清型的vlp可用于將一種或多種治療劑遞送至經hpv免疫或hpv感染的宿主,而不誘導血清型特異性的免疫應答和/或不被宿主應答所中和,并且不失去效力。這種改變的hpv納米顆粒或基于不同血清型的vlp可重復使用(例如,施用1、2、3、4、5、6、7、8、9、10次或更多次)以遞送治療劑。在某些實施方案中,所述對象會產生出識別改變的hpv納米顆粒或基于不同血清型的vlp的新抗體。此外,未感染hpv的對象可產生針對基于以治療目的施用給對象的hpv顆粒血清型的免疫應答。在這些情況下,可使用包含來自其他不同血清型的l1和/或l2蛋白的第二種不同的改變的hpv納米顆粒或第二hpv納米顆粒,以將治療劑繼續遞送至對象(例如,至hpv感染的細胞或者已被免疫接種針對hpv或用本發明的基于hpv的組合物治療的對象中細胞),而不誘導針對初始的hpv血清型和第二種改變的hpv納米顆粒的特異性免疫應答(例如,中和免疫應答)。在對象產生出針對含有第二種l1和/或l2蛋白的第二種改變的hpv納米顆粒或第二種vlp的免疫應答的情況下(或者為防止發生免疫應答),可使用含有第三種l1和/或l2蛋白的第三種改變的hpv納米顆粒或第三種vlp。可使用含有一系列不同的l1和/或l2蛋白的一系列不同的改變的hpv納米顆粒和/或不同的lvp重復該過程幾次。應當理解,在一些實施方案中,當在對象中檢測針對所述第一套的免疫應答時或在治療開始后的預定時間(例如,在施用第一組預定次數之后或預定時間之后)時第一組在對象中失去療效時,可從一組顆粒轉換到不同組的顆粒。
在某些實施方案中,根據hpv的基因型和/或血清型相似性來選擇基于不同血清型的vlp。在一些實施方案中,基于抗體的中和性交叉反應性選擇基于不同血清型的vlp。在一些實施方案中,基于與已在對象中產生中和性抗體的第一和/或第二血清型相關性最遠的不同血清型來選擇基于不同血清型的vlp。例如,hpv18與hpv45密切相關,并且表現出針對所述中和性抗體的高度交叉保護作用。hpv16與hpv31密切相關,并且表現出針對中和性抗體的高度交叉保護作用。hpv58與hpv16和hpv18的相關性更遠,沒有或幾乎沒有觀察到中和性抗體的交叉保護作用。
因此,治療系列可涉及施用本發明的一系列vlp組合物(例如,含有一種或多種治療劑),其中每種連續的vlp組合物均基于來自不同hpv血清型的vlp,例如,來自關系較遠的血清型。例如,在針對hpv16和hpv18免疫接種的對象中,基于不同血清型的適宜vlp可以是包含來自野生型hpv58的l1和/或l2蛋白的顆粒。
在另一個實施方案中,與已在對象中產生中和性抗體的所述第一和/或第二血清型關系很遠的vlp可選自不是hpv的乳頭瘤病毒。在一些實施方案中,vlp可包含來自感染非人的哺乳動物的乳頭瘤病毒的衣殼蛋白,例如,牛乳頭瘤病毒(bovinepapillomavirus,bvp)或棉尾兔乳頭瘤病毒(cottontailrabbitpapillomavirus,crvp)或shope乳頭瘤病毒。應當理解,治療系列可涉及基于不同hpv血清型和/或感染其他非人宿主的不同乳頭瘤病毒的一系列vlp。
可使用不同地改變的hpv納米顆粒或不同血清型的hpv納米顆粒來遞送治療劑,直到宿主產生出針對所述不同地改變的hpv納米顆粒或不同血清型的hpv納米顆粒的抗體。在某些實施方案中,使用上文中所述的方法,基于血清型差異和/或免疫應答改變突變來改變vlp,可用治療劑對對象進行多輪治療,而不會因對象的免疫應答而失去遞送系統的效力。在一些實施方案中,這種方案允許重復或持續治療hpv感染和/或hpv相關癌癥,直到基本上全部hpv感染細胞被清除和/或已發生癌癥或病變的緩解(部分或完全)。然而,應當理解,根據本發明的一些方面,所述方案可用于重復或連續治療其他病癥。
在一些實施方案中,使用hpv疫苗(例如,可商購的疫苗,例如gardasil和cervarix)對對象進行疫苗接種。在這些實施方案中,所述免疫可保護對象免受疫苗所靶向的病毒的感染(例如,對象在疫苗接種后已產生針對其的免疫應答的病毒)和發生這些疫苗特異性的病毒所引起的hpv相關疾病。然而,應當理解,當前可獲得的疫苗不會保護全部hpv基因型和/或血清型的感染。在一些實施方案中,hpv疫苗接種的對象會被不被所述疫苗所靶向的hpv(例如,高風險hpv)感染,例如,接種的對象尚未對其產生免疫應答的那些。在一些實施方案中,所述疫苗接種的對象經歷不同hpv類型感染的多次發生。在一些實施方案中,對象可被1、2、3、4、5、6、7、8、9、10或更多種不同的hpv類型感染,所述hpv類型感染并停留于所述對象的不同細胞中。在一些實施方案中,被高風險hpv感染的已接種對象可發生由高風險hpv(所述接種患者尚未針對其產生免疫應答)引起的hpv相關疾病,例如,hpv相關發育異常或癌癥。在這些實施方案中,可利用本文中所述的vlp,使用本文中所述的方法來治療所述對象。
例如,用可商用疫苗之一免疫接種過的對象可產生針對hpv16和18的中和性抗體,并且還可產生針對hpv6和11的中和性抗體。該免疫接種的對象受到保護而不發生這些hpv類型(hpv16、18(癌癥)和hpv6、11(疣)所引起的宮頸前癌和/或生殖器疣。免疫接種后已產生針對hpv16和18的中和性抗體的對象可產生與其他hpv類型表現出交叉反應性的一些中和性抗體(例如,hpv31(針對hpv16產生的中和性抗體)和hpv45(針對hpv18產生的中和性抗體))。然而,免疫接種的對象仍然會易感其他高風險hpv類型,因為對象并不針對這些類型產生交叉中和性抗體(例如,hpv58等)。可感染所述免疫接種對象的其他高風險hpv類型可以是例如hpv-33、hpv-35、hpv-39、hpv-51、hpv-52、hpv-56、hpv-59、hpv-68和hpv-69。如果所述免疫接種對象尚未產生出交叉中和性抗體,或者尚未產生出足夠特異性的交叉中和性抗體,或者尚未產生出足夠效價的交叉中和性抗體,則當對象被一種或多種高風險hpv類型(所述對象對其沒有產生足夠的保護)感染時,所述免疫接種對象仍處于發生hpv相關疾病(例如發育異常或癌癥)的風險中。
在這樣的對象中,可給對象施用本文中所述的修飾的vlp或包含一種或多種治療劑(例如e7sirna)的不同(關系更遠的)血清型(例如,基于hpv58的野生型vlp)的病毒顆粒,以治療對象的持續高風險hpv感染(所述對象對其沒有產生足夠的保護)引發的早期階段疾病。在該實例中,所述治療使得可消除早期發育異常,并且額外地可對對象提供更廣泛的針對其他額外hpv類型感染的交叉保護。
在一些實施方案中,hpv納米顆粒包含病毒l1蛋白。在一些實施方案中,hpv納米顆粒包含病毒l1蛋白和病毒l2蛋白。在一些實施方案中,所述l1和/或l2蛋白可以是野生型病毒蛋白。在一些實施方案中,l1和/或l2蛋白可通過突變和/或缺失而改變,從而所產生的l1和/或l2蛋白僅包含用于組裝納米顆粒的最“小”結構域。在一些實施方案中,l1和/或l2蛋白還可與提供額外功能的其他蛋白質和/或肽相融合。這些其他蛋白可以是病毒或非病毒蛋白,并且在一些實施方案中,可以是例如宿主特異性或細胞類型特異性蛋白。應當理解,vlp可基于含有一個或多個重組蛋白或其片段(例如,一個或多個hpv膜和/或表面蛋白或其片段)的顆粒。在一些實施方案中,vlp可基于天然顆粒,所述顆粒被加工以整合本文中所述的一種或多種藥劑,但本發明的方面并不限于所述方面。在某些實施方案中,可使用包含一種或多種靶向肽的顆粒。可以使用hpv蛋白或肽的其他組合,其作為本發明的一些方面,但本發明并不限于所述方面。
在一些實施方案中,通過突變、插入和缺失改變病毒野生型衣殼蛋白。迄今為止,所鑒定的全部構象依賴性類型特異性表位都發現于高變環中的hpv-vlp表面上,所述高變環中的氨基酸序列在hpv類型間高度多樣化,其被稱為bc、de、ef、fg和hi環。多數中和性抗體是針對這些多變環上的表位產生的并且是類型特異性的,其具有有限的交叉反應性、交叉中和和交叉保護作用。不同的hpv血清型誘導針對不同類型特異性表位和/或不同環的抗體。
本文中提供的方法將針對hpv特異性血清型而產生的抗體的有限交叉反應性用于治療。在某些實施方案中,病毒衣殼蛋白、hpvl1和/或l2在位于一個或多個高變環和/或表面暴露的環中的一個或多個氨基酸位置上,發生突變。在hpv血清型間不保守的環內的氨基酸位置上發生所述突變。這些位置可以是完全不保守的,即在該位置上可以是任何氨基酸,或所述位置可以是保守的,僅可進行保守氨基酸的改變。
可根據功能、化學或結構方面的考慮因素來進行保守氨基酸的改變。例如,可根據下述化學相似性進行保守氨基酸的改變:酸性(d/e)、脂肪族(a/g/i/l/v)、酰胺(n/q)、芳香族(f/w/y)、堿性(r/h/k)、羥基(s/t)、亞胺基(p)、硫(c/m);或功能相似性:酸性(d/e)、堿性(r/h/k)、疏水性(a/i/l/m/f/p/w/v)、極性(n/c/q/g/s/t/y);或電荷相似性:酸性、堿性、中性;或結構相似性:兼性(ambivalent)(a/c/g/p/s/t/w/y)、外部(r/n/d/q/e/h/k)、內部(i/l/m/f/v),其中括號中一組氨基酸中的任何氨基酸均可改變為本組中的其他氨基酸,并且,根據所用的考慮因素(例如結構、功能或化學),這樣的改變可被認為是保守改變。在一些實施方案中,可考慮一種或多種因素。
在某些實施方案中,可在一個或多個環中的一個或多個位置上引入氨基酸改變,所述改變在一個或多個氨基酸位置上和在一個或多個環中將一種血清型的野生型氨基酸序列改變為可見于其他hpv血清型中的氨基酸序列。例如,如果血清型x的一個環的氨基酸序列是abcdefg,而在不同血清型y的相同環中的氨基酸序列是abhijg(其中abcdefg和abhijfg是不同的氨基酸序列),那么ab和fg是保守的,而cde可能是突變的。可在血清型y的c或d或e,或者在cd或de或ce,或者在cde上引入突變。在這些實施方案中,c可突變為h,d可突變為i,并且e可突變為j。在這些實施方案中,所述一個或多個環可具有一種血清型的氨基酸序列(例如y),而蛋白的其余部分和(未改變的環)的其余部分是不同血清型的(例如x)。在這些實施方案中,僅一小部分的病毒衣殼蛋白突變。
表2顯示不同hpv類型的fg環比對的實例:
共有序列:
fvrhx1fnrx2gx3x4g(e/d)x5(v/i)px6dlx7ix8g(s/t)-gx9x10(a/g)
x11x12x13x14x15x16(f/y)(f/y)x17t
(seqidno:11)
表2中的例子顯示可在任何位置‘x’引入突變,并可在括號中標記的任何位置引入保守突變,而保留相同的保守氨基酸(黑體)。根據表2中的例子,本領域普通技術人員可對任何數目的hpv病毒的hpv序列對任何表面暴露的高變環進行比對,并且使用公知的比對軟件得出保守氨基酸和不保守的氨基酸,而無需過多的實驗。
在某些實施方案中,可對一個或多個氨基酸環進行一個或多個氨基酸改變,將一種血清型的非保守野生型氨基酸改變為其他血清型的等同野生型氨基酸。例如,根據表2的例子,hpv16的fg環的野生型氨基酸260位(l)可改變為(f),其等同于hpv31261位的等同野生型氨基酸。此外,hpv16的fg環的野生型氨基酸的264位(a)可改變為(s),其為hpv31265位的等同野生型氨基酸,等等。以這種方式,一種血清型的病毒衣殼蛋白的一個或多個環(例如,hpv16的l1的fg環)可改變,以或多或少精確模擬其他血清型相同病毒衣殼蛋白的環的氨基酸序列(例如,hpv31的l1的fg環),而保持衣殼蛋白的所有其他氨基酸為野生型(例如,hpv16的l1)。在一些實施方案中,以本文中所述的方式,將含有特異性血清型主要表位的一個或多個環的氨基酸改變為位于不同血清型中相同環的等同位置處的氨基酸,降低了hpv感染個體的免疫系統的hpv特異性抗體對病毒顆粒的識別。在一些實施方案中,所述改變的hpv納米顆粒是免疫沉默的,并且不被hpv感染的對象所產生的針對hpv的hpv特異性抗體所識別。例如,以hpv16免疫接種或感染的對象產生hpv16特異性的抗體。如果所述免疫系統遇到包含源自hpv16的野生型l1蛋白的vlp,則將發生免疫應答。然而,如果所述免疫系統遇到包含源自以本文中所述方法改變的hpv16的l1蛋白的vlp,則將不會(首先)發生hpv16特異性免疫應答。用改變的vlp重復攻擊后,接受所述改變的vlp的對象會產生針對所述顆粒的新免疫應答。在這種情況下,可使用不同地改變的vlp和/或來自其他血清型的vlp用于本文中所述的治療方法。
出乎意料的是,在一些實施方案中,在一種血清型的病毒衣殼蛋白的一個或多個環被改變以模擬其他血清型病毒衣殼蛋白的環的表位結構的情況下,包含所述改變的衣殼蛋白的vlp不被針對兩種血清型中任一種的中和性抗體所識別。根據本發明的一些方面,即使所述環(例如,fg環)含有主要表位,所述血清型也是由病毒衣殼蛋白的其余部分的表位所決定的。當僅有環被修飾而不改變病毒衣殼蛋白其余部分的序列時,獲得了新的血清型,其出乎意料地不被針對初始血清型(或當所述環的序列從第一血清型的序列改變為第二血清型的序列時的血清型)的抗體所識別。在一些實施方案中,可改變一個或多個位置以產生新的血清型,同時保留包裝和遞送藥劑(例如核酸(如rna或dna),例如重組核酸,例如本文中所述的治療性核酸)的能力。
在一些實施方案中,可改變fg環的位置x1、x2、x3、x5、x6、x11和x14中的一個或多個以產生新的血清型,所述血清型仍能夠包裝和遞送藥劑(例如,不同于hpv核酸的異源核酸(例如核酸如rna或dna,例如重組核酸,例如本文中所述的治療性核酸)。在一些實施方案中,第一l1蛋白的這些位置中的一個或多個從第一血清型的氨基酸改變為第二血清型的氨基酸。例如,在一些實施方案中,在所述第一(例如,hpv16)l1序列的情形下,x1、x2、x3、x5、x6、x11和x14中的所有位置可從第一hpv血清型序列(例如,hpv16血清型序列)改變為第二hpv血清型序列(例如,hpv31血清型序列)。在一些實施方案中,在所述第一(例如,hpv16)l1序列的情形下,僅x6、x11和x14從第一hpv血清型序列(例如,hpv16血清型序列)改變為第二hpv血清型序列(例如,hpv31血清型序列)。在一些實施方案中,x1、x2、x3、x5、x6、x11和x14的任何組合(例如,所述位置中的任何1、2、3、4、5、6或7個)可從第一血清型的氨基酸改變為第二血清型的氨基酸,而不改變l1序列的其余部分。應當理解,所述第一和第二血清型可以是任何合適的血清型(例如,hpv16、hpv31、hpv33、hpv34、hpv35、hpv52、hpv58、hpv73、hpv91,或具有特異性fg環序列的任何其他血清型)。還應當理解,在一些實施方案中,在l1序列或其部分未改變而保持包裝和遞送藥劑(例如,不同于天然hpv核酸的核酸,或本文中所述的任何其他藥劑)的能力的情況下,這些位置中的任何一個或多個可改變為任何保守或不保守的氨基酸(無論這種改變是否對應于其他天然血清型的氨基酸)。
在一些實施方案中,仍可包裝和遞送藥劑的經修飾hpv顆粒在l1蛋白的位置x16上沒有改變。例如,經修飾的hpv16可在其他位置上具有一個或多個改變,但在位置x16上保留精氨酸。
應當理解,中和性mab的主要表位已在hpv血清型間不同的一個或多個環上被鑒定。例如,對于hpv11在de環中,對于hpv6在bc環和ef環中以及對于hpv33在bc、de和fg環中,對于hpv16在fg環中和對于hpv31在ef環(例如,如fleury等prot.sci.2009中所述)。使用本文中所述的策略,本領域普通技術人員可比對已表明包含主要表位的其他環的序列,以產生其它的經修飾vlp。
還應當理解,在病毒衣殼蛋白中的任何氨基酸位置上(在一個或多個表面環中,在包含具有朝向內部的基團的氨基酸的位置上,或在衣殼蛋白中的任何其他位置上),可進行任何數目的氨基酸改變(突變、缺失、添加),以修飾或改變免疫原性或者出于任何其他原因(例如,誘導或阻斷構象改變、增加或降低帶電荷的氨基酸基團、改變靶向、增加生物利用度、誘導特異性修飾以增加通過特異性施用途徑的吸收),保持所述改變的衣殼蛋白形成vlp的能力,并且保持所得的vlp將治療劑轉移至靶細胞的能力。
還應當理解,可按本文中教導的和本領域中已知的關于位于環中的線性和構象表位的技術內容引入氨基酸修飾。構象表位可以是例如中和性抗體的識別位點,或者可以是對于細胞靶向而言有重要性的位點,或者可通過已經鑒定的vlp協助進入細胞(例如,如fleury等prot.sci.2009和sadeyen等virology,2002,309:32-40中所述,其內容通過引用全文并入本文)。可根據構象表位來設計環中一個或多個氨基酸的修飾,并且,除了非保守的氨基酸外,可包含一個或多個保守氨基酸的修飾。
在一些實施方案中,可將氨基酸序列插入環中。例如,可將短氨基酸序列插入一個或多個表面暴露的環中。所述短氨基酸序列插入片段可以是4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、30、35、40、45、50、55、60、70、80、90、100、150、200或250個氨基酸的長度,或4個氨基酸至250個氨基酸之間的任何長度。在某些實施方案中,所述插入片段的長度在4至50、5至25或5至15個氨基酸之間。所述插入片段可插入到環中的任何地方。在一些實施方案中,所述插入片段被插入到環的大致中間處。應當理解,如果已知某些環呈現某些基序,并且需要維持所述基序,則要將所述插入片段置于所述基序(無論是n端基序還是c端基序)之外。另外,如果需要破壞存在于某些環中的某些基序,則將所述插入片段置于所述基序中。所述基序可以是線性基序或結構基序,即其可以是基于一級氨基酸序列或其二級(或三級)結構。所述基序可以是可促進vlp攝取和/或靶細胞識別的細胞識別基序,或其可以是被某些抗體識別的表位,或其已知是抗原性的。在使用插入片段促進靶向或細胞吸收的一些實施方案中,所述插入片段可包含例如病毒靶向結構域。應當理解,這些結構域不限于hpv。病毒靶向結構域可源自靶向任何所需細胞的任何病毒。所述插入片段還可包含例如宿主特異性細胞識別基序,例如受體識別基序。在一些實施方案中,插入片段可包含氨基酸序列,所述氨基酸序列包含用作親和標簽的表位,例如streptagtm(stii,wshpqfek,seqidno:12)。
在一些實施方案中,使用插入片段來激發免疫應答。在這些實施方案中,所述插入片段可包含病毒來源(例如,來自多種hpv血清型)的一個或多個表位(例如,多表位(polytope))。例如,可構建包含多種hpv血清型l1蛋白抗原區(表位)的多表位,例如,hpv16、18、31、33和45。在一些實施方案中,可插入蛋白l2的區域。
在一些實施方案中,一個或多個表位的插入將在對象中產生針對所述一個或多個表位的免疫應答。在一些實施方案中,所述免疫應答賦予針對病毒(例如hpv)再感染和/或病毒復育(例如,源自抗病毒治療后剩余的病毒)和/或病毒相關癌癥復發(例如,抗癌治療后源自剩余的病毒轉化癌細胞)的保護。
在一些實施方案中,可將肽連接于vlp表面,以誘導改變的或增強的免疫應答(例如,如果所述肽包含一個或多個表位),或者以改變或增強vlp的靶向和/或細胞攝取(例如,如果所述肽包含一個或多個細胞受體)。例如,所述vlp可具有白蛋白結合結構域以增強其通過血管的轉運,或者具有肽的增強跨細胞作用(transcytosis)(例如,增強底部-頂部跨細胞作用的整合素結合(rgd)部分;硫酸肝素部分或其他部分)和/或受體特異性的結合結構域,以增強其被靶向細胞的吸收(例如egfr結合肽),和/或增強內體(endosome)和/或核轉運的肽。
在一些實施方案中,可使用合適的接頭(linker)通過化學交聯連接所述肽,所述接頭例如戊二醛、亞氨酸酯和bs(peg)9、bs(peg)5、dtssp、edc、sm(peg)2、smcc和磺基smcc(sulfosmcc)(thermoscientific)。
在一些實施方案中,所述肽可通過親和力標簽連接,例如streptagtm。
在一些實施方案中,所述肽為10、20、30、40、50、60、70、80、90、100、150、200、250、300、350、400、450或500個氨基酸的長度。
在某些實施方案中,可重組地生產l1蛋白和l1+l2蛋白。在某些實施方案中,重組生產的l1蛋白和li+l2蛋白可自組裝形成病毒樣顆粒(vlp)。重組生產可發生于細菌、昆蟲、酵母或哺乳動物宿主系統中。在所述宿主系統中,可表達l1蛋白或共表達l1+l2蛋白。
用于在宿主系統中表達和純化l1和l2重組病毒蛋白的方法,用于拆開和重新組裝hpv納米顆粒或vlp的方法,以及對l1和l2的氨基酸序列進行修飾、將vlp給施用對象的實例,和包含vlp的藥物組合物,是本領域中公知的,并且在本文中教導。例如,美國專利no:6,416,945;6,991,795和7,205,126,其通過引用并入本文。然而,應當理解,本文中提供的方法和模式并不限于上述美國專利中的描述。還可以采用本領域中已知的其他方法和模式。
在某些實施方案中,hpv納米顆粒或vlp載有一種或多種治療劑。如本文所述,可通過拆解和重新組裝l1或l1與l2病毒顆粒來加載hpv納米顆粒。可用于協助將病毒衣殼蛋白拆解/重新組裝為vlp的鹽包括zn、cu和ni、ru和fe鹽。可使用其他加載方法,因為本發明不限于這一方面。在一些實施方案中,hpv納米顆粒可在于一種或多種治療劑。
在一些實施方案中,包含l1蛋白或l1與l2蛋白的hpv納米顆粒還包含一種或多種治療劑。在某些實施方案中,所述治療劑包含一種或多種sirna分子,或者一種或多種核酸(例如質粒或其他載體),其每一種均能夠表達一種或多種sirna分子。在一些實施方案中,所述治療劑包含一種或多種反義核酸(例如anti-e6和/或anti-e7)、一種或多種核酸(例如質粒或其他載體),其每一種均能夠表達一種或多種反義核酸。在某些實施方案中,所述hpv納米顆粒包含兩種或更多種治療劑的組合。
在一些實施方案中,所述治療劑為rna干擾的誘導劑或基因沉默的其他誘導劑。rna干擾的誘導劑可以是sirna、shrna、雜交核酸分子,其包含第一部分和第二部分,所述第一部分包含雙鏈核糖核酸(rna)分子,所述第二部分包含單鏈脫氧核酸(dna)分子、更長的雙鏈rna或dna構建體(用于表達sirna或更長rna序列)。基因沉默的其他誘導劑包括dna甲基化誘導劑、或核酶、或適體(aptamer)。在另一些實施方案中,所述治療劑可以是基因表達的調節子,例如pna(肽核酸)。
rna干擾(rnainterference,rnai)是將雙鏈rna(doublestrandedrna,dsrna)引入細胞,以序列依賴的方式抑制翻譯后基因表達的過程。rnai可由短的(例如19至25個核苷酸)dsrna或小干擾rna(sirna)介導。在細胞中,dsrna被切割產生sirna,所述sirna被整合進rna誘導的沉默復合物(rna-inducedsilencingcomplex,risc)中,引導所述復合物至同源的內源性mrna,切割所述mrna轉錄本,并導致所述mrna的破壞。
為了在細胞中誘導rna干擾,可將dsrna作為分離的核酸片段或通過轉基因、質粒或病毒引入細胞。在某些實施方案中,使用vlp將dsrna遞送至靶細胞。
在一些實施方案中,細胞中表達短發卡rna(shrna,shorthairpinrna)分子。shrna包含由小環序列分隔的短反向重復序列。一個反向重復序列與所述目標基因互補。隨后,將shrna加工成為降解所述目標基因mrna的sirna。可在具有dna構建體的細胞內生產shrna,所述構建體在rna聚合酶iii啟動子(例如,人h1或7sk啟動子)的控制下編碼所述shrna序列。或者,可外源性合成shrna并直接引入細胞中,例如,通過vlp遞送。在某些實施方案中,shrna序列的長度在40至100個堿基之間,或者長度在40至70個堿基之間。所述發卡的莖(stemofthehairpin)為例如19至30個堿基對的長度。所述莖可含有g-u配對,以穩定所述發卡結構。
根據sirna序列與目標基因的同源性來對其進行選擇。可使用多種程序,包括blast程序(altschul等(1990)j.mol.biol.215:403-10)或bestfit(geneticscomputergroup,575sciencedrive,madison,wisconsin,usa,wisconsin53711)來確定兩個核苷酸序列之間的同源性。可使用fasta和fastp(見pearson&lipman,1988.methodsinenzymology183:63-98)進行序列對比。sirna、shrna和/或mirna的設計工具和質量是本領域中已知的。用于設計sirna序列和亂序sirna序列的基于網絡的在線軟件系統有例如sidirect、sisearch、seq2svm、deqor、sirnawizard(invivogen)。可使用例如specificityserver,miracle來預測特異性。可用例如husida(人sirna數據庫,humansirnadatabase)和sirnadb(sirna序列的數據庫)來研究目標序列。可在相關序列的全長范圍內進行序列對比,或者可更優選地在約10、15、20、25或30堿基的連續序列內進行對比。在某些實施方案中,sirna與所述目標基因之間同源性的程度為至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、或者至少99%或100%。所述sirna的長度可在10bp至30bp之間,或者在20bp至25bp之間,或者所述sirna的長度為20、21或22bp。
可通過用sirna轉染培養的細胞,繼之以目標mrna的rt-pcr來檢測rnai的發生。其中在sirna誘導rnai時,與對照細胞相比,轉染的細胞中目標mrna的水平將降低。可通過細胞裂解液的western印跡,繼之以用對目的蛋白有反應性的抗體進行探測來確證蛋白產生的降低。
在一些實施方案中,要沉默的基因是hpve6或e7基因。所述sirna序列可以是來自e6或e7基因序列中任何一個的10至30bp的任何連續序列,例如誘導rnai的hpv16或hpv18的序列。或者,可使用包含源自這些序列的連續序列的更長dsrna片段,因為其將在細胞內被切割形成sirna。
可使用本領域中已知的標準的固相或溶液相合成技術來合成sirna。可商業上獲得針對分別編碼hpv-16e6和hpv-18e6的mrna的合成sirna(例如,來自dharmaconresearch,lafayette,usa)。
在一些實施方案中,所述sirna在一端或兩端具有一個或多個脫氧胸苷堿基的突出端(overhang),以通過降低對核酸酶降解的敏感性來增加所述sirna在細胞內的穩定性。
在一些實施方案中,所述sirna為雜交的核酸分子,其包含第一部分和第二部分,所述第一部分包含雙鏈核糖核酸(rna)分子,所述第二部分包含單鏈脫氧核酸(dna)分子。
核苷酸之間的連接可以是磷酸二酯鍵或替代物,例如如下分子式的連接基團:p(o)s,(硫酯(thioate));p(s)s,(二硫酯(dithioate));p(o)nr′2;p(o)r′;p(o)or6;co;或conr′2,其中r是h(或鹽)或烷基(1-12c),r6是通過-o-或-s-連接到鄰近核苷酸上的烷基(1-9c)。
除了天然堿基之外,還可以使用經修飾的核苷酸堿基。例如,經修飾的堿基可提高所述sirna分子的穩定性,因而降低沉默所需的量。術語經修飾的核苷酸堿基包括具有共價修飾的堿基和/或糖的核苷酸。例如,經修飾的核苷酸包括含有糖的核苷酸,所述核苷酸共價連接至3’位置上的非羥基的低分子量有機基團和至5’位置上的非磷酸基團。因此,經修飾的核苷酸還可包括2’取代的糖,例如2’-o-甲基-;2-o-烷基;2-o-烯丙基;2’-s-烷基-;2’-s-烯丙基-;2’-氟-;2’-鹵代-或2疊氮-核糖,碳環糖類似物a-異頭糖;差向異構的糖,例如阿拉伯糖、木糖或來蘇糖、吡喃糖、呋喃糖和景天庚酮糖。
經修飾的核苷酸是本領域已知的,并且包括烷基化的嘌呤和嘧啶、乙酰化的嘌呤和嘧啶,以及其他雜環。這些類的嘧啶和嘌呤是本領域中已知的,并包括偽異胞嘧啶、n4,n4-乙胞嘧啶、8-羥基-n6-甲基腺嘌呤、4-乙酰基胞嘧啶、5-(羧基羥基甲基)尿嘧啶、5氟尿嘧啶、5-溴尿嘧啶、5-羧甲基氨基甲基-2-硫脲嘧啶、5-羧甲基氨基甲基尿嘧啶、二氫尿嘧啶、肌苷、n6-異戊基-腺嘌呤、1-甲基腺嘌呤、1-甲基假尿嘧啶、1-甲基鳥嘌呤、2,2-二甲基鳥嘌呤、2甲基腺嘌呤、2-甲基鳥嘌呤、3-甲基胞嘧啶、5-甲基胞嘧啶、n6-甲基腺嘌呤、7-甲基鳥嘌呤、5-甲基氨基甲基尿嘧啶、5-甲氧基氨基甲基-2-硫脲嘧啶、-d-甘露糖基q核苷(-d-mannosylqueosine)、5-甲氧基羰基甲基尿嘧啶、5甲氧基尿嘧啶、2甲硫基-n6-異戊基腺嘌呤、尿嘧啶-5-氧基乙酸甲酯、偽尿嘧啶、2-硫胞嘧啶、5-甲基-2硫脲嘧啶、2-硫脲嘧啶、4-硫脲嘧啶、5甲基尿嘧啶、n-尿嘧啶-5-氧基乙酸甲酯、尿嘧啶5-氧基乙酸、q核苷(queosine)、2-硫胞嘧啶、5-丙基尿嘧啶、5-丙基胞嘧啶、5-乙基胞嘧啶、5乙基胞嘧啶、5-丁基尿嘧啶、5-戊基尿嘧啶、5-戊基胞嘧啶和2,6,二氨基嘌呤、甲基偽尿嘧啶、1-甲基鳥嘌呤、1-甲基胞嘧啶。
在一些實施方案中,通過核酸序列(例如包含在本文中所述載體中的序列)的轉錄,可重組地制造sirna分子或更長的dsrna分子。所述載體可以是任何rna或dna載體。
所述載體可以是表達載體,其中所述核苷酸序列可操作地連接至與細胞相容的啟動子。適合在各種脊椎動物系統中使用的啟動子是本領域中公知的。例如,合適的啟動子包括病毒啟動子,例如哺乳動物逆轉錄病毒,或dna病毒啟動子,例如mlv、cmv、rsv、sv40iep(立即早期啟動子)和腺病毒啟動子和金屬硫蛋白啟動子。還可使用強哺乳動物啟動子。應當理解,還可使用基本保持相似轉錄活性的所述啟動子的變體。
在一些實施方案中,所述載體可具有至少兩個啟動子,一個指導dsrna有義鏈的表達,一個指導dsrna反義鏈的表達。在另一些實施方案中,可使用兩種載體,一種用于有義鏈,另一種用于反義鏈。或者,所述載體可編碼形成莖環結構的rna,其隨后被細胞切割產生dsrna。
所述核酸構建體可含有基因表達的特異性的細胞的、病毒的或其他啟動子或抑制子。所述啟動子或抑制子可被設計用于反映其中引入了構建體的細胞的環境。例如,所述構建體可含有病毒啟動子,因此,從所述構建體的表達有賴于病毒蛋白的存在,從而所述構建體僅在病毒感染的細胞中表達。類似地,所述構建體可具有某些細胞類型特異性的或某些發育階段特異性的啟動子或抑制子。例如,在所述載體是用在病毒感染的細胞中的情況下,例如hpv感染的細胞,應當使用與所述致病病毒相匹配的病毒啟動子,例如hpv啟動子(例如引起hpv16e6/e7表達的啟動子)用于hpv感染的細胞。在這樣的實施方案中,載體將僅在病毒感染的細胞中表達。
在某些實施方案中,sirna治療劑靶向促進或介導細胞死亡或靶細胞凋亡的靶標。在某些實施方案中,所述sirna治療劑靶向hpv病毒蛋白。在一些實施方案中,sirna分子所靶向的所述病毒蛋白是病毒e6和/或e7。已發現e6sirna強烈抑制病毒癌基因的表達,并且e6sirna表現出強效生長抑制活性(yoshinouchi等,2003)。sirna產生的e7沉默誘導凋亡性細胞死亡。不想受任何特別理論的限制,已描述合成的小干擾(smallinterfering,si)rna,特別是針對抗凋亡hpve7癌基因的sirna,在hpv陽性癌細胞中恢復休眠的腫瘤抑制子途徑(否則其在e7存在下失活),導致凋亡和細胞死亡。在一些實施方案中,sirna引起的e7沉默可足以導致感染的宿主細胞凋亡,而無需抑制e6(milner等)。描述了病毒e6和e7的sirna,例如在butz等(oncogene(2003)22,5938-5945)和milner等(專利申請0117359.0和0216929.0以及wo2005/051431),其通過引用并入本文。
在某些實施方案中,hpv-16e6和hpv-18e6可特異性地被sirna所靶向。在某些實施方案中,hpv-16e6的各靶標序列是
5′-uacaacaaaccguugugug(seqidno:13,377-395位核苷酸)。
在某些實施方案中,hpv-18e6的各靶標序列是
5′-cuaacuaacacuggguuau(seqidno:14,381-399位核苷酸)(如butz等中所述)。
在另一些實施方案中,e6和e7sirna構建體是:
e6(正向):5′gagguauaugacuuugcuutt(seqidno:15);
e6(反向):ttcuccauauacugaaacgaa5′(seqidno:16)
和
e7(正向):5′aggaggaugaaauagauggtt(seqidno:17);
e7(反向):ttuccuccuacuuuaucuacc5′(seqidno:18)
(如milne,wo2005/051431中所述)。
在另一些實施方案中,e6和e7shrna構建體為:
表3
(如在bousarghin等,molcancerther,2009,8:357-365中所述,其通過引用并入本文)。
在某些實施方案中,組裝成hpv納米顆粒的病毒野生型蛋白(例如,l1和/或l1+l2)的氨基酸發生突變和/或替換和/或缺失。在某些實施方案中,這些氨基酸被修飾以增強vlp內部的正電荷。在某些實施方案中,引入修飾以允許sirna分子與面向vlp內部的一種或多種氨基酸更強的靜電相互作用和/或避免sirna漏出所述hpv納米顆粒。
核酸是高度帶電的并且不能通過自由擴散穿過細胞膜。此外,sirna的親水特征和陰離子骨架降低了其被細胞的攝取。在某些實施方案中,治療性抗病毒sirna可被遞送至施用了hpv納米顆粒的對象以增加sirna的細胞攝取(在體內通過生物膜屏障)和/或生物利用度。
應當理解,包含僅促進hpv感染細胞之凋亡的藥劑的vlp組合物在一些實施方案中特別有用,因為它們靶向被hpv感染的細胞(例如,vlp表面組分靶向天然感染的hpv所靶向的相同細胞類型)并遞送殺死所述hpv感染細胞的藥劑。在一些實施方案中,這些組合物可用于治療hpv感染。在一些實施方案中,不需要長期治療,前提是施用合適的劑量(例如,單劑量或預定治療階段的療程,但不是長期治療)來殺所述hpv感染的細胞。然而,在一些實施方案中,本發明的組合物可能不足以殺全部的hpv感染細胞,并需要不只一個療程的治療和/或長期治療。在一些實施方案中,可使用包含抗病毒劑(而不是促凋亡劑)的vlp組合物用于長期治療。
在某些實施方案中,所述治療劑是抗癌劑。在一個優選的實施方案中,所述抗癌劑是吉西他濱。
在某些實施方案中,所述治療劑是化療劑,例如,甲氨蝶呤、長春新堿、阿霉素、順鉑、不含糖的氯乙基亞硝基脲、5-氟尿嘧啶、絲裂霉素c、博來霉素、多柔比星、達卡巴嗪、紫杉醇(taxol)、fragyline、葡甲銨gla、戊柔比星、卡莫司汀和聚苯丙生(poliferposan)、mmi270、bay12-9566、ras法尼基轉移酶抑制劑、法尼基轉移酶抑制劑、mmp、mta/ly231514、ly264618/洛美曲索(lometexol)、glamolec、ci-994、tnp-470、和美新(hycamtin)/拓撲替康、pkc412、伐司樸達(valspodar)/psc833、諾安托(novantrone)/米托蒽醌、metaret/蘇拉明(suramin)、巴馬司他、e7070、bch-4556、cs-682、9-ac、ag3340、ag3433、incel/vx-710、vx-853、zd0101、isi641、odn698、ta2516/馬立馬司他(marmistat)、bb2516/馬立馬司他(marmistat)、cdp845、d2163、pd183805、dx8951f、乳桿菌制劑(lemonal)dp2202、fk317、picibanil/ok-432、ad32/戊柔比星、metastron/鍶衍生物、temodal/替莫唑胺、evacet/脂質體多柔比星、yewtaxan/紫杉醇、taxol/紫杉醇、xeload/卡培他濱、furtulon/脫氧氟尿苷(doxifluridine)、cyclopax/口服紫杉醇、口服紫杉烷(oraltaxoid)、spu-077/順鉑、hmr1275/夫拉平度(flavopiridol)、cp-358(774)/egfr、cp-609(754)/ras癌基因抑制劑、bms-182751/口服鉑類、uft(tegafur/尿嘧啶)、ergamisol/左旋咪唑、eniluracil/776c85/5fu增強劑、campto/左旋咪唑、camptosar/伊立替康、tumodex/雷替曲塞(ralitrexed)、leustatin/克拉立平(cladribine)、paxex/紫杉醇、doxil/脂質體多柔比星、caelyx/脂質體多柔比星、fludara/氟達拉濱、pharmarubicin/表柔比星、depocyt、zd1839、lu79553/雙萘亞胺(bis-naphtalimide)、lu103793/多拉司他汀(dolastain)、caetyx/脂質體多柔比星、gemzar/吉西他濱、zd0473/anormed、ym116、碘粒(lodineseeds)、cdk4和cdk2抑制劑、parp抑制劑、d4809/dexifosamide、ifes/mesnex/ifosamide、vumon/替尼泊苷、paraplatin/卡鉑、plantinol/順鉑、vepeside/依托泊苷、zd9331、taxotere/多西紫杉醇(docetaxel)、阿糖鳥苷的前藥、紫杉烷類似物、亞硝基脲類、烷化劑例如美法侖(melphelan)和環磷酰胺、氨魯米特(aminoglutethimide)、天冬酰胺酶、白消安、卡鉑、苯丁酸氮芥、鹽酸阿糖胞苷、放線菌素d、鹽酸柔紅霉素、雌氮芥磷酸鈉、依托泊苷(vp16-213)、氟尿苷(floxuridine)、氟尿嘧啶(5-fu)、氟他胺、羥基脲(羥基尿素)、異環磷酰胺(ifosfamide)、干擾素α-2a、α-2b、醋酸亮丙瑞林(lhrh-釋放因子類似物)、洛莫司汀(ccnu)、鹽酸氮芥(氮芥)、巰嘌呤、美司鈉、米托坦(o.p′-ddd)、鹽酸米托蒽醌、奧曲肽(octreotide)、光神霉素、鹽酸甲基芐肼、鏈脲霉素、檸檬酸他莫昔芬、硫鳥嘌呤、塞替派、硫酸長春堿、安沙可林(amsrcrine(m-amsa))、阿扎胞苷、促紅細胞生成素(erthropoietin)、六甲三聚氰胺(hexamethylmelamine,hmm)、白介素2、米托胍腙(mitoguazone)(甲基-gag;甲基乙二醛雙-丙咪腙;mgbg)、噴司他丁(pentostatin)(2’脫氧助間型霉素)、司莫司汀(semustine)(甲基-ccnu)、替尼泊苷(vm-26)或硫酸長春地辛,但并不限于這些。
在某些實施方案中,所述治療劑是免疫治療劑,例如,ributaxin、赫賽汀(herceptin)、quadramet、panorex、idec-y2b8、bec2、c225、oncolym、smartm195、atragen、ovarex、百克沙(bexxar)、ldp-03、iort6、mdx-210、mdx-11、mdx-22、ov103、3622w94、抗vegf、賽尼哌(zenapax)、mdx-220、mdx-447、melimmune-2、melimmune-1、ceacide、pretarget、novomab-g2、tnt、gliomab-h、gni-250、emd-72000、lymphocide、cma676、monopharm-c、4b5、ioregf.r3、iorc5、babs、抗flk-2、mdx-260、anaab、smart1d10ab、smartabi364ab或immurait-cea,但不限于這些。
在某些實施方案中,所述治療劑為抗病毒劑。抗病毒劑的實例為:多硫酸鹽/酯(polysulfate,pvas)、多磺酸鹽/酯(polysulfonate,pvs)、多羧酸鹽/酯(polycarboxylate)、多金屬氧酸鹽/酯(polyoxometalates)、菊苣酸(chicoricacid)、津特韋(zintevir)、cosalane衍生物、雙環拉胺類(bicyclams)(即amd3100)、t-22、t-134、alx-40-4c、cgp-64222、tak-779、azt(疊氮胸苷)、ddi、ddc、d4t(二脫氫二脫氧胸苷)、3tc(3′-硫代二脫氧胸苷,3′-thiadideoxycytidine)、abc及其他ddn(2′,3′-二脫氧核苷酸)類似物、奈韋拉平、地拉夫定、依法韋侖、乙米韋林(mkc-442)、卡普韋林、對稱二苯硫脲(thiocarboxanilide)uc-781、阿昔洛韋、伐昔洛韋(valaciclovir)、噴西洛維、泛西洛維、溴乙烯去氧尿苷(bromovinyldeoxyuridine,bvdu,溴呋啶(brivudin))、西多福韋、阿德福韋二匹伏酯(adefovirdipivoxil)、替諾福韋二匹伏酯(tenofovirdisoproxil)、利巴韋林、伐昔洛韋、更昔洛韋、福米韋生、膦甲酸(foscarnet)、eicar(5-乙炔基-1-β-d-呋喃核糖基咪唑-4-甲酰胺,5-ethynyl-1-β-d-ribofuranosylimidazole-4-carboxamide)、霉酚酸、neplanocina、3-deazaneplanocina、6′-c-methylneplanocina、dhcea(9-(反式-2′,反式-3′-二羥基環戊-4′-炔基)腺嘌呤,或c3dhcea((9-(反式-2′,反式-3′-二羥基環戊-4′-炔基)-3-脫氮雜腺嘌呤),例如如declercqjpharmacolexpther2001,297:1-10中所述,其通過引用并入本文,但并不限于這些。
在一些實施方案中,本文中所述的rnai處理還包括用西多福韋(cidofovir)處理。西多福韋是用于治療例如hvp誘導的喉乳頭狀瘤病的抗病毒藥。西多福韋在宮頸癌細胞中也有活性。西多福韋可在基于vlp的rnai處理(例如,e6或e7特異性的sirna或shrna)之前、同時或之后施用。在一些實施方案中,西多福韋與rnai分子同時施用,并用本文中所述的vlp遞送。
其它的治療劑是例如信號轉導抑制劑,例如,絲氨酸-蘇氨酸激酶抑制劑、ras/mapk抑制劑、胰島素生長因子受體抑制劑、egfr和/或pdgfr抑制劑、抗血管生成劑如vegf和/或vegfr的抑制劑、parp調節劑和抑制劑、hedgehog通路抑制劑、與代謝通路的抑制相關的藥劑、β-干擾素、tdf或cprpmedap。
在某些實施方案中,以足以治療對象的量給對象施用包含一種或多種治療劑的hpv納米顆粒。在某些實施方案中,用包含一種或多種治療劑的hpv納米顆粒治療具有hpv感染的對象還包括施用抗癌劑和/或抗病毒劑。這些藥劑可同時或在不同時間共同施用,例如在施用包含一種或多種治療劑的hpv納米顆粒之前或之后。
在某些實施方案中,將包含一種或多種治療劑的hpv納米顆粒表面施用給感染hpv的對象。表面施用可包括以合適的藥物組合物或制劑的形式施用包含一種或多種治療劑的hpv納米顆粒。在某些實施方案中,所述適合表面施用的藥物組合物或制劑可以是凝膠或乳膏。在某些實施方案中,可將所述凝膠和乳膏施用于粘膜。
在某些實施方案中,將包含一種或多種治療劑的hpv納米顆粒施用于粘膜表面的上皮組織,例如,用于治療宮頸癌或結腸直腸癌。在這些實施方案中,包含hpv納米顆粒的藥物組合物還包含粘膜附著物質,例如聚合物。粘膜附著物質是粘著于體腔粘膜表面層或表面的任何制劑,所述表面包括胃腸道表皮的腔表面、結腸直腸上皮的腔表面和子宮頸的腔表面。粘膜上皮細胞層富含粘性分泌物(粘液)。粘膜附著聚合物具有附著至潮濕或濕潤的粘膜組織表面的能力,所述表面例如結腸直腸上皮或子宮頸上皮的粘膜組織表面。
可使用多種聚合物來形成凝膠、乳膏或其他附著物質,例如凝膠,如水凝膠、有機凝膠或熱可逆凝膠。其他可用的聚合物類型包括但不限于熱塑性塑料和膜。所述聚合物可以是例如,聚(環氧乙烷)、聚(乙二醇)、聚(乙烯醇)、聚(乙烯吡咯烷酮)、聚(丙烯酸)、聚(羥基乙基甲基丙烯酸酯)、羥乙基乙基纖維素、羥乙基纖維素和殼聚糖及其混合物、多糖(瓊脂)或羧甲基纖維素。在一些實施方案中,所述凝膠、乳膏或其他附著物質可含有提供粘膜附著作用的其他物質。這樣的材料包括二氧化鈦、二氧化硅和粘土。
可直接施用所述藥物組合物,例如作為凝膠施用,或其可被包含于預先組裝的貼劑或其他能使所述凝膠附著于所靶向的組織或細胞的裝置中(例如,如milner等wo2005/051431中所述)。例如,可采用附著于具有合適柔韌性的背襯層(例如,包含聚(氯乙烯)或羥丙基纖維素))以適應子宮頸表面組織結構的含有生物附著層或粘膜附著層的貼劑,以將包含治療劑和任選地額外治療劑(例如抗癌劑和/或抗病毒劑)的hpv納米顆粒治療性遞送至宮頸組織。所述貼片的物理特性應當理想地保持幾小時至一天或更多天,而不會使患者不適并且在正常的身體運動中不會移位。
在某些實施方案中,可以凝膠(例如,用于施用至所期望的靶區域的丙二醇甲基纖維素的制劑)的形式提供包含一種或多種治療劑的hpv納米顆粒。所述凝膠可提供在管中,例如50ma活性成分混懸于凝膠中。這些凝膠特別方便地用于施用于至皮膚或其他上皮表面(例如,子宮頸或肛門生殖器區域)。
在一些實施方案中,從長的施用器管(例如直腸或陰道施用器)中釋放所述凝膠,例如將其進行直腸或陰道內應用。然而,應當理解,本發明的組合物可以任何合適的形式施用,以到達hpv感染的細胞或其他靶細胞,因為本發明不限于這一方面。例如,可以以栓劑、膠囊劑、乳膏劑、凝膠劑、泡沫劑、噴霧劑、氣霧劑的形式提供本發明的組合物,和/或提供于材料的表面或浸漬于材料內,所述材料可與目標區域(例如,口腔、喉、子宮頸、陰道、肛門等)或其中兩種或更多種的任意組合相接觸。
在一些實施方案中,所述包含一種或多種治療劑的hpv納米顆粒還可以以乳膏或單晶或球丸(pellet)的形式施用,其可被施用于上皮表面或皮膚上,或者用16號套管針插入到上皮表面或皮膚內用于短期治療。
應當理解,可將本發明組合物施用于感染有hpv的對象(例如,診斷或已知具有持續性高風險hpv感染的對象),以治療發育異常或癌癥和/或防止發育異常或癌癥或其他與hpv感染相關疾病的發生。然而,在一些實施方案中,可將本發明的組合物施用(例如,預防性施用)給具有持續高風險hpv感染的對象,所述對象懷疑有被其他血清型高風險hpv感染的風險。
在將本文中所述組合物施用給個體的情況下,所述施用為“預防有效量”或“治療有效量”。根據需要施用最終組合物,其取決于所要治療的疾病和受影響面積的大小。例如,可以每天、每周或每月一次進行施用。
術語組合物的“有效量”是指組合物單獨或與其它給藥一起實現所需生物學作用的必要量或足夠量。當然,所需要的應答取決于所要治療的具體疾病。結合本文中提供的教導,通過在多種活性化合物中選擇并權衡多種因素(例如,效力、相對生物利用度、患者體重、不良副作用的嚴重程度和優選的施用方式),可設計有效的預防性或治療性治療方案,所述方案不引起明顯毒性,但卻完全有效地治療所述具體對象。對于任何具體施用而言的有效量可根據所治療的疾病或不良狀況、對象體重或者疾病或不良狀況的嚴重程度等因素而改變。通常,優選使用各個組份或其組合的最大劑量,即依據合理醫學判斷的最高安全劑量。然而,本領域普通技術人員應當理解,出于醫療上的原因、心理學原因或任何實際其他原因,患者可能堅持較低劑量或耐受劑量。本領域普通技術人員可以憑經驗確定有效量,而無需過多實驗。
對于本文中所述的任何化合物,可首先由動物模型確定治療有效量。治療有效劑量還可由已知表現出類似藥理學活性的化合物的數據來確定,例如其他納米顆粒。可基于所施用化合物的相對生物利用度和效力來調節所施用的劑量。根據上文中所述方法和本領域中公知的其他方法調節所述劑量以達到最大效力是在普通技術人員能力范圍之內的。
在某些實施方案中,提供了治療對象的方法。所述對象可以是任何哺乳動物。當用于不良狀況,例如病癥或疾病(例如癌癥、發育異常或腫瘤)時,本文中使用的術語“治療”是指預防性治療(其增加對象對發生所述不良狀況的抵抗力,或者,換句話說,降低所述患者發生所述不良狀況的可能性)以及在所述對象已經發生所述不良狀況后針對所述疾病的治療,或阻止所述不良狀況的惡化。
在某些實施方案中,本文中所述的治療方法適合于任何hpv感染對象。在某些實施方案中,提供了用于治療生殖器疣和/或尋常疣(verrucavulgaris)的方法。在某些實施方案中,提供了用于治療早期發育異常、cin(ii、iii)和/或原位癌的方法。在某些實施方案中,提供了用于治療宮頸癌和所有其他hpv相關發育異常(例如,唇癌、陰莖癌、口腔鱗狀細胞癌、頭頸癌或非黑素瘤皮膚癌)的方法。在某些實施方案中,提供了用于治療hpv感染后繼發感染的方法,例如單純皰疹病毒感染。在某些實施方案中,所述對象是人。在某些實施方案中,所述對象為雌性。
類似地,本發明的一些方面涉及治療一種或多種組織(例如,唇、陰莖、口腔、陰道、子宮頸、皮膚或其他組織感染)的感染。
在某些實施方案中,在hpv感染的對象中,包含l1或者l1與l2并且還包含一種或多種治療劑的hpv納米顆粒可靶向有變為癌細胞可能的hpv感染細胞。在某些實施方案中,包含l1或者l1與l2并且還包含一種或多種治療劑的hpv納米顆粒可靶向hpv感染的對象作為癌細胞的hpv感染細胞。
在某些實施方案中,給感染有hpv的對象施用包含一種或多種治療劑的hpv納米顆粒,在所述對象中殺死hpv感染的癌細胞。在某些實施方案中,給感染有hpv的對象施用包含一種或多種治療劑的hpv納米顆粒,引發所述對象中hpv感染的癌細胞的凋亡。
宮頸癌通常隨時間緩慢發展。在子宮頸中出現癌之前,子宮頸細胞經歷稱為發育異常的變化,其中不正常的細胞開始在宮頸組織中出現。隨后,癌細胞開始生長并更深入擴散進子宮頸和周圍區域中。
提供了在需要治療的對象中進行治療的方法。需要治療的對象優選為有hpv感染的對象。在一些實施方案中,所述對象處于感染的早期階段。在一些實施方案中,所述對象表現出早期子宮頸發育異常。在一些實施方案中,所述對象表現出cin。在一些實施方案中,所述對象表現出宮頸癌。
在一些實施方案中,所述方法包括以足以治療hpv感染的量將包含l1或l1與l2并且還包含一種或多種治療劑的hpv納米顆粒施用給hpv感染的對象。在某些實施方案中,將hpv納米顆粒表面施用于粘膜。在某些實施方案中,所述方法還包括施用抗癌劑和/或抗病毒劑。在一些實施方案中,所述一種或多種治療劑為sirna分子或sirna編碼分子。在某些實施方案中,所述sirna針對病毒e6和/或e7。在一些實施方案中,所述抗癌劑是吉西他濱。
在一些實施方案中,可使用vlp將抗癌劑至遞送患有癌癥的對象。
在某些實施方案中,可將所述包含一種或多種治療劑的hpv納米顆粒表面施用于上皮或其附近,所述上皮例如子宮頸上皮;或者表面施用于上皮病變處或其附近,所述病變例如宮頸癌或肛門上皮癌。在一些實施方案中,所述一種或多種治療劑為sirna分子或sirna編碼分子。
在一些實施方案中,所述包含一種或多種治療劑的hpv納米顆粒被置于用于上皮表面的表面用制劑中,例如,通過施用于惡性上皮,例如泌尿生殖系統腫瘤,例如肛門、陰道或子宮頸腫瘤,例如子宮頸cin。
在一些實施方案中,所述包含一種或多種治療劑的hpv納米顆粒制備成用于施用于上皮的表面制劑,例如,用于非黑素瘤皮膚癌的治療。
在一些實施方案中,所述一種或多種治療劑為sirna分子或sirna編碼分子。
在一些實施方案中,本發明的一種或多種hpv組合物或方法可與現有的用于hpv感染和/或宮頸癌的治療聯合使用。例如,可在使用表4中概括的治療技術之前和/或之后使用本發明的治療方法和/或組合物。
表4概括了當前用于cin治療的常見技術。
這些治療具有范圍在60至90%間的不同有效率。然而,所有這些治療都是侵入性的操作,其摘除或破壞宮頸組織并經常伴有并發癥。
宮頸癌的發病機制與持續的人乳頭瘤病毒感染密切相關(在zurhausen等中2002綜述)。乳頭瘤病毒是小的無包膜dna病毒,其二十面體衣殼由l1和l2蛋白構成,所述衣殼包封約8kb的閉合環狀雙鏈dna。直徑為50至60nm的病毒衣殼含有72個l1大蛋白五聚體和12至72個的l2小衣殼蛋白拷貝。
包括類型16、18、31、33、35、39、45、51、52、56、58、59、68和hpv-69的15種hpv的亞群被指定為高風險。高風險hpv基因幾乎見于100%的宮頸癌組織樣品中(walboomers等,1999)。在這種特定癌癥的發生中,病毒基因組的整合和隨后兩個主要病毒癌基因(e6和e7)的表達被認為是關鍵步驟。e6與p53腫瘤抑制蛋白結合,并將其靶向泛素介導的降解(münger和howley,2002)。p53指揮對多種應激刺激(例如電離輻射或化學治療藥物所引起的遺傳毒性損傷)的細胞應答。根據損傷的廣泛程度,p53的激活可導致細胞周期阻滯、dna修復機制的激活或細胞凋亡(vousden和lu,2002)。無功能的p53或p53不存在使得細胞分裂速率加快,并促進遺傳不穩定性,促進惡性轉化(attardi,2005)。高風險人乳頭瘤病毒(hpv)的e6和e7mrna的恒定表達分別消除了53和prb的功能,并且是宮頸癌發生所必需的。
此外,hpv16與一小亞類的頭頸部腫瘤相關,主要是瓦爾代爾環(waldeyerring)的組織。已證明,頭頸部其他部位的惡性病變(包括口腔癌和食管癌)中存在一系列hpv類型,包括低風險hpv類型(devillers等)。
世界范圍內,非黑素瘤皮膚癌(基底細胞癌和鱗狀細胞癌)是迄今白種人最常見的癌。這些癌癥主要發生于暴露于陽光的部位,表明uv輻射是該疾病發病中的主要環境因素。此外,還與幾種遺傳學變化相關,包括細胞基因p53中的突變。β-乳頭瘤病毒屬中幾種hpv類型似乎與皮膚的鱗狀細胞癌有關。這包括皮膚hpv類型(hpv20、hpv38和hpv27),其被uv激活或抑制。
因此,本發明的一些方面可用于治療與hpv感染相關的除宮頸癌以外的其他疾病。例如,本發明的一些方面可用于治療hpv感染相關的頭頸癌(例如口腔癌和/或食管癌)。然而,應當理解,本發明的基于hpv的顆粒可用作治療粘膜疾病或病癥(無論其是否是由hpv感染所引起的)的一般遞送載體。因此,可使用本發明的方法和組合物治療其他感染,例如hsv或hiv感染,和/或例如細菌感染,如陰道加德納菌(gardnerellavaginalis)、淋球菌(neisseriagonorrhoeae);真菌感染,如白色念珠菌(candidaalbicans)感染;或寄生蟲感染,如寄生蟲陰道毛滴蟲(trichomonasvaginalis);或生殖道中常見的其他感染。
在一些實施方案中,可使用包含一種或多種治療劑的hpv納米顆粒來治療持續的高風險hpv感染、子宮頸發育異常、前癌病變cini,ii,iii(cin2/3,vin2/3)和/或原位癌。
在一些實施方案中,可使用包含一種或多種治療劑的hpv納米顆粒來治療生殖器疣、非黑素瘤皮膚癌、頭頸癌、口咽癌、外陰癌、陰道癌、陰莖癌和/或肛門癌。
根據治療部位,可將本發明的組合物施用給女性或男性對象。
在一些實施方案中,可使用包含基于hpv的vlp組合物將治療劑遞送至上皮細胞,例如皮膚。在一些實施方案中,可使用所述組合物治療革蘭氏陽性細菌引起的表皮感染,所述細菌包括例如葡萄球菌(staphylococcus)、微球菌(micrococcus)和棒狀桿菌(corynebacterium)屬、金黃色葡萄球菌(staphylococcusaureus)以及化膿性鏈球菌(streptococcuspyogenes),其引起例如皮膚疾病,如膿皰瘡(impetigo)和臁瘡(ecthyma)。在一些實施方案中,包含基于hpv的vlp的組合物可用于治療非黑素皮膚癌。
在一些實施方案中,如本文中所述,可全身施用(例如靜脈內注射(i.v.))包含一種或多種治療劑的經修飾hpv顆粒來治療腫瘤,例如卵巢癌、乳腺癌、口腔鱗狀細胞癌、頭頸癌、nsclc、sclc、膀胱癌或前列腺癌。在一些實施方案中,如本文中所述,癌細胞呈示出hpvvlp和修飾的hpv顆粒的受體,可用于靶向這些癌細胞。在一些實施方案中,還可額外地改變經修飾的hpv顆粒以呈示出腫瘤細胞特異性的靶向劑。
本發明的一些方面在其應用上不限于在上文的說明書中提出的,或者在實施例或附圖中舉例說明的構建細節和組成安排。本發明的一些方面能夠以多種方式實施其他實施或施行方案。另外,本文中使用的用語和術語僅是為了說明的目的,而不應當認為是限制性的。本文中使用的術語“包括”、“包含”或“具有”、“含有”、“涉及”及其變化形式旨在包括其后列出的項目及其等同物以及額外的項目。
實施例
實施例1:包裝了hpv癌蛋白shrna的hpv-vlp對宮頸癌細胞生長的抑制
本研究的主要目的是構建基于hpv的shrna表達系統并探究利用hpv介導的rna干擾進行有效的e6和e7基因沉默。我們在此表明,在宮頸癌細胞中表達e6和e7shrna的hpv假病毒顆粒導致e6和e7表達的消除和癌細胞生長的抑制,提示hpvvlp可用于遞送編碼用于治療宮頸癌之shrna的質粒。
材料和方法
細胞系、細胞培養物和細胞轉染
在37℃下,在含有5%co2的加濕氣氛中,將人宮頸癌細胞系caski(atcccrl-150)和c33-a(atcchtb-31,美國模式培養物保藏中心(americantypeculturecollection))培養于添加有10%fcs(invitrogen)、1%青霉素/鏈霉素和1%丙酮酸鈉的dmem中。用hpv-16轉染caski細胞并表達e6和e7,而c33-a細胞為hpv陰性。以hpv-16e6/e7癌蛋白和c-has-ras共轉染小鼠細胞系tc1(atcccrl-2785)。這些細胞生長于添加有2mmol/l非必需氨基酸和10%fcs的含有10mmol/lhepes、1mmol/l丙酮酸鈉的rpmi1640中。小鼠293ft細胞(invitrogen)源自293t細胞系(atcccrl11268)。其表達sv40大t抗原,并在500μg/ml遺傳霉素(invitrogen)存在下進行培養。
轉染前一天,將細胞用胰酶消化并接種進六孔板中。隨后使用lipofectamine2000(invitrogen),用編碼shrna的質粒轉染細胞,或用hpv-31假病毒顆粒或編碼shrna的慢病毒轉染細胞。收獲細胞,以在結果中標出的不同時間進行分析。
設計和生產表達e6和e7特異性shrna的質粒
為生產pentr/u6進入克隆(entryclone),使用了block-itu6進入載體(entryvector)。我們首先設計并合成了互補dna寡核苷酸(invitrogen),每個含有定向克隆所必需的4個核苷酸突出端(overhang)。圖1b中描述了對應于e6和e7shrna的互補序列。使用invitrogen的“shrnadesigner”軟件選擇e6-2和e7-2序列。e6-1和e7-1序列是jiang和milner(oncogene2002;21:6041-8)描述的序列。我們使用jiang和milner(oncogene2002;21:6041-8)所描述的lacz和對照shrna序列作為對照。用blast確認了所有序列的特異性。
在95℃時,通過在退火緩沖液中孵育4分鐘,使等量的正向和反向鏈寡核苷酸退火生成雙鏈寡核苷酸。生成雙鏈寡核苷酸之后,將其連接進入penter/u6載體(invitrogen)中。將所述質粒測序、擴增并使用qiagen質粒小提試劑盒(qiagen,france)純化。將進入克隆用于瞬時rna干擾分析。
生產表達e6和e7shrna的hpv假病毒顆粒hpv-引
在以重組桿狀病毒(baculovirus)轉染的sf21細胞中表達vlp,所述桿狀病毒編碼密碼子優化的hpv-31l1和l2基因(fleury等,clinvaccineimmunol2008;15:172-5)。在27℃下孵育細胞72小時(touze等,nucleicacidsres1998;26:1317-23;bousarghin等,jclinmicrobiol2004;40:926-32)。離心收集細胞,將其重懸于含有0.5%np40的pbs中,并使其在室溫下靜置30分鐘。隨后,將細胞裂解液在4℃下以14,000×g離心15分鐘。將核酸級分進一步重懸于pbs中并超聲處理。隨后將所述片段上樣至預制的氯化銫梯度的頂部并在beckmansw28轉子中平衡離心(24h,27,000rpm,4℃)。將l1陽性級分合并于pbs中并離心(sw28轉子,3h,28,000rpm,4℃)。將vlp重懸在0.15mol/l的nacl中。
如前所述(touze等,nucleicacidsres1998;26:1317-23),并做了一些修改,生成了假病毒顆粒。簡而言之,在室溫下,將1μgofhpv-31vlp在含有20mmol/ldtt和1mmol/legta的50mmol/ltris-hcl緩沖液(ph7.5)中孵育30分鐘。在該階段,向破壞的vlp中添加編碼shrna、螢光素酶或綠色熒光蛋白的表達質粒(100ng)。隨后用有或沒有zncl2(10nmol/l)的cacl2不斷增加的濃度(最高達5mmol/l終濃度)稀釋該制備物。使用zncl2是因為據報道zncl2可促進hpv殼粒(capsomer)組裝成vlp(hanslip等,biotechnolprog2006;22:554-60)。隨后,將假病毒顆粒用1×pbs透析過夜,并在使用前存儲于4℃。
用電子顯微鏡分析殼粒、vlp和假病毒顆粒的存在。為此,將樣品應用于碳包網格(carbon-coatedgrid),用1.5%乙酸鈾酰(uranylacetate)負染色,并使用jeol1010電子顯微鏡在×50,000標稱放大倍數下觀察。
生產表達e6和e7hrna的慢病毒
使用block-it慢病毒rna干擾表達系統(invitrogen)進行慢病毒的生產。簡而言之,進行編碼e7shrna的pentr/u6質粒和plenti6/block-itdest之間的lr重組反應,生成plenti6/block-it-dest表達構建體。通過使用lipofectamine2000(invitrogen)以9μg的virapowerpackagingmix和3μg的plenti6/block-it-dest表達質粒dna轉染293ft細胞來生產慢病毒。轉染后48小時收集細胞培養上清液。通過用系列稀釋的慢病毒感染tc1細胞來測定表達e7shrna的慢病毒的效價。所述慢病毒儲備液效價為1×106tu/ml。通過將細胞進行殺稻瘟菌素(10μg/ml)選擇來選擇穩定轉導的tc1細胞。
通過逆轉錄pcr分析e6和e7mrna的水平
用1×pbs清洗shrna假病毒顆粒轉染的caski細胞(106),隨后根據制造商的說明書,使用dynabeadsmrnadirect試劑盒(dynalfrancesa)分離mrna。在42℃下,在含有250μmol/l每種脫氧核苷三磷酸、5μmol/l寡核苷酸(dt)20、25單位的rna酶抑制劑和20單位的禽成髓細胞血癥(myeloblastosis)病毒逆轉錄酶(rochediagnostics)的1×孵育緩沖液中,通過逆轉錄1小時由mrna合成單鏈cdna。使用hpv-16e6、e7或甘油醛-3-磷酸脫氫酶(gapdh)特異性的正向和反向引物,對cdna樣品進行pcr擴增。使用的引物為
e6正向,5’caccaaaagagaactgcaatgt3’(seqidn0:31);和反向,ttgctgttctaatgttgttcca(seqidn0:32);e7正向,5’ggagatacacctacattgcatga3’(seqidno:33);和反向ggggcacacaattcctagtg(seqidno:34);甘油醛-3-磷酸脫氫酶正向,5’acagtccatgccatcactgcc3’(seqidno:35);和反向,5’gcctgcttcaccaccttcttg3’(seqidno:36)。在geneamp9700溫度循環器(pekinelmerappliedbiosystems,france)中,以200μmol/l的脫氧核苷酸三磷酸、2μmol/l的每種特異性引物和1單位taq聚合酶(invitrogen)進行pcr,對于e7、e6和gapdh,程序分別為在50℃、55℃或62℃下進行25個循環。在2%的瓊脂糖凝膠上使pcr產物可視化并用geldoc系統(bio-rad)進行分析。
p53的檢測
將細胞(2×105)用pbs1×清洗,直接溶于50μlsds凝膠加樣緩沖液中,并在95℃下孵育10分鐘。將15微升每種樣品在12%sds-page凝膠上分離。將分離的蛋白電轉印到硝酸纖維素膜上用于抗體檢測。使用單克隆抗體do-1(santacruzbiotechnologies)檢測人p53蛋白,并使用多克隆抗體(sigma)檢測內源性β-肌動蛋白。使用堿性磷酸酶綴合的抗小鼠igg抗體(sigma),以硝基藍四氮唑(nitrobluetetrazolium)和磷酸溴氯吲哚(bromochloroindolylphosphate)(sigma)為底物使結合的抗體可視化。
β-半乳糖苷酶和螢光素酶活性的檢測
在用pbs1×清洗過并用含有2%甲醛和0.2%戊二醛的pbs固定過的細胞中,用β-半乳糖苷酶質粒和laczshrna轉染的caski、c33-a和tc1進行β-半乳糖苷酶的檢測。室溫下10分鐘后,清洗細胞,并與β-半乳糖苷酶呈現溶液(β-galactosidaserevelationsolution)(2mmol/lmgcl2、4mmol/l亞鐵氰化鉀、4mmol/l鐵氰化鉀和1mg/mlx-gal)一起孵育。對顯示β-半乳糖苷酶活性的藍色細胞進行計數。通過發光檢測測量螢光素酶基因表達(螢火蟲螢光素酶測定試劑盒;interchim)。在10s范圍內對發光進行積分(victor2,wallac;perkin-elmer),結果表示為計數/秒(cps)/孔。
細胞活力測定
將轉染和未轉染的細胞用胰酶消化并隨后接種進96孔板中。向加有100μl無fcs的dmem的細胞中加入3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑溴化物(0.5mg/ml)并在37℃下孵育。2小時后,添加100μl異丙醇和0.4mmol/lhcl,并在540nm測量吸光度。細胞活力測定為測試孔中獲得的吸光度與未處理細胞中獲得的吸光度之間的比值。
細胞凋亡測定
使用抗ssdna/apostain(abcys)檢測細胞凋亡。簡而言之,用含有1μge6-1、e6-2、e7-1、e7-2shrna和對照shrna的10μg假病毒顆粒轉導生長在六孔板中的tc1細胞(2×105個)。轉染2天后,收獲上清液,將細胞用冰冷的乙醇固定。離心之后,室溫下將5×105個固定的細胞重懸于250μl甲酰胺中5分鐘,隨后在75℃下孵育10分鐘。在該步驟后,添加2ml含有1%脫脂奶粉的pbs。15分鐘后,將細胞離心,并將濾餅重懸于100μl含有抗ssdna單克隆抗體f7-26的pbs中。在15分鐘的孵育和離心之后,將濾餅重懸于100μl含有熒光綴合的抗小鼠igm(20μg/ml,在pbs和1%脫脂奶粉中)的pbs中。孵育15分鐘后,將細胞清洗、離心并重懸于500μl含有1μg/ml碘化丙錠的pbs中。用小鼠igm而不是特異性的一抗處理陰性對照。隨后使用coulterxl流式細胞儀并利用expo32軟件(beckmancoulter,france)分析細胞。
還使用caspase-glo3/7檢測試劑盒(promega)研究了細胞凋亡。如前所述,利用不同shrna轉導細胞。轉導后兩天,將2×105個細胞轉移至白色壁的96孔板(perkin-elmer)的每個孔中,并添加100μl半胱天冬酶(caspase)發光底物。室溫孵育1小時后,在luminoscanascent發光儀(thermoelectron)上讀取板的發光。
小鼠模型中抗腫瘤作用的評價
為了研究e6和e7shrna假病毒對tc1細胞致瘤性的作用,給6組(5只小鼠/組)6周齡的雌性c57bl6小鼠(cerj,legeneststisle,france)皮下接種tc1細胞(2×105個)。在施用于小鼠之前,用假病毒顆粒(10μgvlp/1μge6-1或e7-1shrna)、用編碼e7-1shrna的慢病毒(復數感染,50)或使用含有lipofectamine的1μge7-1shrna轉染tc1細胞。對照組接受未處理的tc1細胞(模擬組),而一個對照組接受hpvvlp處理的tc1細胞。3周之后,處死小鼠,切除腫瘤并稱重。
還在具有tc1細胞腫瘤的小鼠中研究了編碼e7shrna的假病毒顆粒的抗腫瘤效力。用tc1細胞(2×105)皮下(s.c.)接種兩組(10只小鼠/組)6周齡的雌性c57bl6小鼠。接種后七天,全部小鼠中均已形成明顯的腫瘤,以20μgvlp/2μge7-1或20μgvlp/2μg對照shrna的劑量,將含有shrna的假病毒顆粒直接注射進每個腫瘤中,每2天一次,注射2周。3周后,處死小鼠,取出腫瘤并稱重。所有動物研究都經過地區動物倫理委員會(regionalanimalethicscommittee,creea)的批準。
統計學分析
數據表示為均值±se。使用t檢驗進行統計學分析,p<0.05認為是有顯著性。
結果
設計導向hpv-16的e6和e7蛋白的shrna
設計6個序列以促進特異性的沉默。這些序列中的兩個,即sie6-1(138-159)和sie7-1(101-119)已經作為sirna在jiang和milner(oncogene2002;21:6041-8)中描述,分別對應于e6和e7的兩個其他序列sie6-2(421-441)和sie7-2(148-167)是通過使用invitrogenshrna設計器軟件選擇的,并且兩個序列(laczshrna和jiang的對照shrna)用作對照(圖1和表3)。將這些序列退火并插入pentr/u6中。
為了研究假病毒顆粒系統用于遞送shrna的有效性,使用或不使用編碼laczshrna的pentr/u6lacz質粒,用編碼h半乳糖苷酶的質粒轉染tc1、caski和c33-a細胞。在laczshrna存在下,在所研究的全部細胞系中均觀察到了h-半乳糖苷酶表達的降低,在tc1、caski和c33-a細胞中分別為80%、83%和81%抑制。
在zncl2存在下通過將l1殼粒組裝成vlp來生產編碼shrna的假病毒顆粒
使用hpvvlp來包封編碼e6和e7shrna的質粒。為了生成這些假病毒,我們使用了前述的拆解-重新組裝法,只是在重新組裝過程中添加了zncl2作為修改。簡而言之,在含有egta和dtt的緩沖液中孵育純化的vlp,在這些條件下,vlp完全解體為組裝成殼粒的結構。隨后添加e7-1shrna質粒,并在有或沒有zncl2(10nmol/l)存在下,用含有1%dmso和5mmol/lcacl2的緩沖液稀釋該制備物,以重新折疊所述vlp。zncl2的存在促進了顆粒重新組裝為類似假病毒顆粒的結構。在zncl2存在下,所述殼粒還組裝成為直徑為24nm的管狀結構,長度從120至280nm不等。通過比較使用或不使用zncl2所獲得的所述假病毒顆粒制備物轉導293ft細胞的能力來評價zncl2在生產含有編碼螢光素酶之質粒的假病毒顆粒中的作用。在zncl2存在下生成的假病毒顆粒獲得了9,981cps的螢光素酶活性,而沒有zncl2時獲得的假病毒顆粒則為僅845cps。因此,當l1顆粒在zncl2存在下重新組裝進vlp時,觀察到了螢光素酶活性增加了12倍(圖2)。此外,研究了所述hpv假病毒顆粒轉導caski、c33-a和tc1細胞的能力。該假病毒顆粒轉導了所研究的全部細胞系(圖2)。然而,與在caski細胞(5,232cps)或c33細胞(4,016cps)中的相比,在tc1細胞(7,990cps,計數每秒,countspersecond)中觀察到了更高水平的螢光素酶表達。在不存在假病毒顆粒時,在293ft、tc1、caski和c33細胞中觀察到的螢光素酶活性分別為57、84、51和41cps。
e6和e7shrna假病毒顆粒對caski細胞的轉導誘導了基因沉默和細胞生長抑制的提高
使用含有編碼綠色熒光蛋白之質粒的假病毒顆粒來研究假病毒顆粒在細胞中基因轉移的效力。通過流式細胞術檢測到80%的tc1細胞表達綠色熒光蛋白(未顯示數據)。通過測定其干擾蛋白質表達的能力,我們評價了e6和e7shrna的效力。為此,我們首先通過逆轉錄pcr獲得了e6和e7的全長cdna(以及作為對照的gapdh)。結果顯示,在針對e7的shrna存在時,e7mrna降低,jiang的序列獲得了高水平的干擾,而e7-2序列觀察到了較低水平的降低,對照shrna沒有降低(圖3a)。在用e6shrna處理的細胞中檢測e6mrna獲得了類似的結果。當用e7shrna處理細胞時,觀察到了e6mrna的輕微降低。
由于e6在caski細胞中的表達水平太低,以至于不能如gu等(cancergenether2006;13:1023-27)和yamato等(cancergenether2008;15:140-53)所報道的那樣使用可獲得的抗體通過western印跡分析進行檢測,因此根據e6shrna恢復p53表達的能力對其活性進行了篩選。我們的結果表明,在表達e6-1shrna24小時后,western印跡所檢測的p53水平增加(圖3b),并隨時間而降低。在e7-1、e7-2和e6-2shrna存在下,p53表達的增加低于e6-1shrna中觀察到的增加。當用laczshrna處理細胞時,未檢出p53的表達。這些結果提示,通過shrna處理,e6蛋白水平降低,并且p53不僅積累,并且在功能上還是有活性的。
為了驗證e6和e7表達的抑制是否可誘導細胞活力的降低,培養5天后,在shrna轉染和未轉染的caski和tc1細胞中,使用3-(4,5-二甲基噻唑-2-基、)-2,5-二苯基四唑溴化物測試測量540nm的吸光度。我們的結果顯示,e6和e7沉默誘導細胞活力的降低(圖4)。該降低對e7shrna來說更大(70%細胞生長抑制)。當用相同的shrna轉染hpv陰性的子宮頸細胞(例如c33-a)時,未觀察到細胞生長的抑制,表明e6和e7shrna引起的細胞生長抑制是特異性的。對于e6-1和e6-2,以及對于e7-1和e7-2shrna而言,細胞生長的降低是相似的。
用e6和e7shrna假病毒顆粒轉導tc1細胞未誘導凋亡
基于凋亡細胞中dna對熱變性敏感度的增加來進行細胞凋亡測定,以研究細胞死亡是否是由于細胞凋亡所引起的。在該測定中,通過在甲酰胺存在下加熱使dna變性,并用ssdna特異性的單克隆抗體f7-26染色。與對照shrna轉染的細胞相比,流式細胞術未顯示e6-1、e6-2、e7-1和e7-2shrna轉染的tc1細胞的凋亡細胞數目的顯著增加。為了進一步評價凋亡的存在或不存在,在e6和e7shrna假病毒顆粒轉導的tc1細胞中進行了測量半胱天冬酶(caspase)3和7酶活性的半胱天冬酶測定。在使用e6和e7shrna時都沒有觀察到半胱天冬酶活性的增加。該結果提示,e6和e7shrna誘導tc1細胞生長的降低,但這不是通過凋亡性細胞死亡誘導的。
用e6和e7shrna假病毒顆粒體外轉染tc1細胞在小鼠中誘導腫瘤生長的降低
還使用tc1/小鼠模型體內研究了e6和e7shrna假病毒顆粒的效力。使用編碼e6-1和e7-1shrna的hpv假病毒顆粒、單獨的hpvvlp和編碼e7-1shrna的慢病毒體外轉導tc1細胞。24小時之后,皮下注射未轉染和轉染的tc1細胞進c57bl6小鼠中。
21天后,處死小鼠,切除腫瘤并稱重。在對照小鼠中(模擬組和單獨vlp組),腫瘤重量的范圍是1.09至2.12g(均值,1.64g)。對于用e7-1shrna和lipofectamine轉染的tc1細胞,未觀察到腫瘤重量的降低(均值,1.61g)。對于e6-1hpv假病毒顆粒,觀察到了平均腫瘤重量降低42%(p<0.10),對于e7-1慢病毒和e7-1hpv假病毒顆粒,平均大小分別降低70%至80%(p<0.05和p<0.001;圖5)。
在小鼠中用e7shrna假病毒顆粒瘤內轉導tc1細胞腫瘤誘導腫瘤生長摩低
還研究了編碼e7shrna的假病毒顆粒的體內效力,以確定其在帶有tc1細胞腫瘤的小鼠中降低腫瘤生長的能力。根據其體外效力,選擇e7-1shrna用于這些研究。將e7-1shrna假病毒顆粒直接注射進腫瘤中,每2天一次,共2周。1周之后,與對照小鼠相比,在e7-1shrna處理的小鼠中未觀察到腫瘤生長的降低(圖6a)。隨后,在處理的第二周,清楚地觀察到了腫瘤生長的降低,在第二周結束時,在用對照shrna處理的小鼠中平均腫瘤重量為1.05g,而在用e7-1shrna假病毒顆粒處理的小鼠中為0.49g(p=0.045)。
實施例2:在hpv31大殼粒蛋白上的中和構象表位的鑒定和功能意義
本研究的主要目的是表征hpv31假病毒顆粒中和的抗原結構與機制。其中一個問題是誘導hpv中和性抗體的精確表位位置,以及由于與病毒殼粒相互作用而對抗感染保護作用的貢獻。
現已公認,構象表位決定中和性抗體的產生(christensen等,virology1994;205:329-35;rose等,jgenvirol1994;75:2075-79;white等,jvirol1998;72:959-64;white等jvirol1999;73:4882-89;giroglou等jvirol2001;75:1565-70)。因為hpv的中和表位是構象依賴性的,所以其氨基酸組成和表面位置還未被完全表征。
這些研究可用于疫苗設計和病毒-細胞相互作用。此外,對hpv抗原結構的理解對于設計來源于hpv的、具有降低的免疫原性的基因治療載體而言是至關重要的。生成這樣載體的一個先決條件是對激發中和免疫應答的病毒決定簇的更多理解,以設計假病毒顆粒載體,所述載體在其負責產生中和性抗體的構象表位中具有缺失或突變。這些具有降低的免疫原性的突變載體允許再施用這些載體時,不會因為誘導了針對所述載體的中和性抗體而引起顯著的轉基因效力損失。
材料和方法
hpv31單克隆抗體
如前所述生產和表征本研究中使用的hpv31mab(fleury等,archvirol2006;151:1511-23;fleury等,clinvaccineimmunol2008;15:172-75)。h31.d24mab識別已在fg環(271-279位氨基酸)中鑒定的共有線性表位,而h31.f7mab識別已在fg環的n末端部分中鑒定的構象交叉中和表位(crossneutralizingepitope)(fleury等,archvirol2006;151∶1511-23)。13種其他mab識別特異性的構象中和表位。此外,使用camvir-1單克隆抗體(cv)作為對照,所述抗體識別de環上的共有線性表位(carpentier等,jmedvirol2005;77:558-65)。通過用硫酸銨(33%終濃度)鹽析,隨后用磷酸緩沖鹽(pbs,phosphate-bufferedsaline)透析,繼之以蛋白ag/瓊脂糖凝膠(pierce;免疫純igg純化試劑盒)親和層析,使用細菌細胞表面展示法(bacterialcellsurfacedisplaymethod)從未加工的腹水中純化所研究的mab。
假病毒的中和
如前確定每種單克隆抗體的中和能力(fleury等,archvirol2006;151:1511-23;fleury等,clinvaccineimmunol2008;15:172-5)。此外,我們研究了假病毒顆粒細胞表面結合之前或之后是否發生中和。用293ft細胞中產生的hpv31假病毒顆粒進行了測試,并且使用在完全dulbecco’s改良eagle’s培養基(invitrogen,補充有10%fcs、100iu/ml青霉素和100μg/ml鏈霉素的dmem)中培養的、接種于96孔板中的并且在37℃下孵育24小時的cos-7細胞進行中和測定。通過在37℃下將預先與mab一起孵育過的hpv31假病毒顆粒加入到細胞(100μl)中1小時來進行假病毒顆粒細胞表面結合之前的測量中和的測定。通過在37℃下將hpv31假病毒顆粒加入到cos-7細胞中1小時來進行假病毒顆粒細胞表面結合之后的測量中和的測定。清洗三次以除去未結合的假病毒顆粒后,將mab添加到100μldmem中。對于每個測定而言,在37℃下3小時后除去上清液,并添加200μl完全dmem。37℃下進一步孵育48小時之后,通過使用螢火蟲螢光素酶測定試劑盒(interchim,montlucon,france)測量轉染的細胞所表達的螢光素酶來對感染性進行評分,使用多掃描微板發光計(thermo-fisherscientific,courtaboeuf,france)對螢光素酶表達進行定量。如果螢光素酶活性降低>80%,則認為mab是中和性的。如果mab僅在病毒顆粒結合至細胞之前添加時中和假病毒,則對假病毒與細胞結合的抑制進行評分。如果抗體在其添加至cos-7細胞之前和之后中和假病毒顆粒,則認為mab通過細胞附著后機制(postcellattachmentmechanism)中和假病毒顆粒。
重組l1蛋白的生成和vlp的純化
使用bac-to-bac系統(invitrogen,fisher-scientific,illkirch,france),在草地夜蛾(spodopterafrugiperla)(st21)細胞中表達hpvl1蛋白。預先生成了編碼hpv16、hpv31、hpv16dc9和hpv16dc31(分別具有9或31個氨基酸c末端缺失)的l1基因的桿狀病毒(baculovirus)(touze等,femsmicrobiollett2000;189:121-7;touze等,jclinmicrobiol1998;36:2046-51)。用pcr從全長hpv31l1密碼子優化的基因65擴增hpv31dc9和hpv31dc31截短基因,分別使用正向引物(ggatcccaccatgagcctgtggagacccagc,seqidno:37)和反向引物(對dc9而言)(ggaagcttatgtggtggtgctggcgctgggggc,seqidno:38)以及對dc31而言(gcaagcttaggcctgcagcaggaactttctgccc.seoidno:39)。通過ta克隆將pcr產物克隆進pcrtopo2.1中。對陽性克隆進行測序以驗證不存在不需要的突變。隨后將hpvl1基因克隆進之前用bamhi和hindiii消化過的pfastbac1質粒中。根據制造商的建議,使用bac-to-bac系統(invitrogen)生成編碼不同l1缺失基因的重組桿狀病毒。將維持在補充有10%胎牛血清(fcs,invitrogen)的grace昆蟲培養基(invitrogen,cergypontoise,france)中的sf21細胞用各重組桿狀病毒感染,并在27℃下孵育。感染后3天,收獲細胞,并按照之前的描述純化vlp,29,40。簡而言之,將細胞重懸于含有nonidetp40(0.5%)、抑肽素a和亮肽素(leupeptin)(各自均為1μg/ml,sigmaaldrich,saintquentinfallavier,france)的pbs中,并使其在4℃下靜置30分鐘。隨后將核裂解液離心并將沉淀重懸于含有抑肽素a和亮肽素的冰冷pbs中,然后進行超聲處理。隨后,將樣品加載到cscl梯度上,并離心至平衡(22小時,27,000rpm,sw28轉子,4℃)。通過折光檢查法研究cscl梯度片段的密度,并通過10%十二烷基硫酸鈉-聚丙烯酰胺凝膠(sds-page)電泳和考馬斯亮藍染色(coomassiebluestaining)來研究l1蛋白的存在。合并陽性級分,在pbs中稀釋并在beckmansw28轉子(3小時,28,000rpm,4℃)中離心。離心之后,將vlp重懸于0.15mol/l的nacl中并用最大功率的60%,以一次5秒脈沖進行超聲處理。使用microbca試劑盒(pierce,ozyme,france)測定總蛋白含量。
在293ft細胞中產生hpv31l1hbc263/264突變體vlp。使用兩步pcr方案,通過密碼子優化的hpv31l1基因的誘突變來獲得編碼嵌合l1蛋白的dna。進行重疊pcr以在hpv31l1蛋白的263/264位獲得hbc蛋白的dpasre序列。在第一步中,使用優化的hpv31l1dna序列作為模板,并用5’l1-nhei
(ccgctagccaccatgagcctgtggagaccc.seqidno:40)與3’l1-dpasre(ctctctgctggcggggtcgttgaagaagtgccgcacgaa,seqidno:41)作為引物生成一個片段。使用優化的hpv31l1dna序列作為模板,并用3’l1-ecori(cggaattctatcacttcttggttttcttcc,seqidno:42)和5’l1-dpasre(gaccccgccagcagagagagaagcggcaccgtgggcgag,seqidno:43)作為引物擴增另一片段。在第二pcr步驟中,使用這兩個重疊的片段作為dna模板,使用5’l1-nhei和3’l1-ecori為引物。所產生的dna序列l1堿基263/264之間具有hbc78-83編碼序列,并在5’端具有nhei限制性位點并在3’端具有ecori限制性位點。對于蛋白表達而言,將hpv31l1hbc263/264基因克隆進pires哺乳動物表達載體(bdbiosciences,clontech)中。通過經典的堿裂解法和酚/氯仿抽提制備該dna質粒(hpv31l1hbc263/264-pires),并根據制造商的說明書使用fugene6(rochediagnostic,meylan,france),將該dna質粒用于轉染293ft細胞。用總共0.5μgdna和1μlfugene6/cm2培養面積轉染細胞。轉染后44小時收獲293ft細胞,并如前所述純化vlp。
通過電子顯微鏡研究了vlp中表達的不同hpv-l1蛋白的自組裝。為此目的,將vlp制備物應用于碳包網格(carbon-coatedgrid),用1.5%乙酸鈾酰(uranylacetate)負染,并使用jeol1010電子顯微鏡在×50,000的標稱放大倍數下觀察。所有的電子顯微鏡照片都是在30,000×或50,000×下拍攝的。
通過表面等離子共振研究hpv31mab的vlp結合競爭
用配備有cm3(羧甲基化葡聚糖)傳感器芯片的biacore1000(biacoreab,uppsala,sweden)進行分析。以5μl/分鐘的流速,用35μl的0.05mol/l1-乙基-3-(3-二甲基氨基丙基)-碳二亞胺鹽酸鹽和0.2mol/ln-羥基琥珀酰亞胺處理cm3傳感器芯片,然后以5μl/分鐘的流速,將hpv31l1vlp(32μg/ml,在35μlpbs緩沖液中)進行共價偶聯。隨后,以10μl/分鐘的流速,用50μl1mol/l乙醇胺-hcl(ph8.5)封閉殘余的羧基。通過以10μl/分鐘的流速注射5μlhcl-甘氨酸(10mmol/l,ph2.2)來消除未結合的vlp。所有在室溫下進行的相互作用分析均采用20μl/分鐘的流速。對于每個mab,通過三次注射30μl以pbs稀釋10倍的腹水來獲得結合的hpv31l1vlp的抗體飽和。通過注射30μl以pbs稀釋4倍的相同mab的雜交瘤上清液來驗證mab飽和。隨后,通過連續注射五次以pbs稀釋4倍的不同雜交瘤上清液(每次30μl)建立競爭。隨后,通過三次注射10μl的30mmol/lhcl來使生物傳感器再生,并對同樣的vlp偶聯的流動室進行另一個飽和-競爭循環。研究了幾種其他的再生緩沖液(包括2mol/lnacl、10mmol/lnaoh和20、25、30和50mmol/lhcl)。所選擇的緩沖液(30mmol/lhcl)顯示除去100%的結合抗體,但不從傳感器芯片上除去vlp,并且不影響vlp構象,因為針對構象表位的抗體仍然如再生處理之前一樣有效地與vlp結合。
利用細菌細胞表面展示進行表位做圖
使用pflitrx載體的細菌細胞表面展示法使用插入有硫氧還蛋白(thioredoxin)結構域(trxa)的12mer肽文庫來限制肽。該硫氧還蛋白結構域自身被插入到大細菌鞭毛蛋白(flic)中,以展示于大腸桿菌(e.coli)的表面(lu等,biotechnology(ny)1995;13:366-72;james等,science2003;299:1362-1367)。通過將1ml肽文庫儲備液接種進50ml含有100μg/ml氨芐西林的imc培養基(6g/lna2hpo4,3g/lkh2po4,0.5g/lnacl,1g/lnh4cl,0.2%酪蛋白氨基酸(casaminoacid),0.5%葡萄糖,1mmol/lmgcl2)中而獲得pflitrx隨機肽展示文庫(invitrogen,cergypontoise,france),并隨后在25℃下振蕩(225-250rpm)過夜。通過將100μg/ml色氨酸添加到來自過夜培養于50ml含有100μg/ml氨芐西林的imc培養基的1010細菌中來誘導肽表達,隨后在25℃下振蕩6小時。
對于針對抗hpv31抗體的文庫篩選而言,通過用定軌搖床以50rpm輕度搖動將1ml無菌水中的20μgmab包被到60mm板(nunclond,nunc,atgc,marne-la-valle′e,france)上1小時。用10ml無菌水清洗后,添加10ml封閉溶液(含有100μg/ml氨芐西林、1%低脂奶粉、150mmol/lnacl、1%a-甲基甘露糖苷的imc培養基)并在搖動下孵育1小時。傾出封閉溶液后,將10ml細菌細胞培養物與0.1g奶粉、300μl5moi/lnacl、500μl20%a-甲基甘露糖苷(終濃度:1%脫脂奶粉、150mmol/lnacl、1%a-甲基甘露糖苷)一起加入。在以50rpm輕度搖動1分鐘并在室溫下孵育1小時后,用10ml含有100μg/ml氨芐西林和1%a甲基甘露糖苷的imc培養基將所述板清洗五次(50rpm,5分鐘)。隨后,通過震蕩所述板30秒將結合的細菌細胞洗脫進殘余體積的清洗溶液中。將其轉移至50ml培養瓶中,并在25℃和搖動(225-250rpm)下培養過夜。將該淘洗循環(panningcycle)再重復4次,并將來自第五次淘洗的過夜培養物在含有100μg/ml氨芐西林的rmg板(6g/lna2hpo4、3g/lkh2po4、0.5g/lnacl、1g/lnh4cl、2%酪蛋白氨基酸、0.5%葡萄糖、1mmol/lmgcl2、1.5%瓊脂)上劃線,并在30℃下孵育過夜。將來自rmg/氨芐西林板上的24至30個克隆中的每一個接種進2ml含有100μg/ml氨芐西林的rm培養基(6g/lna2hpo4、3g/lkh2po4、0,5g/lnacl、1g/lnh4cl、2%酪蛋白氨基酸、1%甘油、1mmol/lmgcl2)中。30℃下搖動孵育過夜后,通過經典的堿裂解酚/氯仿dna小量制備法提取dna。使用flitrx正向測序引物對核苷酸序列進行分析。在abiprism3100avantdna測序儀(perkinelmer,courtaboeuf,france)上運行序列。使用dialign2(morgenstern等,gioinformatics1999;15∶211-18)分析序列。
通過elisa檢測mab對野生型和突變vlp的反應性
用vlp包被微板孔(maxisorp,nunc)。在4℃下孵育過夜并用pbs-吐溫20(0.1%)清洗兩次后,在37℃下將各孔用補充有1%fcs的pbs飽和1小時。在37℃下,用在pbs5×-吐溫(1%)-fcs(10%)中稀釋的mab將各孔一式兩份地孵育(兩個測試和一個對照)。清洗4次后,將以pbs-吐溫(1%)-fcs(10%)稀釋1000倍的過氧化物酶綴合的山羊抗小鼠igfc(sigmaaldrich)添加至孔中并在37℃下孵育1小時。隨后,清洗4次后,添加在25mmol/l檸檬酸鈉和50mmol/lna2hpo4中的0.4mg/ml鄰苯二胺和0.03%過氧化氫。30分鐘后,用h2so4(4n)終止反應,并在490nm讀取吸光度。為進行數據分析,從受試樣品的od值中減去在無一抗時獲得的光密度(od)值。顯示的數據是三至四次測定的平均值。
基于肝素和ecm的酶聯免疫吸附測定
使用源自giroglou等(jvirol2001;75:1565-70)描述的用于hpv33vlp的肝素結合測定的測定方法測試了vlp與肝素間的相互作用。在4℃下,用每孔200ng肝素-bsa(sigma)或matrigelvr(bdbiosciences,lepontdeclaix,france)涂布位微滴定板(maxisorp,nunc)過夜。在用含有0.1%吐溫20的pbs清洗4次后,通過在37℃下用pbs加1%fcs孵育1小時封閉非特異性結合位點。清洗后,添加200ng/孔的在pbs中稀釋的vlp。在37℃下孵育60分鐘并清洗4次之后,添加在pbs、0.1%吐溫20和10%fcs中按1∶1000稀釋的抗hpv31vlpmab并在37℃下孵育60分鐘。在37℃下孵育1小時并清洗4次后,使用共價連接辣根過氧化物酶的小鼠抗igg抗體檢測結合的抗體。在37℃下孵育1小時并清洗4次后,添加100μl含有鄰苯二胺和h2o2的底物溶液。30分鐘后,通過添加100μl2mol/lh2so4終止反應,并用自動板檢測儀讀取492nm下的吸光度。從測試孔的值中減去沒有vlp的對照孔的吸光度。同時,用肝素-bsa或matrigelvr涂布第二板。孵育并清洗后,添加200ng/孔的vlp(其在37℃下與在pbs、0.1%吐溫20和10%fcs中稀釋1000倍的mab預孵育1小時)。如前所述,使用共價連接辣根過氧化物酶的小鼠抗igg抗體檢測結合抗體。按照所觀察到的在vlp與肝素相互作用之前和之后添加mab之間od的降低來計算vlp與肝素或matrigel結合的抑制。結果表示為od降低的百分比。
vlp與hs和ecm結合的測定
如前所述,用肝素-bsa包被微滴定板(maxisorp,nunc)。封閉步驟后,添加用pbs稀釋的vlp。在37℃下孵育60分鐘并清洗之后,添加在pbs、0.1%吐溫20和10%fcs中按1∶5000稀釋的canvir1mab,并在37℃下孵育60分鐘。清洗四次之后,使用共價連接辣根過氧化物酶的小鼠抗igg抗體檢測結合抗體,并隨后如前所述進行肝素與mab相互作用的檢測。結果表示為od值。
通過hpv31l1蛋白的同源性建模(homologymodeling)使hpv31表位可視化
將hpv31l1蛋白的序列(genbankid,p17388)作為輸入值提交給swiss-model建模工具(swissmodel.expasy.org)。基于序列相似性的模板檢索鑒定了hpv16l1(pdb編碼1dzl和2r5h)、hpv-35l1(2r5j),hpv-11l1(2r5k)和hpv-18l1(2r5i)作為可能的3d模板。因為hpv31l1與hpv16和hpv35l1序列更相似,所以我們選擇了相應的3d模板(1dzl、2r5h和2r5j)來模擬hpv31的l1結構。使用anaolea(swissmodel.expasy.org/anolea/)評價了hpv31l1的模型,發現其正確地用于進一步的表位位置結構分析。使用swisspdbviewer,利用hpv31l1模型和hpv16vlp(1dzl)的非晶體學對稱性(變換矩陣)(chen等,molcell2000;5:557-67),重新構建了hpv31的l1五聚體。以pdb格式存儲了hpv31l1vlp五聚體的原子坐標并用pymol程序顯示,所述pymol程序是一種用于大分子結構的分子圖形可視化工具(pymol.org)。
結果
使用表面等離子體共振對hpv31l1mab進行表位做圖
使用針對hpv31l1蛋白的15種mab進行表位做圖。測試這些mab之間的所有競爭。例如[圖7(a)],通過用h31.f16mab(未加工的腹水)使偶聯的hpv31l1vlp飽和來建立表位競爭,并通過注射相同mab(雜交瘤上清液)來驗證mab飽和。發生在添加h31.f16mab之后的低共振單位(low-resonanceunit,ru)(-52ru)證明達到了飽和。飽和之后,由于飽和mab的解離導致ru降低,并且這是負ru的原因。隨后,通過連續注射h31.b18、h31.d7、h31.e16、h31.e17和h31.f7mab(雜交瘤上清液)來建立mab結合競爭。h31.e16和h31.f7mab不結合hpv31l1vlp(分別為-1和-13ru),提示這兩個mab所識別的表位與h31.f16mab所識別的表位是相似的或非常接近的。與此相反,使用h31.b18、h31.d7和h31.e17mab觀察到了顯著的vlp結合(分別為171、523和69ru),提示這些抗體所識別的表位與h31.f16mab所識別的不同。隨后,通過三次注射30mmol/lhcl使生物傳感器再生。該方法用于所有其他競爭性測定。
所研究的15種mab中的每一種都與至少3種其他mab競爭,但沒有一種mab與所有其他mab競爭。使用這些結果建立了表位圖[圖7(b)],h31.f7mab所識別的表位在該圖中為中心位置。該mab所識別的表位已在l1fg環上鑒定(carpentier等,jmedvirol2005;77:558-65;fleury等,archvirol2006;1511-23)。與其他mab(h31.b18、h31.b1和h31.h9)競爭較小的mab位于所述表位圖的外圍。
hpv31mab與hpv31/hbcvlp的結合
使用hpv31l1/hbc263/264突變體和hpv31l1wtvlp分析了mab的反應性,以鑒定一些中和表位是否位于fg環上。除了以前產生的hpv31l1vlp以外,我們還通過在位置263-264插入乙型肝炎核心(hbc)dpasre而構建了hpv31l1突變體。所有類型特異性mab的vlp結合都受到在263/264位插入hbc的影響。應當指出,非中和性h31.d24mab(其識別位于271-279位的線性表位(svptdlyik,seqidno:44))的反應性不受所述插入的影響。camvir-1mab(其識別在fg環以外鑒定的線性表位)的結合也不受所引入的突變的影響。交叉中和性mabh31.f7類似地與hpv16和hpv31wtvlp均有反應,但受到在位置263/264插入hbc的影響。
利用細菌表面展示對5種mab進行表位做圖
利用細菌展示肽文庫進行表位做圖提供了進行單克隆和多克隆抗體表位做圖的新方法(rockberg等,natmethods2008;5:1039-45)。使用一種此類系統(pflitrx細菌展示系統)鑒定l1表位。使用pflitrx載體的細菌細胞表面展示利用插入到硫氧還蛋白結構域中的12mer肽文庫來限制所述肽,允許構象表位的展示。該硫氧還蛋白結構域自身插入到大腸桿菌的大細菌鞭毛蛋白中,以展示在細菌表面。將從腹水中純化的高效價mab包被到nuclond板上,用于抗hpv31抗體的文庫篩選,并且對結合到板上的mab進行體外篩選輪次,以選擇與所述mab相互作用的細菌展示肽。對于每個輪次,將細菌文庫添加至細胞培養皿中進行陽性選擇。洗掉未結合的細菌,并回收結合的細菌。五個輪次之后,選出單克隆并分離dna用于測序。首先使用dialign2程序分析序列。選出高評分的匹配的肽,隨后使用dialign2與全長hpv31l1蛋白序列進行比對。將與選出的所有肽相匹配的hpv31l1序列保留。我們首先將該系統用于h31.d24mab,其識別以前鑒定的hpv31l1的fg環中271-279位的線性表位(svptdlyik,seqidno:44)。在進行細菌展示選擇后,將24個陽性克隆進行測序和分析。用h31.d24mab選出的24個肽中的六個彼此f2匹配,并與hpv31l1蛋白匹配(參見圖8),所鑒定的共有序列位于275-279位(dliyk,seqidno:46)。
因而,使用細菌展示來研究mabh31.f7所識別的中和構象表位,mabh31.f7與hpv16、18和58具有交叉反應活性,并弱中和hpv類型16和31。使用h31.f7mab通過細菌展示選出了24個陽性克隆。所選出的24個肽中5個彼此匹配,并與hpv31l1蛋白序列259-266位(rhffnrsg,seqidno:47)相匹配。還研究了三種類型特異性的識別構象表位的中和性mab(h31.f16、h31.h12和h31.b1)。選出每種mab的陽性克隆。用h31.f16mab選出的五種肽、用h31.h12mab選出的五種肽以及用h31.b1mab選出的六種肽彼此匹配,并且與用于h31.f16mab的hpv31l1蛋白序列sgtvgesvp(265-273位)(seqidno:48)、用于h31.h12mab的rsgtvg序列(264-269位)(seqidno:49)和用于h31.b1mab的rsgtvgesv序列(264-272位)(seqidno:50)相匹配。
假病毒顆粒附著前和附著后的mab中和
hpv16和hpv33特異性抗體已顯示出在附著至靶細胞之前或之后進行中和(selinka等,jvirol2003;77:12961-67;day等,jvirol2007;81:8784-92)。通過抗hpv31mab的病毒中和機制是通過中和測定確定的,其中在添加f3假病毒顆粒至cos-7細胞之前[圖9(a)]或細胞附著后1小時[圖9(b)]添加mab。六種mab[h31.b1、h31.c24、h31.g5、h31.e16、h31.f7和h31.d7,圖9(b)]通過抑制細胞附著中和了hpv31假病毒,因為其在病毒附著之前中和,而不是在假病毒與細胞結合之后[圖9(b)]。其他8種mab通過細胞附著后機制中和了hpv31假病毒,因為其在細胞附著之前和之后中和假病毒。應當指出,通過表面等離子體共振分析獲得的表位圖[圖7(c)]提示,這六種mab中的5種通過抑制細胞附著中和hpv31假病毒。
vlp與hs和ecm的結合:hpv31mab和l1c末端缺失的作用
使用elisa研究了hpv31mab對vlp與肝素之結合的抑制作用,其中在vlp與elisa板上包被的肝素結合之前向vlp添加mab。結果表明,識別線性表位的非中和性h31.d24mab強烈抑制vlp與肝素的結合,因為14種mab中僅6種識別f4構象中和表位[圖10(a)]。通過表面等離子體共振分析獲得的表位圖表明,mab中的一些抑制vlp與肝素結合[圖7(c)]。在附著至細胞之前中和假病毒顆粒的mab與抑制與hs之結合的mab之間沒有明顯的相關性。然而,三種中和性抗體(h31.g5、h31.e16和h31.d7)表現出了這兩種能力(參見圖10)。使用matrigelvr作為ecm的替代物,通過elisa研究了對vlp與ecm蛋白之結合的抑制作用。結果[圖10(b)]顯示,除了h31.c24(37%抑制)之外,全部的中和性抗體均抑制vlp與ecm蛋白的結合(>50%)。非中和性抗體h31.d24不抑制vip與ecm蛋白的結合。
為進一步研究vlp與hpsg的相互作用,我們使用了4種c末端缺失的突變體用于分析肝素與l1蛋白的結合。已生產了分別具有c末端9個和31個氨基酸缺失的hpv16d9和hpv16d31突變體,類似地生產了44和hpv31d9和hpv31d31l1突變體用于本研究的目的。如前邊在相應的hpv16缺失突變體44中觀察到的那樣,這些hpv31缺失突變體自組裝成為vlp(參見圖7),并且這4種c末端缺失的vlp以與wtvlp相似的結合方式與肝素結合。然而,當這些vlp變性時,失去與肝素的結合,確證了肝素與vlp構象基序結合,而該基序不存在于l1蛋白的c末端部分(參見圖11)。因為hpv感染靶細胞是多步驟的過程,涉及hspg、ecm和未知的二級受體,所以我們研究了hpv31mab對ecmhpvvlp結合之中和的作用。
h31.d24識別的表位是線性表位,三種中和性mab(h31.b1、h31.f16和h31.h12)識別的表位是構象表位,而h31.b1mab是部分交叉中和性的和交叉反應性的。
h31.f7mab識別的表位(即交叉反應性的和部分交叉中和性的mab)是在hpv31l1蛋白fg環的n末端部分的259-268位鑒定的(rhffnrsgtv,seqidno:45)[圖12,利用swisspdbviewer,使用hpv31l1模型和hpv16vlp的aq6非結晶對稱信息,重新構建了3d殼體結構[pdb編碼:1dzl,(chen等,molcell2000;5:557-67)]],且根據hpv31模型,其大多數是來自所述殼體表面的不可接近的f6。這與fg環的早期區域證明的hpv類型之間的相同結構的事實和bishop等的基于l1蛋白結構的假說是一致的。該假說提出,fg環的該區域必須能夠在類型之間誘導交叉反應性,但是抗原性較差和/或是不可接近的。
對于hpv16和hpv33來說,已表明多種l1蛋白表面暴露的環對于表位的中和性抗體的誘導有貢獻,所述表位僅在一個環中被鑒定,或者幾個環對結合位點15、46、47有貢獻,有人提出l1的非連續區域可對mab識別的中和表位有貢獻。我們的結果支持hpv31中和性抗體主要針對fg環,而fg環僅對與中和性抗體的結合有貢獻。l1高變環彼此緊密臨近的事實并沒有排除其他環中的突變或插入影響fg構象表位的的可能性,如roth等47所觀察到的那樣。我們觀察到識別dlyik(seqidno:44)序列(275-279)的交叉反應性的h31.d24mab顯著降低hpv31與肝素結合的能力,因此證實了賴氨酸278在hs結合中的作用。然而,該抗體對hpv31假病毒顆粒41、65和識別構象表位(所述表位已知與位于fg環n末端部分的序列相結合)的三種其他中和性抗體與肝素的結合沒有作用或作用有限。h16.v5和h16.e70mab已表明不阻斷與細胞表面的相作用。然而,這些中和性抗體抑制病毒與hacat細胞產生的ecm相結合,并通過細胞附著后機制中和假病毒顆粒43。與此相一致的是,我們觀察到三種類型特異性的中和性抗體不與hs競爭與vlp的結合,并且其中僅一種(h31.b1)被vlp與細胞的結合所抑制。然而,與非中和性的h31.d24mab不同,所有這些抗體均競爭與ecm的結合。這些結果提示,這些抗體識別hpv16vlp與hs35結合中所涉及的賴氨酸的構象堿性簇的鄰近表位。應當指出,該簇最重要的賴氨酸存在于h31.d24mab所識別的表位中。此外,對于mab對hpv31假病毒顆粒的附著前和附著后中和的研究表明,hpv31中和性抗體中的6種通過阻止病毒顆粒與細胞表面結合而發揮作用,另外8種中和性mab通過阻止其內化而干擾假病毒顆粒。我們的結果表明,對于整體的mab而言,中和與mab結合hs之能力之間沒有相關性。lopez等66最近報道,在天然感染中檢測到的抗hpv抗體抑制hpv16與hs的結合,并且其觀察到具有最高中和效價的那些抗體是那些抑制hs結合的抗體。總之,我們的結果證明hpv31中和性mab識別位于hpv31l1蛋白fg環上的構象表位,并且其通過阻斷與靶細胞的附著,或通過細胞附著后的中和來發揮作用。通過細菌表面展示對三種類型特異性中和表位的精確確定證明了其在fg環中央部分的定位,并鑒定了在相對保守的fg環n末端部分的交叉反應性和部分交叉中和性的構象表位。fg環的溶劑暴露的氨基酸殘基分布在沿著由pro273至leu287所界定的軸而形成的溝的兩側[圖12]。我們的結果表明,所述溝的右側部分含有被h31.d24mab所識別的線性非中和性表位。這也是硫酸肝素結合的熱點,因而解釋了為什么h31.d24和hs競爭對該區域的結合。所鑒定的構象中和性表位均位于fg環溝的左側(參見圖12)。如以前對于針對bpvl1蛋白的mab所描述的那樣,可通過mab結合模式上的差異來解釋針對這些表位的抗體不與hs強烈競爭這一事實67。然而,一些其他hpv31中和性mab確實與hs競爭結合,這提示當其與其各自的表位結合時,這些mab具有不同的傾斜(tilt),因而干擾hs更大或更小程度的結合,或是其針對來自溝兩側的氨基酸殘基。h31.d24mab與vlp的尖端結合,這支持了這樣的假說,即非中和表位還存在于hpv顆粒的表面上。所獲得的結果表明,hpv31的fg高變環中中和性表位密集,提示hpv31mab與fg環中央部分上的重疊但不同的表位結合,這與hpvvlp表面上的fg環的暴露相一致,因而證實了中和性抗體主要位于殼粒的尖端和冠。該結果還支持并證實了阻斷病毒與ecm的附著(而不是阻斷病毒與hs的附著)是重要的中和機制。
實施例3:hpv16/31l1突變體的生成
乳頭瘤病毒是小的無包膜dna病毒,其二十面體衣殼由l1和l2蛋白構成,所述衣殼包封約8kbp的閉合環狀雙鏈dna。直徑50-60nm的病毒衣殼含有72個l1大蛋白的五聚體和12至72拷貝的l2小衣殼蛋白。用自組裝成病毒樣顆粒(vlp)的l1蛋白進行了免疫接種誘導產生高水平的中和性抗體,并賦予類型特異性的長期保護,如在動物模型中證明的那樣(breitburd等,jvirol1995;69:3959-63;suzich等,pnas1995;92:11553-57;christensen等,jvirol1996;70:960-65)。抗體應答通常是針對vlp外表面上存在的病毒衣殼l1蛋白的外環上發現的表位而產生的(christensen等,virology2001;291:324-34;sadeyen等,virology2003;309:32-40;orozco等,jvirol2005;79:9503-14;yaegashi等,jvirol1991;65:1578-83)。中和性衣殼表位是抗體介導的針對hpv的免疫保護作用的重要決定簇,并且線性和構象表位均被鑒定位于hpvl1vlp和假病毒顆粒的表面上(yaegashi等,jvirol1991;65:1578-83;volpers等,jgenvirol1995;76:2661-67;heino等,jgenvirol1995;76:1141-53;christensen等,virology1996;224:477-86)。
據報道hpv16l1的fg環和hpv31l1的ef環中的l1殘基涉及中和性抗體的結合(sadeyen等,virology2003;309:32-40;white等,jvirol1999;73:4882-89;combita等,jvirol2002;76:6480-86;carter等,jvirol2003;77:11625-32)。
本研究的目標是研究嵌合hpv顆粒的免疫原性。我們將含有hpv16主要表位(aa256-294)的l1衣殼蛋白fg外環的氨基酸替換為hpv31(aa257-295)的l1fg環的對應氨基酸,生成嵌合l1hpv納米顆粒,所述納米顆粒維持hpv16l1的整體野生型序列,僅在fg環中有3個hpv31樣替換(hpv-vlpx)或7個hpv31樣替換(hpv-vlpy)(圖13)。
從感染了重組桿狀病毒的sf21昆蟲細胞中產生和純化所述嵌合l1蛋白。sf21昆蟲細胞產生大量的嵌合l1蛋白(2.5-3mg/升)。l1hpvx和l1hpvy嵌合蛋白與hpv16野生型l1類似地組裝成為vlp。含有除了hpv-vlpy中的7個交換之外的突變的嵌合構建體不組裝成為vlp。
為了測試嵌合vlp的感染性,測定了其將遺傳物質轉移進細胞的能力。將hpv-vlpx和hpv-vlpy以及作為對照的hpv16野生型vlp解離,添加螢光素酶報告質粒,并在重新結合時包封到vlp中。將cos-7細胞(非洲綠猴腎細胞,atcccrl-1651)與vlp體外接觸并孵育。孵育后,除去培養基,在螢光素酶裂解緩沖液中清洗并裂解細胞。如圖14所示,嵌合的hpv-vlpx和y保留了野生型hpv-16vlp的感染能力。
為檢測嵌合vlp的免疫原性,用hpv16、hpv31和兩種嵌合hpvx和y免疫小鼠(每組10只)。如圖15所示,hpv-vlp嵌合體的免疫反應性與hpv16和hpv31之間的交叉反應性是同一數量級的,其是最小的(至少比實際免疫應答低2個對數)。在用hpv16免疫接種的小鼠中,用elisa測量的hpv16特異性抗體的效價可預期地為約2000gmt。出乎意料的是,在hpv-vlpx和y感染的小鼠中基本上沒有發現hpv16特異性抗體,盡管l1hpv-vlpx和y幾乎完全維持hpv16野生型氨基酸序列這一事實。因此,這些嵌合體不產生hpv16特異性抗體。如所預期的,在hpv31感染的小鼠中,基本上沒有發現hpv-16特異性抗體。甚至更出乎意料的結果是,在hpv-vlpx和y感染的小鼠中基本上沒有發現hpv31特異性抗體,盡管嵌合體的fg環類似于hpv31的這一事實,尤其是對于l1hpvy的fg環(其與野生型hpv31的fg環的不同僅在于一個氨基酸(hpv31291t-n290hpv16))來說。如所預期的,在hpv16感染的小鼠中基本上沒有發現hpv31特異性抗體,而在hpv31中則發現可靠的應答(約1900gmt)。有趣的是,在hpv16或hpv31免疫的小鼠中也未檢測到x和y特異性抗體,提示基本上沒有交叉反應性。對于x和y,在x或y免疫的小鼠中,可檢測到中等的交叉反應性(對于x和y而言,分別為538和857gmt)。
數據表明,可以設計帶有突變的假病毒載體,其在所述假病毒載體來源的物種之間基本沒有交叉反應。這一大大降低的免疫原性將允許重新施用這些載體,而不會因為在hpv感染的個體中誘導針對所述載體的中和性抗體而明顯損失轉基因效力。
實施例4:通過用包封了l2基因的hpv假病毒顆粒進行免疫來誘導針對異hpv的中和性抗體
用自組裝成病毒樣顆粒(vlp)的l1進行的免疫誘導了高效價的中和性抗體,并賦予動物針對同源的實驗性感染的保護作用[breitburd等,jvirol1995;69(6):3959-63;suzich等,pnas1995;92(25):11553-7]。還已經表明,保護作用是由針對構象表位的中和性抗體介導的。這些結果已經導致了針對生殖器hpv類型的疫苗的產業開發。臨床前研究已表明,l1vlp所誘導的中和性抗體主要是類型特異性的[roden等,jvirol1994;68(11):7570-4;roden等,jvirol1996;70(9):5875-83]。然而,已報道了hpv6和11以及hpv16和31之間低水平的交叉中和[christensen等,virology1994;205(1):329-35;white等,jvirol1998;72(2):959-64;giroglou等,vaccine2001;19(13-14):1783-93;combita等,jvirol2002;76(13):6480-6]以及hpv18和45之間較高水平的交叉中和[mclaughlin-drubin等,virology2003;312(1):1-7]。臨床試驗已表明,免疫應答與針對hpv16和hpv18的感染以及相關的病變相關[ault等,lancet2007;369(9876):1861-8;paavonen等,lancet2007;369(9580):2161-70]。當前含有l1vlp的hpv疫苗促進強烈的、主要是類型特異性的中和性抗體應答。用hpv16和18疫苗的臨床試驗也已揭示了針對hpv類型的交叉保護作用限于密切相關的類型。對兩種疫苗明顯建立了針對hpv31的保護作用,僅對一種疫苗建立了針對hpv45的保護作用[paavonen等,lancet2007;369(9580):2161-70;brown等,jinfectdis2009;199(7):926-35]。因為批準的hpv疫苗僅靶向15種高風險hpv類型中的兩種,所以需要另外的策略來阻止其他高風險hpv類型的感染。
l2蛋白已作為候選的預防性疫苗出現,因為在乳頭瘤病毒感染的動物模型中用l2免疫接種誘導能夠介導比l1vlp更寬范圍保護作用的交叉中和性抗體[roden等,jvirol1994;68(11):7570-4;christensen等,virology1991;181(2):572-9;yin等,virology1992;187(2):612-9;chandrachud等,virology1995;211(1):204-8;gaukroger等,jgenvirol1996;77(7):1577-83;campo等,virology1997;234(2):261-6;roden等,virology2000;270(2):254-7;embers等,jvirol2002;76(19):9798-805],并且臨床前和臨床發現[gambhira等,cancerres2006;66(23):11120-4;alphs等,pnas2008;105(15):5850-5;karanam等,vaccine2009;27(7):1040-9]已經證明l2疫苗誘導廣譜交叉中和性抗體。然而,l2蛋白和l2肽的免疫原性低于lvlp,并且將l2蛋白整合進l1vlp中由于l1的免疫顯性而不提高抗l2應答[roden等,virology2000;270(2):254-7]。這提示,如果這樣的基于l2的疫苗是有效的,那么必須研究新的疫苗策略。
本研究的目的是研究提高l2蛋白與免疫系統的接觸以產生廣譜hpv疫苗的可能性。
材料和方法
抗體
camvir-1單克隆抗體(bdbiosciences,lepontdeclaix,france)與已定位于hpv-16l1蛋白的203至209位氨基酸之間的線性表位相結合[fleury等,archvirol2006;151(8):1511-23]。h16.v5mab針對hpv16l1蛋白的構象中和表位[christensen等,virology1996;223(1):174-84]。兔抗hpv16l2免疫血清由richardroden惠贈。使用streptagii抗體(hrp綴合的)檢測hpvvlp上steptagii肽的存在(novagen,vwr,fontenaysousbois,france)。
細胞系
cos-7細胞(非洲綠猴腎細胞,atcccrl-1651)生長于補充有10%熱滅活的胎牛血清(fcs)、100iu/ml青霉素和100μg/ml鏈霉素以及1mmol/l丙酮酸鈉的dulbecco改良eagle培養基(invitrogen,illkirch,france)中。293ft細胞系(invitrogen)是穩定表達sv40標簽和來自pcmvport6at.neo質粒的新霉素抗性基因的293細胞系的快速生長變體。293ft細胞系生長于dulbecco改良eagle培養基中,所述培養基除了補充有上述成分外,還補充有1%非必需氨基酸和500μg/mlg418。細胞系生長在37℃下的含有5%co2的加濕氣氛中。
在昆蟲細胞中生產hpv18、hpv31和hpv58vlp
按照以前的描述[touze等,jclinmicrobiol.1998;36(7):2046-51;combita等,femsmicrobiollett2001;204(1):183-8],從感染了重組桿狀病毒的sf21昆蟲細胞中生產和純化hpv58l1/l2vlp、hpv31l1/l2vlp和hpv18l1/l2vlp,所述桿狀病毒編碼l1和l2基因。
l2streptactin融合蛋白(l2sa)的生產和純化
包含上游(bamhi和sali)和下游(hindiii)限制性位點的不含起始密碼子的streptactin(sa)序列[voss等,proteineng1997;10(8):975-82]是由geneart(regensburg,germany)使用用于在草地夜蛾中表達的經調整密碼子使用而合成的。將sa序列克隆到pfastbacdual表達載體(invitrogen)的sali和hindiii位點之間,以獲得pfastbacdualsa質粒。隨后將hpv16l2orf融合在saofr的5’末端。為此,使用hpv16l2f和hpv16l2δr,通過pcr從含有野生型l2基因(fn297862)的人密碼子改編形式的質粒中擴增hpv16l2δnlsorf(氨基酸12至442)。設計正向引物以引入bamhi位點和起始密碼子上游的kozak序列,以及含有sali限制性位點的反向引物。隨后,通過ta克隆將pcr產物克隆進pcr2.1載體(invitrogen)。隨后,通過測序來驗證不存在不想要的pcr誘導的突變。將pcr2.1-16l2anls和pfastbacdualsa質粒用bamhi和saii限制性酶切,并將l2基因與streptactin基因融合,以生成pfastbacdual-16l2δnls(l2sa)。
根據制造商的推薦,使用bac-to-bac系統(invitrogen)生成了編碼l2sa的重組桿狀病毒。在27℃下,使sf21昆蟲細胞生長于補充有青霉素、鏈霉素和兩性霉素b(invitrogen)的sf900ii培養基中。以m.o.i.10感染細胞并使之生長4天。刮下細胞,以300×g離心并隨后重懸于含有0.5%nonidetp40和抗蛋白酶混合物(roche,meylan,france)的pbs1×中,并在冰上孵育30分鐘。將裂解液在4℃以12,000×g離心10分鐘,上清液代表細胞質級分。將代表核部分的沉淀進行超聲處理(3次脈沖,15秒,vibracell,fischerscientific,france)。通過western印跡分析l2sa蛋白的表達。為此,將蛋白質通過12.5%sdspage分離并轉移至硝酸纖維素膜(protranba83,schleicherandschuell,manteslaville,france)。在4℃下,將該膜在含有5%低脂奶粉的tnt(15mmol/ltris,140mmol/lnacl,0.05%吐溫20)中飽和過夜,并隨后用tnt-5%奶清洗3次。室溫下將膜與在tnt-5%奶中按1/1000稀釋的兔多克隆抗l2抗體一起孵育1小時,隨后清洗三次并添加堿性磷酸酶綴合的山羊抗小鼠iggfc(sigmaaldrich)(1/2,500,在tnt-5%奶中)。在室溫下孵育1小時并在tnt-5%奶中清洗三次以及在tnt中清洗兩次后,使用bcip/nbt液體底物系統(sigma-aldrich,saintquentinfallavier,france)使免疫斑點顯色。根據制造商的說明書(pierce,ozyme,montignylebretonneux,france),將l2sa蛋白在固定的亞氨生物素上通過親和進行純化。
l1l2savlp的生產
按照以前的描述[sadeyen等,virology2003;309(1):32-40],在使用允許在野生型hpv16衣殼基因140-141位插入steptagii肽(stii,wshpqfek,seqidno:12)[schmidt等,natprotoc2007;2(6):1528-35]的引物的兩個pcr步驟后,構建l116-steptagii基因。在第一個pcr步驟中,使用表現人化密碼子使用的l1基因作為模板,并使用正向l116stii/反向stii和正向stii/反向l116stii。第二個pcr步驟中,使用正向l116stii/反向l116stii引物,以將如此獲得的兩個重疊片段融合,以便產生l116streptagii序列(l1stii)。如上文所述將最終的pcr產物克隆和測序,并最終克隆到pfastbacdual質粒的bamhi和hindiii之間,以產生重組的桿狀病毒。
通過cscl梯度超離心從感染的昆蟲細胞中純化vlp。通過在相互作用緩沖液(100mmol/ltrishclph8,1mnacl,0.25%tritonx100)中將l1stiivlp與l2sa融合蛋白混合而獲得與l1stiivlp結合的l2sa蛋白。為了分析所獲得的嵌合vlp(l1l2savlp),在sw-60轉子(beckman)中通過超離心(60,000rpm,1小時)使vlp沉淀,隨后通過上文中的western印跡法分析l2和strep-tag的存在。
生產具有插入到de環中的hpv31l2肽(13-88位)的hpv31vlp
選擇hpv31l2蛋白的交叉中和表位(13-88位氨基酸)用于插入l1蛋白中[pastrana等,virology2005;337(2):365-72;gambhira等,jvirol2007;81(21):11585-92;richards等,pnasusa2006;103(5):1522-7]。通過兩個pcr步驟[fleury,clinvaccineimmunol2008;15(1):172-5]構建在140-141位含有限制性位點xhoi和smai的hpv31l1基因序列,以使用pires31l1l2h插入hpv31l2肽序列13-88位(l213-88)中。在第一個pcr步驟中,使用正向-l1h31/反向-l1和反向-l1h31/正向-l1為引物,擴增hpvl131的5’和3’部分。在第二個pcr步驟中,將這兩個片段用作模板,使用正向-l1h31/反向l1h31作為引物。隨后將該pcr產物克隆進pcrtopo2.1中,測序并亞克隆進之前用bamhi和hindiii酶切的pfastbac1質粒中。從pires31l1l2h和l213-88正向和反向引物擴增編碼13-88位hpv31l2基因片段的dna,并按上文克隆。用xhoi/smai消化pcr2.1topo/l213-88和pfastbac1/l1,以插入編碼hpvl2肽的序列。生成編碼l1-l213-88蛋白的重組桿狀病毒,并按上文所述3感染昆蟲細胞。
表5.使用的寡核苷酸序列
hpv58和hpv31假病毒顆粒的生成
使用密碼子改變的hpv衣殼基因的細胞系統獲得了hpv31和58假病毒顆粒[bucki等,methodsmolmed2005;119:445-62]。簡而言之,設計hpv58l1和l2基因,使其含有在人類中高度表達的基因中最頻繁使用的密碼子(分別為fn178626和fn178627)。將l1和l2基因克隆進哺乳動物雙順反子表達載體pires(bdbiosciences,clontech)中。將l1基因克隆到cmvie啟動子下游的mcsa的nhei和ecori限制性位點之間。隨后將l2基因克隆至pires-l1的mcsb的xbai和noti限制性位點之間。通過經典的酚/氯仿dna制備法制備了用于生成假病毒顆粒的編碼螢光素酶的dna質粒(pgl3luc,promega,charbonnières-les-bains,france)或piresl2δnls。后一種質粒在xbai和noti限制性位點之間含有改編hpv31l2的12至442位氨基酸的dna序列。該序列是從含有人類密碼子改編的hpv31全長l2基因的質粒中通過pcr擴增的[fleury等,clinvaccineimmunol2008;15(1):172-5]。對于293ft細胞中假病毒顆粒的生成,用0.5μgdna(0.25μgpgl3-luc,或pcmv-gfp或pires-l2質粒,0.25μgl1l2質粒)和1μlfugene6(roche)每cm2培養面積轉染細胞。轉染后兩天收獲細胞,并按照以前的描述純化假病毒顆粒[fleury等,clinvaccineimmunol2008;15(1):172-5],并在-80℃下保存待用。使用camvir-1抗體,通過與已知濃度的同源類型的vlp相比較,以western印跡測定假病毒顆粒的量。
hpv16和18假病毒顆粒的生產
通過以前發表的拆分-重新組裝法[touze等,nucleicacidsres1998;26(5):1317-23]并做一些修改[bousarghin等,molcancerther2009;8(2):357-65],生產了hpv16和18假病毒顆粒。在室溫下,將l1/l2vlp(100μg)在含有20mmol/ldtt和1mmol/legta的50mmol/ltris-hcl緩沖液(ph7.5)中孵育30分鐘。在此階段,向所述破壞的vlp中添加pgl3luc(10μg)。隨后在10nmzncl2存在下,用遞增濃度的cacl2(高至5mmol/l的終濃度)稀釋該制備物。隨后,用pbs1×過夜透析假病毒顆粒并儲存在4℃下備用。
免疫方案
將6周齡的balb/c小鼠(cerjjanvier,legeneststisle,france)用不同的疫苗制備物進行肌內免疫。組1的小鼠接受鹽水,組2至5的小鼠分別接受有或沒有氫氧化鋁的10μghpv16l2-sa蛋白(l2sa)、l1stii-l2sa(l1l2savlp)、hpv16l1l2(l1l2vlps)。組6和7的小鼠分別接受1或10μgpires-hpv31l2δnls質粒(dnal2)。組8至10的小鼠分別接受hpv31l1、hpv31l1-31l213-88vlp(l1/l2(13-88)vlp)、hpv31l1l2vlp(31l1l2vlp)。組11的小鼠接受10μg含有hevorf2108-660表達質粒(hevpsv)的hpv31假病毒顆粒。組12和13的小鼠分別接受含有gfp表達質粒(gfppsv)的hpv58假病毒顆粒和包封有hpv31l2δnls質粒(l2psv)的hpv58假病毒顆粒。通過western印跡分析在不同的l1l2vlp和假病毒顆粒之間調節l1蛋白的量。在第0、7和21天對小鼠進行免疫。最后一次注射后兩周收集血清樣品并儲存于-20℃。所有動物操作都是按照批準的方案進行的,并且遵從實驗動物合理使用和照顧的推薦標準,實驗由地區動物倫理委員會(creeacentrelimousin)批準。
通過elisa測定抗hpv血清效價
將200納克的vlp分配到96孔板(maxisorp,nunc,atgc,marne-la-vallée,france)的一半孔中,并在4℃下孵育過夜。用pbs-吐溫(0.1%)清洗兩次后,在37℃下用補充有1%fcs的pbs飽和1小時。在45℃下,將孔一式兩份(一個測試和一個對照)用以稀釋緩沖液(pbs5x,1%吐溫,10%fcs)兩倍稀釋(始于1∶25)的小鼠血清孵育1小時。清洗4次后,將在pbs-吐溫(1%)-fcs(10%)中按1∶1000稀釋的過氧化物酶綴合的山羊抗小鼠igg(fc特異性的)(sigmaaldrich)添加至孔中,并在45℃下孵育1小時。清洗4次后,添加在25mmol/l檸檬酸鈉和50mmol/lna2hpo4中的0.4mg/ml鄰苯二胺和0.03%過氧化氫。30分鐘之后,用h2so44n終止反應并在492nm讀取光密度(od)。對于數據分析,從測試抗原的od值中減去在l2不存在下獲得的od值。當測試孔與對照孔之間od差異大于0.2時,結果被認為是陽性的。各效價代表給出od差異大于0.2的最終稀釋度的倒數。各小鼠的值為一式兩份的平均值。計算每個組的幾何平均效價(geometricmeantiter,gmt)。將沒有可檢出抗體效價(<25)的動物的效價指定為1,以計算gmt。對于抗l2抗體的檢測而言,進行與上文中所述相同的elisa,不同之處是將純化的l2sa蛋白添加至vlp所在的nunc板的每個孔中。
通過elisa檢測l1、l2和strep-tag基序
通過elisa分析了嵌合vlp的l1抗原性和l2或strep-tag模體在vlp表面上的存在。在4℃下,用200ngvlp將微滴定板的孔包被過夜。按照上文中的描述,使用抗streptagii的單克隆抗體或多克隆的抗l2抗體進行elisa,用來分別研究vlp表面上的streptagii基序和l2蛋白的存在,或使用h16.v5和h31.f16單克隆抗體,以分別研究hpv16和hpv31l1蛋白的構象表位的存在。
hpv16、18、31和58假病毒顆粒的中和測定
通過抑制用含有pgl3-luc質粒的假病毒顆粒對cos-7細胞的假感染來進行中和測定。在96孔板(tpp,atgc)中接種cos-7細胞(104/孔)。在37℃下孵育24小時之后,清洗細胞兩次,之后加入假病毒顆粒/稀釋的血清混合物。調節假病毒顆粒的量以獲得0.2rlu的相對螢光素酶活性(luminoskanascent,thermoscientific,courtaboeuf,france)(hpv16為1∶500、hpv18為1∶50、hpv31為1∶800和hpv58為1∶10000),并且將50μl的稀釋的假病毒顆粒與50μl以不完全dmem兩倍稀釋(從1∶25至1∶51,200)的小鼠血清混合。在37℃下孵育1小時之后,將所述混合物添加至孔中。37℃下3小時后,添加100μl完全dmem。
在37℃下孵育48h之后,測量螢光素酶的基因表達(螢火蟲螢光素酶一步測定試劑盒,fluoprobes,interchim,
統計學分析
比較各抗體效價和幾何平均效價,以評價elisa和中和性應答。使用xlstat軟件(addinsoft,paris,france)通過t檢驗比較組的結果(每組10只動物)。
結果
hpv31l2和hpv16l2嵌合顆粒以及編碼l2的hpv58假病毒顆粒的生產
我們生產了兩種嵌合l1-l2顆粒,以研究l2疫苗針對廣譜hpv類型的保護潛力。為了用l2修飾衣殼的外側,第一種是基于hpv16l1修飾的vlp蛋白與融合至streptactin的hpv16l2蛋白之間的相互作用,所述streptactin為鏈霉親和素的工程化形式。為實現這一目的,將模擬生物素結合環的序列streptagii肽(wshpqfek,seqidno:12)插入到l1蛋白的de環位置140/141之間,以避免生物素與l1vlp化學偶聯,生物素具有與l1中和表位偶聯的風險。當使用重組桿狀病毒在sf-21昆蟲細胞中表達和在cscl梯度上純化時,l1stii重組蛋白自組裝成為與野生型l1蛋白具有相同外觀和類似產量的病毒樣顆粒(圖16)。將載玻片用乙酸鈾酰負染并用透射電鏡以50000×放大倍數觀察(標尺條=200nm)。
第二種嵌合型l1/l2蛋白含有插入到hpv31l1蛋白的de環中的hpv31l2肽(aa13-88)。當使用重組桿狀病毒在昆蟲細胞中表達時,l1l2(13-88位)重組蛋白不允許產生形狀良好的vlp,而是主要導致蛋白和/或殼粒的聚集(圖16)。
通過elisa,使用針對構象和線性表位的抗l1mab研究了這兩種嵌合vlp的l1抗原性(圖17)。結果表明,嵌合型hpv16l1stiivlp上h16.v5所識別的構象l1表位不受影響。然而,與所觀察到的與hpv31l1vlp的結合相比,觀察到了h31.f16mab與hpv31l1-l213-88vlp的結合的明顯降低。還通過elisa,使用分別針對streptagii序列或多克隆的抗l2抗體的mab研究了vlp表面上的streptagii或l2肽(13-88)的存在。所獲得的結果(圖17)顯示,streptagii和l2序列存在于嵌合vlp的表面上。
此外,通過將5μgvlp與對應于1/1質量比(一個l2sa蛋白/一個l1蛋白)的10μgl2sa融合蛋白混合而測定了l1stiivlp與l2sa蛋白結合的能力。通過復合vlp的超離心繼之以用western印跡檢測l2sa分析了l2sa與l1stiivlp的結合。在超離心沉淀中檢測到l2sa和l1stiivlp(圖18),表明l2sa蛋白與vlp有效地結合。當l2sa與野生型hpv16vlp混合時,未觀察到結合。elisa也證明了l2蛋白在l1l2savlp中的存在(圖17)。在293ft細胞中生產了包封有編碼hpv-31l2δnls基因的質粒的hpv58假病毒顆粒。通過感染cos-7細胞研究了其轉導l2基因的能力。l2蛋白表達的western印跡分析表明,轉導后兩天檢測到了l2(圖18)。為了排除在cos-7細胞中檢出的l2是因為存在輸入的假病毒顆粒的可能性,用包封了gfp基因的類似假病毒顆粒轉導了cos-7細胞。在這些情況下,未證明l2的存在(圖18)。
用嵌合vlp和假病毒顆粒免疫的小鼠中的抗hpv16-l2免疫應答
在未免疫的小鼠中未檢測到抗hpv16l2抗體(組1)。在接受l2sa蛋白的小鼠(組2)中,觀察到了348的抗l2gmt(表6)。在用hpv16l1l2savlp和hpv16l1l2vlp免疫的小鼠(組3和4)中,觀察到了抗l2抗體水平的增加,gmt分別為1160和1055(p=0.035和p=0.05)。向hpv16l1l2vlp中添加氫氧化鋁作為佐劑(組5)進一步以非顯著性的方式(p=0.247)增加了同源性的抗l2抗體的水平。
在用hpv31l1vlp免疫的小鼠(組8)中未檢測到抗l2抗體,但在l1l213-88vlp免疫的所有小鼠(組9)中,gmt為730,而在以lil2vlp免疫的小鼠(組10)中水平更高,gmt為1100(p=0.189)。在以對照假病毒顆粒免疫接種的小鼠(組11和12)中,檢測到了類似水平的抗l2抗體,gmt為855和1212(p=0.459)。通過比較這些對照假病毒顆粒,在以編碼l2的假病毒顆粒免疫的小鼠中,抗l2gmt(2600)更高(分別為p=0.001和p=0.101)。
表6:
誘導針對hpv18、hpv31和hpv58的中和性抗體
用hpv16l2sa蛋白或hpv16l1l2vlp免疫的小鼠(組3至5)中均未產生針對異源hpv類型(hpv18、hpv31和hpv58)的中和性抗體(表6)。當向通過l1和l2蛋白的自組裝獲得的hpv16vlp中添加氫氧化鋁時,僅僅檢測到針對hpv31的低水平的中和性抗體(gmt85)(組5)。
在以hpv31l1或hpv31l1l2vlp和hpv31hevpsv免疫的小鼠(組8、10和11)中檢測到了同源性的hpv31中和性抗體,gmt分別為2800、3400和5198(圖19)。低效價的hpv58中和性抗體僅在接受hpv31l1l2vlp(組10)和含有hevorf2無關基因的hpv31假病毒顆粒(組11)的小鼠中觀察到。在接受hpv31疫苗制備物的來自組8至11的小鼠中,未檢測到針對hpv18的中和性抗體。
在以hpv58假病毒顆粒免疫接種的小鼠(組12和13)中檢測到了高水平的同源中和性抗體,gmt分別為4650和5382。在以編碼gfp的假病毒顆粒免疫的小鼠中檢測到了低水平的針對hpv31(gmt=50)的中和性抗體,并且在以編碼hpv31l2蛋白的hpv58假病毒顆粒免疫的小鼠中觀察到了顯著增加的抗hpv31中和性抗體(gmt為733)。僅在用hpv58l2psv免疫的小鼠中,僅僅檢測到針對hpv18的中和性抗體,gmt為400。還研究了來自組10、12和13的小鼠的hpv16中和性抗體。以hpv31l1l2vlp免疫接種的小鼠產生了低水平的hpv16中和性抗體,gmt為40。在以編碼gfp的hpv58psv免疫的小鼠(組12)中未檢測到hpv16中和性抗體,但在以編碼l2的hpv58psv免疫的小鼠(組13)中檢測到了hpv16,gmt為60。
專利、專利申請和科學出版物以及參考文獻通過引用全文并入本文。
以下內容對應于母案申請中的原始權利要求書,現作為說明書的一部分并入此處:
1.一種遞送化合物至對象的方法,所述方法包括
給對象施用經修飾人乳頭瘤病毒(hpv)樣顆粒,其中所述顆粒包含一種或多種包封在hpv樣顆粒中的異源化合物,所述顆粒包含免疫原性改變的表面蛋白。
2.項1的方法,其中所述表面蛋白為具有經修飾fg環序列的經修飾l1蛋白。
3.項2的方法,其中所述l1蛋白具有hpv16、hpv31、hpv33、hpv34、hpv35、hpv52、hpv58、hpv73或hpv91血清型的序列,并且其中所述l1蛋白的fg環具有一個或多個氨基酸改變,所述改變使所述蛋白在人對象中的免疫原性發生改變。
4.項3的方法,其中所述一個或多個氨基酸改變是在seqidno:11的x1-x17中的一個或多個位置上。
5.項4的方法,其中在位置x16的氨基酸沒有改變。
6.項5的方法,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的一個或多個是經修飾的。
7.項6的方法,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的2-3個是經修飾的。
8.項6的方法,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的4-7個是經修飾的。
9.項6的方法,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的3個是經修飾的。
10.項6的方法,其中seqidno:11的位置x6、x11和x14是經修飾的。
11.項6的方法,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14全部都是經修飾的。
12.項10的方法,其中所述l1蛋白具有hpv16血清型的序列,其中seqidno:11的位置x6、x11和x14分別改變成t、t和n,并且seqidno:11的其余位置具有hpv16血清型的特征性氨基酸。
13.項10的方法,其中所述l1蛋白具有hpv16血清型的序列,其中位置x1、x2、x3、x5、x6、x11和x14分別改變成f、s、t、s、t、t和n,并且seqidno:11的其余位置具有hpv16血清型的特征性氨基酸。
14.前述項中任一項的方法,其中所述一種或多種化合物是治療劑或醫療劑。
15.前述項中任一項的方法,其中所述治療劑是核酸或小分子。
16.項15的方法,其中所述治療劑是sirna、shrna或者編碼sirna或shrna的核酸。
17.項16的方法,其中所述sirna或shrna靶向hpv-e6和/或hpv-e7。
18.項15的方法,其中所述小分子是抗病毒劑。
19.項15的方法,其中所述小分子是抗癌劑。
20.項15的方法,其中所述小分子是吉西他濱。
21.前述項中任一項的方法,其中所述hpv樣顆粒與其它藥劑一起施用。
22.項21的方法,其中所述其它藥劑是抗病毒劑。
23.項21的方法,其中所述其它藥劑是抗癌劑。
24.項21的方法,其中所述其它藥劑是吉西他濱。
25.前述項中任一項的方法,其中所述醫療化合物是成像劑或造影劑。
26.前述項中任一項的方法,其中所述hpv樣顆粒施用給對所述表面蛋白的血清型沒有中和免疫應答的對象。
27.項26的方法,其中所述對象未針對所述表面蛋白的血清型進行過免疫。
28.項26的方法,其中所述對象未感染過具有與所述hpv樣顆粒中所述表面蛋白的血清型相同血清型的hpv。
29.項26的方法,其中所述對象的所述免疫應答是在選擇用于施用的hpv樣顆粒之前評價的。
30.前述項中任一項的方法,其中所述hpv樣顆粒施用于粘膜組織。
31.前述項中任一項的方法,其中所述hpv樣顆粒施用于上皮部位。
32.項30的方法,其中所述粘膜組織是宮頸組織。
33.前述項中任一項的方法,其中所述hpv樣顆粒被表面施用。
34.前述項中任一項的方法,其中所述hpv樣顆粒被靜脈施用。
35.前述項中任一項的方法,其中所述hpv樣顆粒施用于感染了病毒的組織。
36.項35的方法,其中所述病毒是hpv。
37.項35的方法,其中所述病毒是皰疹病毒。
38.項37的方法,其中所述病毒是hsv。
39.項35-38中任一項的方法,其中所述化合物是抗病毒化合物。
40.項35-38中任一項的方法,其中所述化合物是靶向病毒rna的sirna、hnrna或反義rna。
41.項35-38中任一項的方法,其中所述化合物是表達靶向病毒rna之sirna、hnrna或反義rna的質粒。
42.前述項中任一項的方法,其中所述hpv樣顆粒施用于患有與hpv感染相關的癌的對象。
43.前述項中任一項的方法,其中所述hpv樣顆粒施用于患有與hpv感染相關病毒感染的對象。
44.項43的方法,其中所述病毒感染是hsv感染。
45.前述項中任一項的方法,其中所述hpv樣顆粒施用于患有與hpv感染相關之細菌或寄生蟲感染的對象。
46.一種在有免疫系統缺陷的對象中治療皮膚病癥的方法,
所述方法包括將前述項中任一項的組合物施用于有免疫系統缺陷的對象的皮膚感染部位,
其中所述組合物包含用于治療皮膚感染的藥劑。
47.項46的方法,其中所述免疫系統缺陷與hiv感染相關。
48.項46的方法,其中所述皮膚感染為病毒、細菌、微生物或寄生蟲感染。
49.一種方法,包括給患有癌的對象施用前述項中任一項的表面組合物,其中所述組合物包含有效降低癌的生長或發育的化合物,并且其中所述組合物與用于促進施用部位的非特異性免疫應答的組合物一起施用。
50.一種方法,包括給患有癌的對象施用前述項中任一項的表面組合物,其中所述組合物包含有效降低癌的生長或發育的化合物,并且其中施用兩種或更多種具有不同血清型的不同hpv表面蛋白,以促進施用部位的免疫應答。
51.一種向對象施用化合物的方法,所述方法包括:
在第一時間段中向對象施用包含化合物的第一hpv樣顆粒,和
在第二時間段中向對象施用包含所述化合物的第二hpv樣顆粒,其中所述第一和第二hpv樣顆粒具有不同的血清型。
52.項51的方法,其中所述第一和第二hpv樣顆粒的血清型獨立地為天然或改變的血清型。
53.項52的方法,其中所述第一和/或第二hpv樣顆粒的血清型是嵌合的血清型。
54.一種治療對象中hpv相關宮頸癌的方法,所述方法包括:
給患有hpv相關宮頸癌的對象施用hpv樣顆粒,所述顆粒包含一種或多種治療劑,其量足以治療所述hpv相關宮頸癌。
55.項54的方法,其中所述hpv樣顆粒表面施用。
56.項54的方法,其中所述hpv樣顆粒表面施用于上皮或其附近,所述上皮例如宮頸上皮;或者表面施用于上皮病變處或其附近,所述病變例如宮頸癌或肛門上皮癌。
57.一種用于將化合物遞送給對象的組合物,所述組合物包含經修飾人乳頭瘤病毒(hpv)樣顆粒,其中所述顆粒包含包封于hpv樣顆粒中的一種或多種異源化合物,所述顆粒包含免疫原性改變的表面蛋白。
58.項57的所述組合物,其中所述衣殼蛋白是l1蛋白。
59.項58的所述組合物,其中所述l1蛋白具有經修飾fg環序列。
60.項59的所述組合物,其中所述l1蛋白具有hpv16、hpv31、hpv33、hpv34、hpv35、hpv52、hpv58、hpv73或hpv91血清型的序列,并且其中所述l1蛋白的fg環具有一個或多個氨基酸改變,所述改變使該蛋白在人對象中的免疫原性發生改變。
61.項60的所述組合物,其中所述一個或多個氨基酸改變是在seqidno:11的x1-x17中的一個或多個位置處。
62.項59-61中任一項的組合物,其中位置x16的氨基酸沒有改變。
63.項59-61中任一項的組合物,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的一個或多個是經修飾的。
64.項63的組合物,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的2-3個是經修飾的。
65.項63的組合物,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的4-7個是經修飾的。
66.項63的組合物,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14中的3個是經修飾的。
67.項63的組合物,其中seqidno:11的位置x6、x11和x14是經修飾的。
68.項63的組合物,其中seqidno:11的位置x1、x2、x3、x5、x6、x11和x14全部是經修飾的。
69.項67的組合物,其中所述l1蛋白具有hpv16血清型的序列,其中seqidno:11的位置x6、x11和x14分別改變成t、t和n,并且seqidno:11的其余位置具有hpv16血清型的特征性氨基酸。
70.項68的組合物,其中所述l1蛋白具有hpv16血清型的序列,其中位置x1、x2、x3、x5、x6、x11和x14分別改變成f、s、t、s、t、t和n,并且seqidno:11的其余位置具有hpv16血清型的特征性氨基酸。
71.項57的組合物,其中所述一種或多種化合物是治療劑或醫療劑。
72.項71的組合物,其中所述治療劑是核酸或小分子。
73.項72的組合物,其中所述治療劑是sirna、shrna或者編碼sirna或shrna的核酸。
74.項73的組合物,其中所述sirna或shrna靶向hpv-e6和/或hpv-e7。
75.項72的組合物,其中所述小分子是抗病毒劑。
76.項75的組合物,其中所述小分子是抗癌劑。
77.項75的組合物,其中所述小分子是吉西他濱。
78.項57的組合物,其中所述hpv樣顆粒包含l1蛋白,或者包含l1蛋白與l2蛋白。
79.項57的所述組合物,其中所述表面蛋白是嵌合的,并且包含融合進l1環中的l2序列。
80.項57的組合物,其中所述l2序列附著至l1顆粒的表面。
81.項79或80的組合物,其中所述l2序列是hpv31l2蛋白的13至88位殘基。
序列表
<110>inserm,institutnationaldelasanteetdelarecherche
medicale
aurabiosciences
coursaget,pierrel.
touze,antoinea.
fleury,maximej.j.
combelas,nicolas
muniz,edmundo
delospinos,elisabet
<120>hpv顆粒及其用途
<130>a0915.70002wo00
<150>us61/168914
<151>2009-04-13
<160>65
<170>patentinversion3.5
<210>1
<211>39
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>1
phevalarghisleupheasnargalaglyalavalglygluasnval
151015
proaspaspleutyrilelysglyserglyserthralaasnleuala
202530
serserasntyrpheprothr
35
<210>2
<211>39
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>2
phevalarghisphepheasnargserglythrvalglygluserval
151015
prothraspleutyrilelysglyserglyserthralathrleuala
202530
asnserthrtyrpheprothr
35
<210>3
<211>39
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>3
phevalarghisphepheasnargalaglylysleuglyglualaval
151015
proaspaspleutyrilelysglyserglythrthralaserilegln
202530
serseralaphepheprothr
35
<210>4
<211>39
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>4
phevalarghisleupheasnargalaglythrvalglyaspalaile
151015
proaspaspleumetilelysglythrglyasnthralaserproser
202530
sercysvalphetyrprothr
35
<210>5
<211>37
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>5
phevalarghisleupheasnargalaglythrvalglygluthrval
151015
proalaaspleutyrilelysglythrthrglythrleuproserthr
202530
sertyrpheprothr
35
<210>6
<211>41
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>6
phevalarghisphepheasnargalaglythrleuglyaspproval
151015
proglyaspleutyrilelysglyserasnserglyasnthralathr
202530
valglnserseralaphepheprothr
3540
<210>7
<211>39
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>7
phevalarghisphepheasnargalaglylysleuglyglualaval
151015
proaspaspleutyrilelysglyserglyasnthralavalilegln
202530
serseralaphepheprothr
35
<210>8
<211>39
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>8
phevalarghisleupheasnargalaglyaspthrglyasplysile
151015
proaspaspleumetilelysglythrglyasnthralathrproser
202530
sercysvalphetyrprothr
35
<210>9
<211>39
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>9
phevalarghisphepheasnargalaglythrthrglyaspalaval
151015
prolysaspleutyrilealaglythrglyasnargalaasnileala
202530
glyseriletyrtyrserthr
35
<210>10
<211>41
<212>prt
<213>人工序列
<220>
<223>合成的肽
<220>
<221>misc_feature
<222>(11)..(11)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(15)..(15)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(18)..(18)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(26)..(27)
<223>x=任何氨基酸或無氨基酸
<220>
<221>misc_feature
<222>(32)..(34)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(37)..(37)
<223>x=任何氨基酸
<400>10
phevalarghisphepheasnargalaglyxaavalglygluxaaval
151015
proxaaaspleutyrilelysglyserxaaxaaglyasnthralaxaa
202530
xaaxaaserserxaaphepheprothr
3540
<210>11
<211>41
<212>prt
<213>人工序列
<220>
<223>合成的肽
<220>
<221>misc_feature
<222>(5)..(5)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(9)..(9)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(11)..(12)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(14)..(14)
<223>x=eord
<220>
<221>misc_feature
<222>(15)..(15)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(16)..(16)
<223>x=vori
<220>
<221>misc_feature
<222>(18)..(18)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(21)..(21)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(23)..(23)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(25)..(25)
<223>x=sort
<220>
<221>misc_feature
<222>(26)..(27)
<223>x=任何氨基酸或無氨基酸
<220>
<221>misc_feature
<222>(29)..(30)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(31)..(31)
<223>x=aorg
<220>
<221>misc_feature
<222>(32)..(37)
<223>x=任何氨基酸
<220>
<221>misc_feature
<222>(38)..(39)
<223>x=fory
<220>
<221>misc_feature
<222>(40)..(40)
<223>x=任何氨基酸
<400>11
phevalarghisxaapheasnargxaaglyxaaxaaglyxaaxaaxaa
151015
proxaaaspleuxaailexaaglyxaaxaaxaaglyxaaxaaxaaxaa
202530
xaaxaaxaaxaaxaaxaaxaaxaathr
3540
<210>12
<211>8
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>12
trpserhisproglnpheglulys
15
<210>13
<211>19
<212>rna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>13
uacaacaaaccguugugug19
<210>14
<211>19
<212>rna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>14
cuaacuaacacuggguuau19
<210>15
<211>21
<212>rna
<213>人工序列
<220>
<223>合成的寡核苷酸
<220>
<221>misc_feature
<222>(20)..(21)
<223>n=t
<400>15
gagguauaugacuuugcuunn21
<210>16
<211>21
<212>rna
<213>人工序列
<220>
<223>合成的寡核苷酸
<220>
<221>misc_feature
<222>(1)..(2)
<223>n=t
<400>16
nncuccauauacugaaacgaa21
<210>17
<211>21
<212>rna
<213>人工序列
<220>
<223>合成的寡核苷酸
<220>
<221>misc_feature
<222>(20)..(21)
<223>n=t
<400>17
aggaggaugaaauagauggnn21
<210>18
<211>21
<212>rna
<213>人工序列
<220>
<223>合成的寡核苷酸
<220>
<221>misc_feature
<222>(1)..(2)
<223>n=t
<400>18
nnuccuccuacuuuaucuacc21
<210>19
<211>47
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>19
caccagagttcaaaagcccttcatcgaaatgaagggcttttgaactc47
<210>20
<211>47
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>20
aaaaagagttcaaaagcccttcatttcgatgaagggcttttgaactc47
<210>21
<211>47
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>21
caccgctacacaaatcagcgatttcgaaaaatcgctgatttgtgtag47
<210>22
<211>47
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>22
aaaactacacaaatcagcgatttttcgaaatcgctgatttgtgtagc47
<210>23
<211>49
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>23
caccaggaggatgaaatagatggttcgaaaaccatctatttcatcctcc49
<210>24
<211>49
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>24
aaaaggaggatgaaatagatggttttcgaaccatctatttcatcctcct49
<210>25
<211>50
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>25
caccgcccattacaatattgtaacccgaaggttacaatattgtaatgggc50
<210>26
<211>50
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>26
aaaagcccattacaatattgtaaccttcgggttacaatattgtaatgggc50
<210>27
<211>50
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>27
caacgaggtatatgactttgcttttcgaaaaaagcaaagtcatatacctc50
<210>28
<211>50
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>28
aaaagaggtatatgactttgcttttttcgaaaagcaaagtcatatacctc50
<210>29
<211>50
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>29
caccggtcgatgtatgtcttgttgccgaagcaacaagacatacatcgacc50
<210>30
<211>50
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>30
aaaaggtcgatgtatgtcttcttgcttcggcaacaagacatacatcgacc50
<210>31
<211>22
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>31
caccaaaagagaactgcaatgt22
<210>32
<211>22
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>32
ttgctgttctaatgttgttcca22
<210>33
<211>23
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>33
ggagatacacctacattgcatga23
<210>34
<211>20
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>34
ggggcacacaattcctagtg20
<210>35
<211>21
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>35
acagtccatgccatcactgcc21
<210>36
<211>21
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>36
gcctgcttcaccaccttcttg21
<210>37
<211>31
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>37
ggatcccaccatgagcctgtggagacccagc31
<210>38
<211>33
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>38
ggaagcttatgtggtggtgctggcgctgggggc33
<210>39
<211>34
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>39
gcaagcttaggcctgcagcaggaactttctgccc34
<210>40
<211>30
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>40
ccgctagccaccatgagcctgtggagaccc30
<210>41
<211>39
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>41
ctctctgctggcggggtcgttgaagaagtgccgcacgaa39
<210>42
<211>30
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>42
cggaattctatcacttcttggttttcttcc30
<210>43
<211>39
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>43
gaccccgccagcagagagagaagcggcaccgtgggcgag39
<210>44
<211>9
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>44
servalprothraspleutyrilelys
15
<210>45
<211>10
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>45
arghisphepheasnargserglythrval
1510
<210>46
<211>5
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>46
aspleuiletyrlys
15
<210>47
<211>8
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>47
arghisphepheasnargsergly
15
<210>48
<211>9
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>48
serglythrvalglygluservalpro
15
<210>49
<211>6
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>49
argserglythrvalgly
15
<210>50
<211>9
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>50
argserglythrvalglygluserval
15
<210>51
<211>31
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>51
ggatcccaccatgagcctgtggagacccagc31
<210>52
<211>31
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>52
aagctttcacttcttggttttcttccgcttg31
<210>53
<211>49
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>53
cttctcgaactgggggtggctccagttctcggtgtcgtccagcttgttc49
<210>54
<211>48
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>54
tggagccacccccagttcgagaaggccagcgcctacgccgccaacgcc48
<210>55
<211>31
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>55
aagctttcacttcttggttttcttccgcttg31
<210>56
<211>31
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>56
ggatcccaccatgagcctgtggagacccagc31
<210>57
<211>44
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>57
cgggtctagagaattctcgagagggcctccggcgtatctgttgc44
<210>58
<211>42
<212>dna
<213>人工序列
<220>
<223>合成的肽
<400>58
ctcgagaattctctagacccgggcaccgataacagggagtgc42
<210>59
<211>27
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>59
cccgggggccagggtgtcggtggcggt27
<210>60
<211>30
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>60
ctcgaggccagcgccacccagctgtacaag30
<210>61
<211>31
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>61
gtcgaccatgtagtagctggggtgcaggatg31
<210>62
<211>35
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>62
ccggatccgccaccatggccagcgccacccagctg35
<210>63
<211>39
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>63
ccctctagagccaccatggccagcgccacccagctgtac39
<210>64
<211>37
<212>dna
<213>人工序列
<220>
<223>合成的寡核苷酸
<400>64
gcggccgctatcacaggatgtagtagctggggtgcag37
<210>65
<211>6
<212>prt
<213>人工序列
<220>
<223>合成的肽
<400>65
aspproalaserargglu
15
- 還沒有人留言評論。精彩留言會獲得點贊!