磁性聯合交聯酶聚集體生物催化劑及其制備方法和應用與流程
本發明屬于生物工程技術領域,具體涉及一種磁性聯合交聯酶聚集體生物催化劑及其制備方法和應用。
背景技術:
(r)-3-奎寧醇(分子式c7h13no,分子量為127.18,cas號:25333-42-0)是合成阿地溴銨、索利那新和瑞伐托酯等藥物的關鍵性手性中間體。目前工業上主要是利用手性催化劑,如:xylskewphos/pica-ruthenium(ii)復合物或binap/iphan-ru(ii)復合物等,不對稱還原3-奎寧酮合成(r)-3-奎寧醇,但該化學合成方法需篩選手性配體;所使用的過渡金屬價格昂貴、毒性較大、難以從產物中去除;而且制備的產物光學純度較低,需進一步純化。另一種方法是外消旋拆分,該方法的缺陷在于其理論產率最大只有50%。
相對于化學合成方法,基于酶的生物合成法具有底物特異性;高度化學選擇性、區域選擇性和立體選擇性;反應條件溫和;催化活性高;原子經濟性好等獨特優勢。生物方法合成(r)-3-奎寧醇涉及兩個過程:一是借助羰基還原酶利用nadh或nadph將3-奎寧酮還原為(r)-3-奎寧醇;二是借助輔酶再生酶將氧化型nad+或nadp+轉化為還原型nadh或nadph,實現雙酶偶聯不對稱還原合成(r)-3-奎寧醇。具體過程如下:
生物催化不對稱還原合成(r)-3-奎寧醇過程
無論是用野生型微生物全細胞還是重組微生物全細胞作為生物催化劑,由于細胞本身結構的限制,致使底物/產物、輔酶在細胞內外擴散受阻,導致生物轉化時間長、催化效率低。而游離酶被認為是化學工業合成中最為有效的手性催化合成工具之一。但在實際的生產應用過程中,由于酶生物催化劑脫離酶所依賴的自然環境,致使其穩定性降低、催化活性低。盡管通過定向進化、基因重排和定點突變等生物分子工程技術能改善酶的穩定性和催化活性,但技術難道大、酶純化成本高、回收過程復雜、易致產品污染、難以循環利用等問題嚴重阻礙了酶的商業化以及在工業領域的催化應用。
酶固定化技術既能有效克服游離酶生物催化劑的缺陷,又能提高酶的穩定性和催化活性,易于從反應混合物中分離和循環再利用,實現連續反應,降低生產成本(robertdicosimo,josephmcauliffe,ayrookaranj.poulosebandgregorybohlmann,industrialuseofimmobilizedenzymes,chem.soc.rev.,2013,42,6437-6474)。但基于載體的物理吸附、化學鍵結合和包埋等酶固定化方法:需使用高純度的酶,致使生產成本增加;需使用無催化活性的載體,導致酶的體積活性、時空產率和催化產率降低。基于無載體的交聯酶聚集體(cleas)是一種快速、簡單和低成本的固定化方法:無需高純度酶,生產成本降低;能直接從發酵液中一步實現純化和固定化單酶(完成一步反應)或多酶(完成級聯反應);能提高酶的長期操作穩定性和催化活性;能循環再利用。但是cleas質軟、機械性能差、易聚集成塊、難以過濾回收,這些缺陷都阻礙了cleas的工業化應用。
技術實現要素:
為了解決現有技術中的問題,根據本發明的第一方面,本發明的目的在于提供一種磁性聯合交聯酶聚集體(combi-cleas)生物催化劑,該生物催化劑能用于催化級聯反應、長期操作穩定性好、催化活性高、易于磁分離和可循環再利用。
本發明的目的是這樣實現的:
一種磁性聯合交聯酶聚集體生物催化劑,包含nadh依賴的3-奎寧酮還原酶(qnr)、葡萄糖脫氫酶(gdh)、氨基功能化的磁性納米粒,其特征在于:在衍射角度2θ為30.5±0.2°、35.4±0.2°、44.7±0.2°、57.3±0.2°、63.4±0.2°處有衍射峰。
根據本發明的一個實施方案,上述磁性聯合交聯酶聚集體生物催化劑在波數為3316±4、2946±4、1659±4、1540±4、1092±4、799±4、583±4、463±4處有紅外特征吸收峰。
根據本發明的一個實施方案,上述磁性聯合交聯酶聚集體生物催化劑為球形顆粒,粒徑為1.5±0.5μm。
根據本發明的一個實施方案,上述磁性聯合交聯酶聚集體生物催化劑的酶負載量為5-15%。
根據本發明的一個實施方案,上述氨基功能化的磁性納米粒為氨基功能化的磁性fe3o4納米顆粒,由以下方法制得:將磁性fe3o4納米顆粒用乙醇/水混合溶液分散,在20-80℃以400-1000r/min攪拌1.0-3.0小時。加濃氨水攪拌0.5-1.5小時,再加入適量四乙氧基硅烷,控制轉速1000-2000r/min攪拌8-16小時,最后加入適量氨丙基三乙氧基硅烷,ph值8-11,轉速1000-2000r/min攪拌8-16小時,然后磁性分離得到氨基功能化的磁性fe3o4納米顆粒。
根據本發明的一個實施方案,上述磁性fe3o4納米粒由以下方法制得:將fecl3·6h2o和fecl2·4h2o以物質的量之比為2:1的比例溶于去離子水中,在氮氣保護下以轉速500-1500r/min機械攪拌0.5-1.0小時,再加入濃度為8-12m的naoh溶液,以轉速1000-2000r/min機械攪拌1-1.5小時,溫度升至70-100℃,熟化0.5-2.0小時;降至室溫,磁性分離得到磁性fe3o4納米顆粒。
根據本發明的第二方面,本發明的另一目的在于提供上述磁性聯合交聯酶聚集體生物催化劑的制備方法。
根據本發明的一個實施方案,上述磁性聯合交聯酶聚集體生物催化劑的制備方法,包括磁性fe3o4納米顆粒的制備、磁性fe3o4納米顆粒氨基功能化、磁性聯合交聯酶聚集體步驟,其特征在于:所述磁性fe3o4納米顆粒的制備為將fecl3·6h2o和fecl2·4h2o以物質的量之比為2:1的比例溶于去離子水中,在氮氣保護以轉速500-1500r/min機械攪拌0.5-1.0小時,再加入濃度為8-12m的naoh溶液,轉速1000-2000r/min機械攪拌1-1.5小時,溫度升至70-100℃,熟化0.5-2.0小時,降至室溫,磁性分離得到磁性fe3o4納米顆粒;所述磁性fe3o4納米顆粒氨基功能化為將磁性fe3o4納米顆粒用乙醇/水混合溶液分散,在20-80℃以轉速400-1000r/min攪拌1.0-3.0小時。加濃氨水攪拌0.5-1.5小時后,再加入適量四乙氧基硅烷,控制轉速1000-2000r/min攪拌8-16小時,最后加入適量氨丙基三乙氧基硅烷,ph8-11,以轉速1000-2000r/min攪拌8-16小時,然后磁性分離得到氨基功能化的磁性fe3o4納米顆粒;所述磁性聯合交聯酶聚集體為將氨基功能化的磁性fe3o4納米顆粒分散在含有qnr和gdh的磷酸鹽緩沖溶液中,在4-25℃,轉速400-800r/min攪拌0.5-1.0小時,然后加入沉淀劑,攪拌0.5-1.5小時,再加入戊二醛,以轉速200-600r/min攪拌交聯1-12h,分離即得。
根據本發明的一個實施方案,上述沉淀劑選自乙醇、異丙醇、飽和硫酸銨、丙酮、乙腈中的一種或幾種組合;優選飽和硫酸銨。上述戊二醛的濃度為10-120mm,優選40mm。上述交聯時間為1-12小時,優選8小時。
具體的說,一種磁性聯合交聯酶聚集體生物催化劑的制備方法,其特征在于,采用如下步驟:
步驟(1)
將物質的量比為2:1的fecl3·6h2o(10.8116g)和fecl2·4h2o(3.9762g)溶于100-200ml去離子水,氮氣保護,轉速500-1500r/min機械攪拌0.5-1.0小時;滴加10-30ml濃度為8-12m的naoh溶液,轉速1000-2000r/min機械攪拌1-1.5小時;升溫至70-100℃,熟化0.5-2.0小時;降至室溫,磁性分離并用去離子水洗滌3-5次,干燥,得磁性fe3o4納米顆粒;
步驟(2)
取步驟(1)制備的磁性fe3o4納米顆粒100-200mg,分散到體積比為5:2的140-280ml的乙醇/水溶液中,氮氣保護,在20-80℃,轉速400-1000r/min攪拌1.0-3.0小時;加入2-4ml濃氨水,攪拌0.5-1.5小時后,加入0.4-0.8ml的四乙氧基硅烷,轉速1000-2000r/min攪拌8-16小時;滴加0.8-1.6ml氨丙基三乙氧基硅烷,ph8-11,轉速1000-2000r/min攪拌8-16小時;磁鐵分離,去離子水洗滌3-5次,得氨基功能化的磁性fe3o4納米顆粒;
步驟(3)
取步驟(2)制備的氨基功能化的磁性fe3o4納米顆粒4-6mg,分散在1.6-2.4ml含有qnr(4.0mg/ml)和gdh(2.0mg/ml)的磷酸鹽緩沖溶液(pbs,10mm,ph7.2-7.5)中,在4-25℃,轉速400-800r/min攪拌0.5-1.0小時。加入7-12倍體積的冰冷的沉淀劑,攪拌0.5-1.5h;加入0.8-1.2ml的戊二醛,轉速200-600r/min攪拌交聯1-12h;磁分離,pbs洗3次,得磁性combi-cleas。
本發明磁性fe3o4納米顆粒的制備中去離子水及氫氧化鈉溶液的用量由本領域普通技術人員根據實際情況確定;磁性fe3o4納米顆粒氨基功能化步驟中乙醇與水的比例、乙醇與水的用量、四乙氧基硅烷用量以及氨丙基三乙氧基硅烷用量均由本領域普通技術人員根據反應實際情況確定;磁性聯合交聯酶聚集體步驟中磷酸鹽緩沖溶液的用量根據實際情況確定,同時qnr和gdh的用量根據實際情況確定。
根據本發明的第三方面,本發明的再一目的在于提供上述磁性聯合交聯酶聚集體生物催化劑在合成(r)-3-奎寧醇中的應用。
根據本發明的第四方面,本發明的再一目的在于提供一種(r)-3-奎寧醇的合成方法,該方法使用上述磁性聯合交聯酶聚集體生物催化劑進行酶催化反應,合成(r)-3-奎寧醇。
根據本發明的一個實施方案,一種(r)-3-奎寧醇的合成方法,其特征在于:
將磁性combi-cleas分散在pbs中,加入3-奎寧酮,葡萄糖、nad+和nadh,在室溫條件下,ph為7.2-8.0,以50~150rpm轉速攪拌,生物轉化時間為1-3h。
具體的,一種(r)-3-奎寧醇的生物催化合成方法,包括如下步驟:
步驟(1)
將物質的量比為2:1的fecl3·6h2o(10.8116g)和fecl2·4h2o(3.9762g)溶于100-200ml去離子水,氮氣保護,轉速500-1500r/min機械攪拌0.5-1.0小時。滴加10-30ml濃度為8-12m的naoh溶液,轉速1000-2000r/min機械攪拌1-1.5小時。升溫至70-100℃,熟化0.5-2.0小時;降至室溫,磁性分離并用去離子水洗滌3-5次,干燥,得磁性fe3o4納米顆粒;
步驟(2)
取步驟(1)制備的磁性fe3o4納米顆粒100-200mg,分散到體積比為5:2的140-280ml的乙醇/水溶液中,氮氣保護,在20-80℃,轉速400-1000r/min攪拌1.0-3.0小時。加入2-4ml濃氨水,攪拌0.5-1.5小時后,加入0.4-0.8ml的四乙氧基硅烷,轉速1000-2000r/min攪拌8-16小時;滴加0.8-1.6ml氨丙基三乙氧基硅烷,ph8-11,轉速1000-2000r/min攪拌8-16小時;磁鐵分離,去離子水洗滌3-5次,得氨基功能化的磁性fe3o4納米顆粒;
步驟(3)
取步驟(2)制備的氨基功能化的磁性fe3o4納米顆粒4-6mg,分散在1.6-2.4ml含有qnr(4.0mg/ml)和gdh(2.0mg/ml)的磷酸鹽緩沖溶液(pbs,10mm,ph7.2-7.5)中,在4-25℃,轉速400-800r/min攪拌0.5-1.0小時。加入7-12倍體積的冰冷的沉淀劑,攪拌0.5-1.5小時;加入0.8-1.2ml的戊二醛,轉速200-600r/min攪拌1-12小時。磁分離,pbs洗3次,得磁性combi-cleas。
步驟(4)
取步驟(3)制備的combi-cleas生物催化劑40-60mg分散在含有:4-6mm3-奎寧酮、7.2-10.8mm葡萄糖、0.04-0.06mmnad+和0.04-0.06mmnadh的pbs中,總體積8-12ml;在4-25℃,ph7.5-8.0,以轉速50-200r/min攪拌,生物轉化時間為1-3小時。
有益效果:
1、本發明提供一種磁性聯合交聯酶聚集體生物催化劑,該催化劑在衍射角度2θ為30.5±0.2°、35.4±0.2°、44.7±0.2°、57.3±0.2°、63.4±0.2°處有衍射峰;同時在波數3316±4、2946±4、1659±4、1540±4、1092±4、799±4、583±4、463±4處有紅外特征吸收峰。經電鏡掃描顯示,本發明磁性聯合交聯酶聚集體生物催化劑具有凹凸不平的球形表面結構,粒徑為1.5±0.5μm;熱重分析顯示,本發明磁性聯合交聯酶聚集體生物催化劑酶負載量高達5-15%。
2、本發明使用氨基功能化的磁性納米粒聯合交聯酶聚集體固定化技術,從細胞裂解上清液中直接固定qnr和gdh,形成磁性combi-cleas生物催化劑,不需要高純度的qnr和gdh,能一步完成靶酶的純化和固定化;同時可通過磁性回收,制備與分離均不需要特殊設備,工藝條件溫和,操作方便,成本低,適合工業化。
3、本發明磁性聯合交聯酶聚集體生物催化劑(combi-cleas)硬度適中,機械性能較好;易于磁分離,可循環利用;循環過程中無qnr和gdh泄露,長期操作穩定性好,適合工業化。
4、使用本發明的磁性combi-cleas生物催化劑,用于不對稱合成(r)-3-奎寧醇,可實現羰基還原和輔酶nadh/nad+原位再生同時進行;同時能有效克服底物、輔酶和產物的擴散限制,催化活性好,催化效率高。
5、使用本發明的磁性combi-cleas催化劑不對稱合成(r)-3-奎寧醇,轉化率為100%,收率高達70-85%,對映體值為100%,同時轉化時間大大降低(1-3h),經濟價值明顯。本發明生物催化不對稱合成(r)-3-奎寧醇所用介質為水,有利于節約資源,環境友好,符合綠色化學和可持續發展要求。
附圖說明
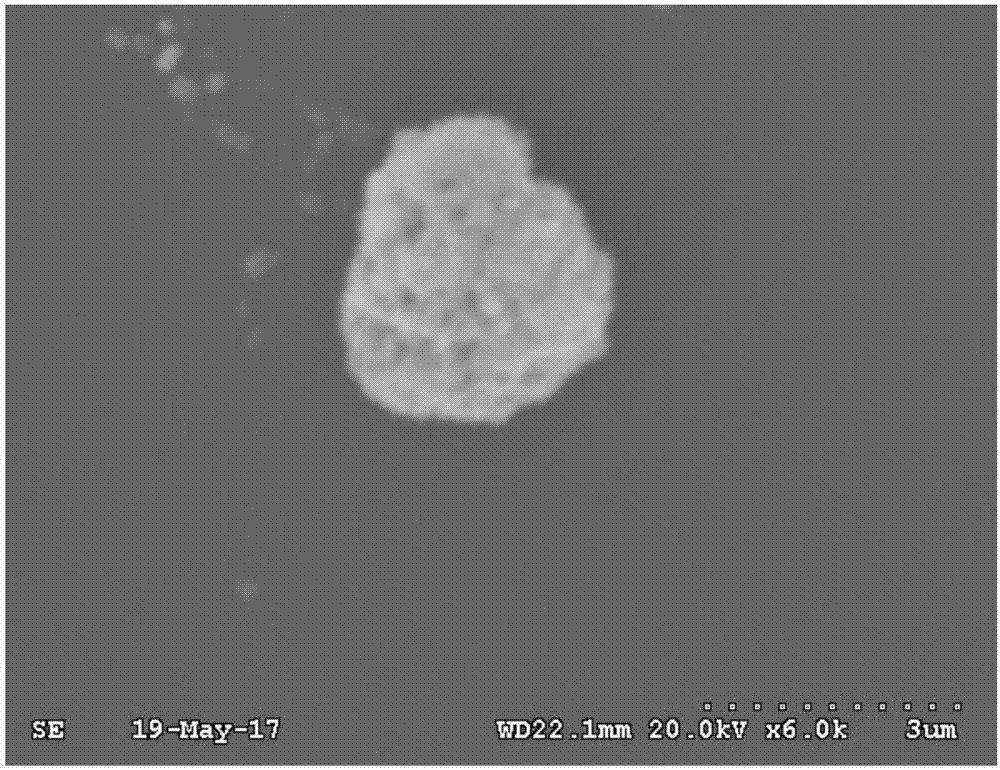
圖1是磁性combi-cleas的掃描電鏡分析;
圖2是磁性combi-cleas的紅外光譜分析;
圖3是磁性combi-cleas的粉末x衍射分析;
圖4是磁性combi-cleas的熱重分析;
圖5是磁性combi-cleas的循環再利用;
圖2-4中的磁性催化劑為本發明磁性聯合交聯酶聚集體生物催化劑。
具體實施方式
下面通過具體實施例對本發明進行具體描述,在此指出以下實施例只用于對本發明進行進一步說明,不能理解為對本發明保護范圍的限制,本領域的技術熟練人員可以根據上述發明內容對本發明作出一些非本質的改進和調整。除特殊說明外,本發明所述份數均為重量份,所述百分比均為質量百分比。本發明所有原料及試劑均為市售產品,其中緩沖溶液pbs購至北京中杉金橋生物技術有限公司,ph值為7.4。本發明濃氨水,濃度22-25%。本發明所用羰基還原酶為nadh依賴的特異性的3-奎寧酮還原酶(qnr,accessionno:ab733448),輔酶再生酶為葡萄糖脫氫酶(gdh,accessionno:ay930464)。
實施例1
酶活性測定
qnr酶活性測定:
標準反應混合體系:緩沖溶液b(pbs,ph7.2-7.4),3μmol3-奎寧酮,0.3μmolnadh,適量的酶qnr,總體積1ml。在λ=340nm處測定吸光度值變化。酶活性單位定義:25℃,1min內轉化1μmolnadh所需的酶量。
gdh酶活性測定:
標準反應混合體系:緩沖溶液b(pbs,ph7.2-7.4),10μmol葡萄糖,1μmolnad+,適量的酶gdh,總體積1ml。在λ=340nm處測定吸光度值變化。酶活性單位定義:25℃,1min內轉化1μmolnad+所需的酶量。
實施例2
磁性fe3o4納米顆粒的制備:
將物質的量比為2:1的fecl3·6h2o(10.8116g)和fecl2·4h2o(3.9762g)溶于100-200ml去離子水,氮氣保護,轉速500-1500r/min機械攪拌0.5-1.0小時。滴加10-30ml濃度為8-12m的naoh溶液,轉速1000-2000r/min機械攪拌1-1.5小時。升溫至70-100℃,熟化0.5-2.0小時;降至室溫,磁性分離并用去離子水洗滌3-5次,干燥,得磁性fe3o4納米顆粒;
磁性fe3o4納米顆粒氨基功能化:
取磁性fe3o4納米顆粒100-200mg,分散到體積比為5:2的140-280ml的乙醇/水溶液中,氮氣保護,在20-80℃,轉速400-1000r/min攪拌1.0-3.0小時。加入2-4ml濃氨水,攪拌0.5-1.5小時后,加入0.4-0.8ml的四乙氧基硅烷,轉速1000-2000r/min攪拌8-16小時;滴加0.8-1.6ml氨丙基三乙氧基硅烷,ph8-11,轉速1000-2000r/min攪拌8-16小時;磁鐵分離,去離子水洗滌3-5次,得氨基功能化的磁性fe3o4納米顆粒;
實施例3
聯合交聯固定qnr和gdh:
取實施例2制備的氨基功能化的磁性fe3o4納米顆粒5mg,分散在1.0ml含有qnr(4.0mg/ml)和gdh(2.0mg/ml)的磷酸鹽緩沖溶液(pbs,10mm,ph7.2-7.5)中,在4℃,轉速600r/min攪拌0.5小時。加入9倍體積的冰冷的沉淀劑(飽和硫酸銨),攪拌1.5小時。加入1.0ml濃度為40mm的戊二醛,轉速400r/min攪拌8.0h。磁分離,pbs洗3次,得磁性combi-cleas。
對實施例3制備的磁性combi-cleas進行掃描電鏡分析
將樣品溶液滴加于潔凈的蓋玻片上,40℃真空干燥,噴金覆蓋樣品,用掃描電鏡(sem,s-3000n型)成像,分析結果見附圖1。附圖1為combi-cleas微球,呈現表面凹凸不平的球形。
對實施例3制備的磁性combi-cleas進行紅外光譜分析
紅外光譜分析:采用kbr壓片法制備樣品,范掃波長描圍4000~400cm-1,底物和產品的紅外光譜圖見附圖2,在波數為3316±4,、2946±4、1659±4、1540±4、1092±4、799±4、583±4、463±4處有紅外特征吸收峰。
對實施例3制備的磁性combi-cleas進行粉末x衍射(xrd)分析
使用普析xd-2x-ray衍射儀測定樣品晶體衍射峰,測試條件:cu靶
對實施例3制備的磁性combi-cleas進行熱重分析(tga)
使用mettler1100sf系統測定生物催化劑的酶負載量。將約2mg樣品置于鋁鍋中,按20ml/min通入氮氣,加熱速度為15℃/min,掃描范圍為30-600℃。tga分析結果見附圖4。根據失重計算,生物催化劑酶負載量為8.77%。
實驗中發現,沉淀劑的種類、戊二醛濃度及聯合交聯固定qnr和gdh的時間對combi-cleas酶活性均有不同程度的影響。
參照實施例3的制備方法,考察不同種類沉淀劑(乙醇、異丙醇、丙酮、飽和硫酸銨、乙腈)對combi-cleas酶活性的影響,結果見表1。
表1不同沉淀劑對combi-cleas酶活性的影響
使用有機溶劑做沉淀劑,酶活性回收率低。當用飽和硫酸銨為沉淀劑時,qnr和gdh的活性回收率分別為104.0±0.7%和98.1±1.9%,對酶活性影響最小,活性回收率最高。本發明優選的沉淀劑為飽和硫酸銨。
參照實施例3的制備方法,考察戊二醛濃度對combi-cleas酶活性的影響,結果見表2。
表2不同戊二醛濃度對combi-cleas酶活性的影響
隨戊二醛濃度增大,酶活性回收率增加。當濃度達到40mm時,qnr和gdh的活性回收率最高,超過40mm時,活性回收率有減小趨勢。本發明優選的交聯劑濃度為40mm。
參照實施例3的制備方法,考察交聯時間(加入戊二醛后的反應時間)對combi-cleas酶活性的影響,考察結果見表3。
表3不同交聯時間對combi-cleas酶活性的影響
戊二醛濃度為40mm,qnr和gdh的活性回收率隨交聯時間延長而增大,交聯時間為8小時,qnr和gdh的活性回收率最高。本發明優選的交聯時間為8小時。
實施例4
磁性combi-cleas催化不對稱合成(r)-3-奎寧醇:
取50mg磁性combi-cleas分散在含有:5mm3-奎寧酮、9mm葡萄糖、0.05mmnad+和0.05mmnadh的pbs中,總體積10ml。在20℃,ph7.5-8.0,以轉速150r/min攪拌。選用流動相為v二氯甲烷/v甲醇=9/1,通過tlc監控反應,生物轉化時間為2h。反應完成后,磁性分離回收催化劑。上清液用高濃度naoh調節至ph值大于12,然后在80℃減壓濃縮至總體積的1/4。加入等體積的正丁醇抽提3次,收集有機相,減壓濃縮蒸干。在90℃,用甲苯溶解固體,難溶物趁熱過濾,濾液冷卻,有白色針狀晶體出現,過濾,得白色固體。
對實施例4制備的白色固體進行紅外光譜、1hnmr和質譜分析
紅外光譜:1747cm-1左右的羰基特征峰消失,在3103cm-1出現羥基特征峰,表明3-奎寧酮被還原成3-奎寧醇;
1h-nmr(400mhz,dmso)分析:δ4.946(s,1h),δ3.879(q,1h),δ2.531-3.164(m,6h),δ1.392-2.014(m,5h);
mr分析:產物的理論分子量為:127.18,質譜測定為:127)。
對實施例4制備的白色固體進構型分析
用clarus580gc系統(perkinelmer,usa)測定對映體值,手性柱為(hydrodex-β-6-tbdm,25m×0.25mm×0.25μm,macherey-nagel),使用火焰離子檢測器。從60℃程序升溫至180℃,升溫速度為5℃/min,保持3min.進樣器和檢查器的溫度分別為220℃和250℃。以標準品(r)和(s)-奎寧醇做對照,測得產品的對映體值為100%,其構型r型。
實施例5
磁性combi-cleas的回收和循環再利用。
取50mg磁性combi-cleas分散在含有:5mm3-奎寧酮、9mm葡萄糖、0.05mmnad+和0.05mmnadh的pbs中,總體積10ml。在20℃,ph7.5-8.0,以轉速150r/min攪拌。tlc監控反應,反應完成后,磁性分離回收催化劑。直接用于下一次轉化。發現本發明提供的生物催化劑可循環8次,單次循環的轉化率和對映體值均為100%,結果見附圖5。循環8次以后,催化效率明顯降低。但在循環過程中,無qnr和gdh泄露。
實施例6
取實施例2制備的氨基功能化的磁性fe3o4納米顆粒4-6mg,分散在1.6-2.4ml含有qnr(4.0mg/ml)和gdh(2.0mg/ml)的磷酸鹽緩沖溶液(pbs,10mm,ph7.2-7.5)中,在4-25℃,轉速400-800r/min攪拌0.5-1.0小時。加入7-12倍體積的冰冷的沉淀劑,攪拌0.5-1.5h;加入0.8-1.2ml的戊二醛,轉速200-600r/min攪拌交聯2.0-12.0h。磁分離,pbs洗3次,得磁性combi-cleas。
使用實施例3的方法進行粉末x衍射(xrd)分析、紅外光譜分析、掃描電鏡分析及熱重分析(tga),結果顯示實施例6制備的磁性聯合交聯酶聚集體生物催化劑,在衍射角度2θ為30.5±0.2°、35.4±0.2°、44.7±0.2°、57.3±0.2°、63.4±0.2°處有衍射峰;同時在波數為3316±4,、2946±4、1659±4、1540±4、1092±4、799±4、583±4、463±4處有紅外特征吸收峰。經電鏡掃描顯示,本發明磁性聯合交聯酶聚集體生物催化劑具有凹凸不平的球形表面結構,粒徑為1.5±0.5μm;熱重分析顯示,磁性聯合交聯酶聚集體生物催化劑酶負載量高達5-15%。
實施例7
取實施例6制備的combi-cleas生物催化劑40-60mg分散在含有:4-6mm3-奎寧酮、7.2-10.8mm葡萄糖、0.04-0.06mmnad+和0.04-0.06mmnadh的pbs中,總體積8-12ml;在4-25℃,ph7.5-8.0,以轉速50-200r/min攪拌,生物轉化時間為1-3h。
使用實施例4或5的方法檢測實施例7不對稱合成(r)-3-奎寧醇的轉化效果,結果顯示,轉化率為100%,收率高達70-85%,對映體值為100%。磁性combi-cleas的回收和循環再利用過程中,無qnr和gdh泄露。
實施例8
在不經過本發明生物催化劑處理,直接用表達qnr和表達gdh的重組大腸桿菌處理實驗,以作對比。反應體系:0.1g混合濕細胞作生物催化劑,5mm3-奎寧酮,9mm葡萄糖,0.05mmnad+和0.05mmnadh,緩沖溶液b(pbs,ph7.2-7.4),總體積10ml。反應溫度25℃,以100rpm連續攪拌,反應過程中控制ph在7.5-8.0.用tlc監控反應,流動相為v二氯甲烷/v甲醇=9/1。轉化時間明顯延長(5.5h),轉化率為95%,對映體值100%,不能回收和循環利用。
本發明磁性聯合交聯酶聚集體生物催化劑用于不對稱合成(r)-3-奎寧醇,與實施例8相比,不僅能回收和循環利用,還明顯縮短反應時間,經濟價值明顯。同時本發明生物催化不對稱合成(r)-3-奎寧醇所用介質為水,有利于節約資源,環境友好,符合綠色化學和可持續發展要求。
- 還沒有人留言評論。精彩留言會獲得點贊!