一種光熱轉換納米材料負載青蒿素類藥物的復合材料及其制備方法與應用與流程
本發明涉及一種光熱轉換納米材料負載青蒿素類藥物的復合材料及其制備方法與應用,屬于新型納米材料領域。
背景技術:
光熱轉換的納米材料是一種能吸收某種光尤其是近紅外光,通過等離子體共振或者能量躍遷帶產生的熱,從而在局部導致高溫,最終殺死腫瘤細胞的功能材料,很多生物材料學者致力于合成這種材料,將它應用于光熱治療等。光熱轉換材料在生物醫學上具有很大的應用潛能。
青蒿素(ART)是從黃花蒿中提取的有效成分,為目前最有效的抗瘧疾藥物之一。近年來,青蒿素及其衍生物的抗腫瘤作用也得到了科學家的證實,其主要衍生物有雙氫青蒿素、蒿甲醚、蒿乙醚、青蒿琥酯等。青蒿素類藥物主要是通過過氧橋鍵的斷裂產生氧自由基來抑制腫瘤細胞的生長。
技術實現要素:
本發明的目的是提供一種光熱轉換納米材料負載青蒿素類藥物的復合材料及其制備方法與應用,本發明復合材料能顯著增強抑制腫瘤細胞生長的效果。
本發明提供的復合材料,它包括光熱轉換納米材料負載的青蒿素類藥物后形成的復合物。
上述的復合材料中,所述光熱轉換納米材料為含有金屬離子的納米材料;
所述青蒿素類藥物為青蒿素、雙氫青蒿素、蒿甲醚、蒿乙醚和青蒿琥酯中的至少一種。
上述的復合材料中,所述青蒿素類藥物與所述光熱轉換納米材料的摩爾質量比可為0.0010~0.0220:1,具體可為0.00354:1、0.0010~0.00354:1、0.00354~0.0220:1、0.0020~0.0120:1或0.0015~0.0200:1。
上述的復合材料中,所述含有金屬離子的納米材料的粒徑為10nm~999nm,具體可為10nm、100nm、10nm~100nm或10nm~500nm;
所述含有金屬離子的納米材料中的金屬離子選自Fe3+、Fe2+、Co3+、Ni3+、Mn3+、Mn4+和Cu2+中的至少一種;
所述含有金屬離子的納米材料中的金屬離子的摩爾分數為0~100%,但不包括0和100%。
本發明中,所述含有金屬離子的光熱轉換納米材料可通過常規方法制備得到,如:固相法、液相法或氣相法等。
上述的復合材料中,所述含有金屬離子的納米材料為所述金屬離子的氧化物、氫氧化物、硫化物以及絡合物中的至少一種;
所述復合材料還包括負載材料,所述負載材料負載所述光熱轉換納米材料和所述青蒿素類藥物;所述負載材料與所述光熱轉換納米材料的摩爾比可為0.1~1.0:1,具體可為0.5:1、0.1~0.5:1、0.5~1.0:1或0.2~0.8:1;
所述負載材料具體包括多孔UCNP、介孔UCNP、多孔硅和介孔硅中的至少一種。
本發明中,所述光熱轉換納米材料為具體可為Mn3O4納米顆粒、Fe3O4納米顆粒和鐵卟啉中的至少一種。
本發明還提供了上述的復合材料的制備方法,包括如下步驟:將所述光熱轉換納米材料的水溶液和青蒿素類藥物溶液混合后結合,使所述光熱轉換納米材料負載上所述青蒿素類藥物,即得到所述復合材料。
上述的制備方法中,所述結合的形式為包覆、靜電吸附、多孔吸附和中空負載中的至少一種;
所述方法中,還包括加入所述負載材料混合的步驟。
上述的制備方法中,所述青蒿素類藥物溶液為所述青蒿素類藥物溶于乙醇的溶液;
所述光熱轉換納米材料的水溶液的濃度為1~15mmol·mL-1,具體可為10mmol·mL-1、1~10mmol·mL-1、10~15mmol·mL-1或5~12mmol·mL-1;
所述青蒿素類藥物溶液的濃度為0~0.05mmol·mL-1,具體可為0.0354mmol·mL-1、0~0.0354mmol·mL-1、0.0354~0.05mmol·mL-1或0.01~0.04mmol·mL-1;
所述負載材料的水溶液的濃度為1~10mg·mL-1,具體可為5mg·mL-1、1~5mg·mL-1、5~10mg·mL-1或2~8mg·mL-1。
本發明進一步提供了所述的復合材料在制備抑制腫瘤的藥物中的應用。
上述的應用中,所述腫瘤包括結腸腫瘤、肝部腫瘤和肺部腫瘤中的至少一種。
使用本發明復合材料治療腫瘤時,為了降解部分所述光熱轉換納米材料,需要還原性物質的參與,使部分降解的所述光熱轉換材料中游離的金屬離子促進青蒿素類藥物過氧橋鍵的斷裂,協同青蒿素發揮化學治療的作用使最終的抑制腫瘤細胞生長效果大大增強;
其中還原性物質為可與所述光熱轉換納米材料反應的離子或化合物,具體可為:氫離子、谷胱甘肽和抗壞血酸中的至少一種;本發明復合材料在體內使用時,體內都含有上述原性物質;如果離體使用,則需要加入上述原性物質。
本發明具有以下優點:
本發明運用含有金屬離子的光熱轉換納米材料與青蒿素類藥物的復合能實現抑制腫瘤生長的顯著增強的效果。與現有技術相比,本發明所提供的光熱轉換納米復合材料為新型光熱轉換納米材料,使部分降解的光熱轉換材料中游離的金屬離子促進青蒿素類藥物過氧橋鍵的斷裂,協同青蒿素類藥物發揮化學治療的作用,可以使得抑制腫瘤生長的效果顯著增強。
附圖說明
圖1為實施例1中的Mn3O4納米顆粒溶液的TEM圖。
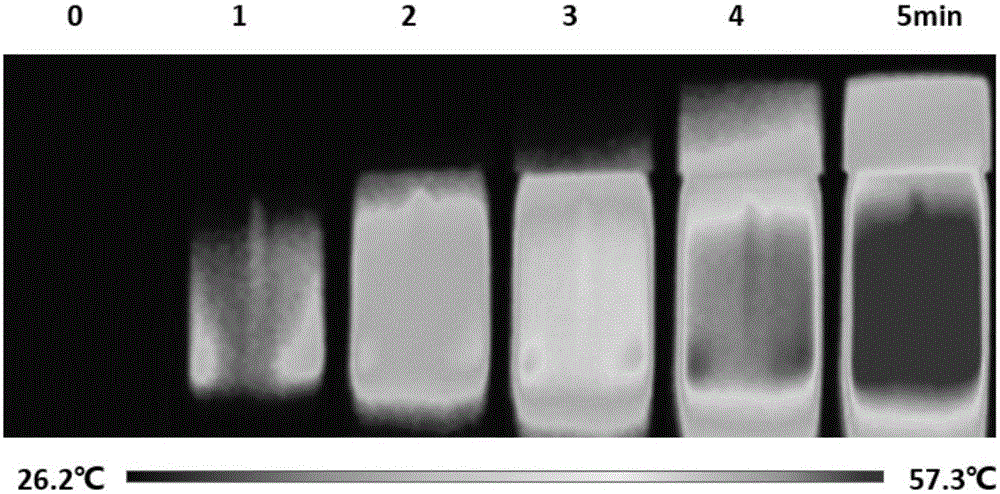
圖2為本發明實施例1中的Mn3O4納米顆粒溶液的光熱溫度變化圖。
圖3為本發明實施例1中的ART、Mn3O4和Mn3O4-ART的細胞毒性實驗圖(MTT)。
圖4為本發明實施例2中的Fe3O4納米顆粒溶液的TEM圖。
圖5為本發明實施例2中的Fe3O4納米顆粒溶液的光熱溫度變化圖。
圖6為本發明實施例2中的ART、Fe3O4和Fe3O4-ART的細胞毒性實驗圖(MTT)。
圖7為本發明實施例3中同時負載鐵卟啉和青蒿素的納米顆粒的透射電鏡圖(TEM)。
圖8為本發明實施例3中負載鐵卟啉的多孔納米顆粒溶液的光熱溫度變化。
圖9為本發明實施例3中的僅負載鐵卟啉、僅負載青蒿素(ART)和同時負載鐵卟啉與青蒿素的納米顆粒的細胞毒性實驗圖(MTT)。
具體實施方式
下述實施例中所使用的實驗方法如無特殊說明,均為常規方法。
下述實施例中所用的材料、試劑等,如無特殊說明,均可從商業途徑得到。
下述實施例中所用的Mn3O4納米顆粒是按照如下方法制備得到:
1)在敞開體系中將1mmol的Mn(CH3COO)2、2mmol的油酸(OA)和10mmol的油胺(OM)溶解于15mL的二甲苯溶液中,攪拌并緩慢加熱至90℃,然后在劇烈攪拌下加入1mL去離子水,使溶液在90℃陳化3h。反應結束后,自然冷卻至室溫,用適量的乙醇進行沉淀,離心洗滌,去除上清液得到固體產物;向固體中加入適量環己烷溶液后超聲分散,再加入適量乙醇后,再離心分離,去掉上清液;重復以上步驟,繼續用環己烷和乙醇洗滌幾次后,即可得到油溶性Mn3O4納米顆粒。
2)將油溶性Mn3O4納米顆粒溶液與NOBF4以質量比1:1混合超聲處理,處理的溫度為20℃,時間為5min,洗去表面的油溶性配體,然后分別用CH2Cl2和無水乙醇洗滌兩遍,得到Mn3O4納米顆粒(納米顆粒,直徑為10-20nm),其中,Mn3O4納米顆粒中Mn2+和Mn3+的質量分數為72.05%。
下述實施例中所用的Fe3O4納米顆粒是按照如下方法制備得到:
準確稱量3.3g的FeCl3·6(H2O),1.5g的檸檬酸鈉,6.0g CH3COONa3(H2O),溶解于100mL的乙二醇并通過攪拌至溶液黃色澄清液體,然后將其轉入高溫高壓反應釜中,加熱至200℃,時間為10h。冷卻至室溫后,將黑色的沉淀物分別用去離子水和乙醇洗滌三次后,即得到Fe3O4納米顆粒。將制備好的Fe3O4納米顆粒分散于去離子水中,其中,Fe3O4納米顆粒中的Fe2+和Fe3+的質量分數是72.36%。
實施例1、Mn3O4納米顆粒負載青蒿素(ART)的復合材料
首先,記錄10mmol·mL-1的Mn3O4納米顆粒溶液的透射電鏡圖(TEM),并測量其在808nm激光照射下5分鐘的升溫情況。將1mL 10mmol·mL-1的Mn3O4納米顆粒水溶液用PEG修飾后與1mL 0.0354mmol·mL-1的青蒿素(ART)的乙醇溶液攪拌混合30min,靜電吸附結合,用去離子水離心洗滌,即得到Mn3O4納米顆粒負載青蒿素(ART)的復合材料(簡稱Mn3O4-ART復合材料),記錄混合液的透射電鏡圖(TEM)。分別將Mn3O4、青蒿素(ART)和Mn3O4負載青蒿素的復合材料(Mn3O4-ART)做MTT測試。
圖1為Mn3O4納米顆粒的TEM圖,從圖1可得知:Mn3O4納米顆粒的尺寸約為10nm;圖2為Mn3O4納米顆粒溶液的光熱溫度變化,從圖2中可得知:Mn3O4納米顆粒溶液在808nm激光下照射5分鐘后可升高約31.1℃。圖3為Mn3O4、ART和Mn3O4-ART的細胞毒性實驗圖(MTT),從圖3可知三種納米材料對于癌細胞都有抑制生長的作用,而本發明Mn3O4-ART復合材料的抑制效果最為明顯。
實施例2、Fe3O4納米顆粒負載青蒿素(ART)的復合材料
首先,記錄10mmol·mL-1的Fe3O4納米顆粒溶液的透射電鏡圖(TEM),并測量其在808nm激光照射下5分鐘的升溫情況。將1mL 10mmol·mL-1的Fe3O4納米顆粒水溶液用PEG修飾后與1mL0.0354mmol·mL-1的青蒿素(ART)的乙醇溶液攪拌混合30min,靜電吸附結合,用去離子水離心洗滌,即得到Fe3O4納米顆粒負載青蒿素(ART)的復合材料(簡稱Fe3O4-ART復合材料),記錄混合液的透射電鏡圖(TEM)。分別將Fe3O4、青蒿素(ART)和Fe3O4負載青蒿素的復合材料(Fe3O4-ART)做MTT測試。
圖4為Fe3O4納米顆粒的TEM圖,從圖4可得知:Fe3O4納米顆粒的尺寸約為100nm;圖5為Fe3O4納米顆粒溶液的光熱溫度變化,從圖5中可得知:Fe3O4納米顆粒溶液在785nm激光下照射5分鐘后可升高約25.1℃。圖6為Fe3O4、ART和Fe3O4-ART的細胞毒性實驗圖(MTT),從圖6可知三種納米材料對于癌細胞都有抑制生長的作用,而本發明Fe3O4-ART復合材料的抑制效果最為明顯。
實施例3、鐵卟啉負載青蒿素(ART)的復合材料
首先,將1mL 10mmol·mL-1鐵卟啉負載于1mL 5mmol·mL-1多孔的納米顆粒(多孔UCNP的水溶液)上,記錄負載鐵卟啉的多孔納米顆粒的透射電鏡圖(TEM),并測量10mmol·mL-1納米顆粒在750nm激光照射下5分鐘的升溫情況。將1mL0.0354mmol·mL-1的青蒿素(ART)負載于已負載過鐵卟啉的多孔納米顆粒上,即得到鐵卟啉負載青蒿素(ART)的復合材料(又稱同時負載鐵卟啉與青蒿素(ART)的納米顆粒),記錄負載鐵卟啉和青蒿素的多孔納米顆粒的透射電鏡圖(TEM)。分別將僅負載鐵卟啉、僅負載青蒿素(ART)和同時負載鐵卟啉與青蒿素的納米顆粒做MTT測試。
圖7為同時負載鐵卟啉和青蒿素的納米顆粒的透射電鏡圖(TEM),從圖7可得知:尺寸約為30nm;圖8為負載鐵卟啉的多孔納米顆粒溶液的光熱溫度變化,從圖8中可得知:負載鐵卟啉的多孔納米顆粒溶液在750nm激光下照射5分鐘后可升高約30.7℃。圖9為分別將僅負載鐵卟啉、僅負載青蒿素(ART)和同時負載鐵卟啉與青蒿素的納米顆粒的細胞毒性實驗圖(MTT),從圖9可知三種材料對于癌細胞都有抑制生長的作用,而同時負載鐵卟啉與青蒿素(ART)的納米顆粒的抑制效果最為明顯。
- 還沒有人留言評論。精彩留言會獲得點贊!