一種攜載抗腫瘤藥物連接CD22單抗靶向淋巴瘤的血小板靶向載藥體系的制備方法與流程
本發明屬于生物藥物載體制備領域,尤其涉及一種以連接cd22單抗靶向淋巴瘤細胞的血小板作為靶向藥物載體攜載抗腫瘤藥物的制備方法。
背景技術:
惡性淋巴瘤是一組原發于淋巴組織的惡性腫瘤,按病理和臨床特點可分為兩大類:霍奇金淋巴瘤(hl)和非霍奇金淋巴瘤(nhl),后者占90%以上。nhl發病率近年來急劇增加,其中,b細胞淋巴瘤是與惡性b細胞單克隆擴增相關的一組異質性腫瘤,約占成人nhl的85%。高度異質性血液惡性腫瘤的b細胞淋巴瘤表現出不同的臨床和生物學特征。盡管治療反應有所進展,但高水平b細胞nhl的5年生存率低于50%,化療依然是b細胞淋巴瘤的一線治療。但是化療具有明顯的副作用,包括骨髓抑制、免疫功能低下、消化道反應等,提高藥物的靶向性、降低治療的毒副作用成為目前淋巴瘤診治的挑戰,所以研究和開發能將抗淋巴瘤藥物靶向傳遞到腫瘤細胞內部或周圍以期較少副反應的藥物載體具有十分重要的意義。
目前而言,藥物載體主要包括磁性納米藥物載體、脂質體載體、微粒載體等,但它們均存在諸多缺點,如載藥率不高,穩定性較差,毒性作用較強等,因而生物藥物載體憑借其良好的生物相容性、緩控釋藥等特點在眾多載藥體系中脫穎而出。
以生物作為藥物載體的研究已進行了很多年,研究較為深入的包括白蛋白載藥和紅細胞載藥等。臨床上應用成功的典型范例是以人血清白蛋白為載體的紫杉醇產品,研究顯示其可在腫瘤細胞和組織中蓄積,可用于治療乳腺癌、卵巢癌等。另外的研究顯示,經紅細胞包載后釋放的甲氨蝶呤和長春新堿等藥物,抑制腫瘤生長及誘導其凋亡的效果較裸藥更為顯著。
血小板是從骨髓成熟的巨核細胞脫落下來的碎片,直徑約2um,在成人血液中數量約為(1-3)×1011個/l,其壽命約7-14天,平均9天,衰老的血小板大多被肝臟中的kupfer細胞清除,因而血小板具有良好的生物相容性、安全性及較長的血循環時間。血小板在止血、愈合傷口、血栓形成等過程中起著重要作用,并且與腫瘤的發生發展也具有密切的關系。腫瘤細胞經過一系列反應活化血小板,活化的血小板通過腫瘤細胞誘導的血小板聚集(tcipa)作用聚集在腫瘤細胞周圍,形成血小板-腫瘤細胞復合物,正是這種作用促進了血小板與腫瘤細胞的粘附,并且活化后的血小板將攝取的藥物釋放,而血小板攝取藥物及小顆粒的作用與巨噬系統的吞噬作用不同,即不會將內吞的物質殺死和清除,從而保證了藥物原有的結構和活性,保留了藥效。另外研究顯示,血小板的載藥率遠高于納米顆粒的載藥率,且血小板與細胞毒藥物具有協同作用,可以增加其殺傷作用。
然而血小板的特異性和精確靶向的挑戰限制了它們作為藥物載體的功效。相比之下,單克隆抗體(mab)是高度特異性和精確的靶向系統。結合了藥物的腫瘤特異性抗體可以將藥物引導到腫瘤細胞,證明其可能用于靶向藥物遞送。由于90%以上的b細胞淋巴瘤細胞上有cd22抗原表達,且cd22抗原的表達率為80%-100%,遠高于正常成熟b淋巴細胞,并且結合cd22的抗體可以被迅速內化,cd22作為化學免疫偶聯物也因此引起了特別注意,被用于將細胞毒性藥物靶向遞送至腫瘤細胞。
因此,在這項工作中,我們建議使用連接cd22單抗的血小板作為治療b細胞淋巴瘤的新型藥物靶向遞送系統,其具有含量豐富、生物相容性好、載藥率高、主動靶向性好、對腫瘤細胞療效高而對正常組織損害小的優勢,這方面目前還沒有相關的研究報導。
技術實現要素:
為克服現有技術的不足,本發明的目的在于提供一種以連接cd22單抗的血小板作為藥物載體包載抗腫瘤藥物的制備方法,制成攜載抗腫瘤藥物連接cd22單抗的血小板靶向載藥體系,具有生物相容性好、載藥率高、主動靶向性強、在腫瘤組織的酸性環境中釋放率高,從而增加藥物的抗腫瘤活性等優點。
為達到上述目的,本發明是通過以下的技術方案來實現的。
一種攜載抗腫瘤藥物連接cd22單抗靶向淋巴瘤的血小板靶向載藥體系的制備方法,包括以下步驟:
(1)環境溫度為20±5℃,在全血中加入重量百分含量為2-4%檸檬酸鈉溶液,離心后得到血小板豐富血漿;
(2)將步驟(1)得到的血小板豐富血漿再深度離心,并用pbs緩沖液洗滌至不再含有血漿及其他血液成分,得到洗滌血小板;
(3)將步驟(2)得到的洗滌血小板與3-馬來酰亞胺基苯甲酸-n-羥基琥珀酰亞胺酯試劑(mbs)試劑在37±0.5℃的避光環境中震蕩反應1~2小時,離心洗滌,得到表面修飾(馬來酰亞胺基團)指向巰基的血小板。
(4)將抗cd22單抗與traut’s試劑在37±0.5℃的避光環境中震蕩反應1~2小時,然后超濾離心,得到富含巰基的抗cd22單抗。
(5)將步驟(3)得到的表面修飾為指向巰基的馬來酰亞胺基團的血小板與步驟(4)得到的富含巰基的抗cd22單抗混合,在37±0.5℃的避光環境中震蕩反應8~12小時,經離心洗滌,得到連接cd22單抗的血小板。
(6)將步驟(5)得到的連接cd22單抗的血小板與抗腫瘤藥物在37±0.5℃的避光環境中震蕩反應1~2小時,得到抗腫瘤藥物與連接cd22單抗的血小板反應物。
(7)將步驟(6)得到的抗腫瘤藥物與連接cd22單抗的血小板反應物通過瓊脂糖凝膠2b分離柱分離,并離心洗滌,得到攜載抗腫瘤藥物連結cd22單抗的血小板靶向載藥體系。
所述步驟(1)中,全血與重量百分含量為2-4%檸檬酸鈉溶液的體積比為7:1~10:1,優選為9:1。
所述步驟(1)中離心為以1200rpm離心5~10min。
所述步驟(2)中深度離心為以3600rpm離心8~12min。
所述步驟(2)得到洗滌血小板計數控制在(2.5-3.0)×105/ul。
所述步驟(3)中洗滌血小板與mbs試劑體積比為50:1。
所述步驟(3)中離心洗滌是用pbs緩沖液以3600rpm離心洗滌2~3次,每次5~8分鐘。
所述步驟(4)中抗cd22單抗濃度為1mg/ml。
所述步驟(4)中抗cd22單抗與traut’s試劑的濃度比為50:1。
所述步驟(4)中超濾離心是于超濾離心管中3300rpm離心過濾20~30min。
所述步驟(5)中離心洗滌是用pbs緩沖液以3600rpm離心洗滌2~3次,每次5~8min。
所述步驟(6)中抗腫瘤藥物為蒽環類抗腫瘤藥物或烷化劑類抗腫瘤藥物的一種,抗腫瘤藥物的濃度為0.05~0.15mmol/l。
所述蒽環類抗腫瘤藥物優選柔紅霉素,烷化劑類抗腫瘤藥物優選環磷酰胺。
所述步驟(6)中抗腫瘤藥物與洗滌血小板的體積比為1~4:1,優選為2:1。
所述步驟(7)中離心洗滌是用pbs緩沖液以3600rpm離心洗滌2~3次,每次5~8min。
有益效果:與現有技術相比,本發明的優點在于:
(1)本發明將連接cd22單抗的血小板作為靶向生物載藥系統,包載某些常見抗腫瘤藥物應用于淋巴瘤的化學治療中。血小板作為機體的一部分,具有良好的生物相容性,包載藥物后不會引起免疫排斥反應,避免了作為外來物的納米載藥系統存在的排斥反應問題,可使攜載的化療藥物血循環時間延長;同時血小板的含量豐富,其裝載藥物的量遠遠高于納米載體。
(2)通過將化療藥物包載于連接cd22單抗的血小板中,由于cd22單抗有主動靶向遞送作用,實現了將藥物選擇性釋放于特定部位的目的,提高了藥物對腫瘤組織的靶向性,從而增加了藥物對腫瘤組織的療效而減少了其對正常組織的損害,同時以較少的藥物劑量即可達到相同的抗腫瘤作用,有效的減輕了藥物副作用。這些都對提高患者生活質量和醫療質量具有重要意義,并且具有一定的社會和經濟效益,具有廣闊的應用前景。
附圖說明
圖1為本發明制備的攜載柔紅霉素連接cd22單抗的血小板靶向載藥體系的蛋白電泳考馬斯亮藍染色結果;其中第一泳道為單純的血小板,第二泳道為攜載柔紅霉素的血小板,第三泳道為攜載柔紅霉素連接cd22單抗的血小板,第四泳道為單純的抗cd22單抗。
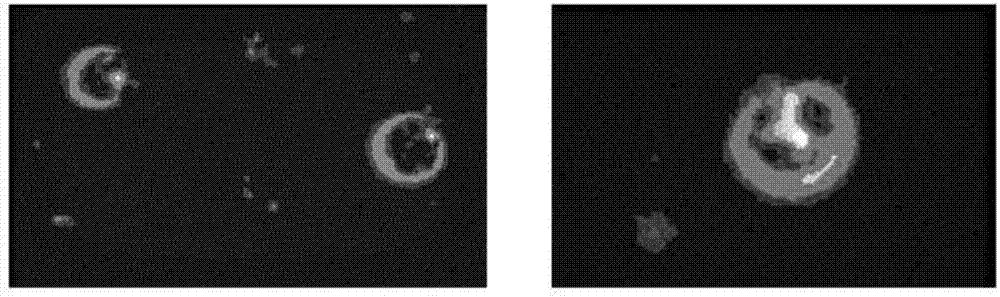
圖2為本發明制備的攜載柔紅霉素連接cd22單抗的血小板靶向載藥體系的熒光顯微鏡圖像;其中左圖為單純的血小板、右圖為連接cd22單抗的血小板攜載了柔紅霉素。
圖3為單獨血小板和連接cd22單抗的血小板攜載柔紅霉素后的掃描電鏡圖像;其中左圖為單純的血小板、右圖為連接cd22單抗的血小板攜載了柔紅霉素。
圖4為連接cd22單抗的血小板載柔紅霉素的藥物體外釋放曲線。
具體實施方式
下面結合附圖對本發明作進一步的詳細說明。
實施例1
一種攜載柔紅霉素連接cd22單抗的血小板靶向載藥體系的制備方法,該方法包括如下步驟:
第一步:在環境溫度為20±5℃的室溫條件下,在取得的全血中加入重量百分比為3.2%檸檬酸鈉溶液抗凝,全血與檸檬酸鈉溶液的體積比為9:1,1200rpm離心5min后得到血小板豐富血漿;
第二步:血小板豐富血漿以3600rpm離心10min,并用pbs緩沖液洗滌三次,使其不再含有血漿及其他血液成分,棄去上清,得到洗滌血小板,控制血小板計數為(2.5-3.0)×105/ul。
第三步:將洗滌血小板500μl的重懸液與10μlmbs試劑在37±0.5℃的避光環境中震蕩反應1小時,3600rpm離心洗滌3次,每次8分鐘,得到表面修飾(馬來酰亞胺基團)指向巰基的血小板;將抗cd22單抗與traut’s試劑以濃度比50:1混合,在37±0.5℃的避光環境中震蕩反應1小時,然后3300rpm超濾離心20min,得到抗富含巰基的cd22單抗。
第四步:將表面修飾(馬來酰亞胺基團)指向巰基的血小板與富含巰基的抗cd22單抗混合,在37±0.5℃的避光環境中震蕩反應8小時,并以3600rpm,8min離心洗滌3次,得到連接cd22單抗具有靶向淋巴瘤細胞功能的血小板。
第五步:將0.1mmol/l的柔紅霉素與制得的連結cd22單抗的血小板混合,柔紅霉素與血小板的體積比為2:1,輕輕將其吹打至混合均勻。將混合物在37±0.5℃的避光環境中以100rpm震蕩反應1小時,然后通過瓊脂糖凝膠2b分離柱分離,再用pbs緩沖液以3600rmp離心洗滌3次,每次8分鐘,即得到新型攜載柔紅霉素連接cd22單抗的血小板靶向載藥體系。
采用上述方法制備出的攜載柔紅霉素的血小板靶向載藥體系,通過蛋白電泳考馬斯亮藍染色、熒光顯微鏡和掃描電鏡進行表征,結果表明抗cd22單抗成功連接于血小板上、柔紅霉素可被包載于血小板內且未影響血小板的形態,如圖1、圖2、圖3所示。采用高效液相色譜法計算得到其包封率和包載率分別為61.3%和83.4%,表明藥物的包封率及包載率均較高。通過觀察不同ph環境中藥物的釋放率,證明酸性環境中藥物的釋放率明顯增加如圖4所示,表明血小板載藥體系可減少細胞毒藥物在正常細胞、組織的釋放,從而降低化療藥物的毒副作用。
下面通過試驗對本實施例的有益效果作進一步的詳細說明。
1、蛋白電泳考馬斯亮藍染色結果證明了抗cd22單抗成功連接于血小板載藥體系,如圖1所示。由于柔紅霉素具有自發熒光性,通過熒光顯微鏡觀察靶向血小板載藥體系,可見藥物被包載于血小板內如圖2所示,通過高效液相色譜法定量計算其載藥率和包封率,分別為46.3%和86.6%,表明靶向血小板載藥體系對蒽環類抗腫瘤藥物具有較高的包載及包封率。通過掃描電鏡,發現載藥后的血小板形態與單純的血小板形態相似,無明顯改變如圖3所示,說明藥物不會對血小板造成明顯影響,另外通過cck-8法檢測到單純的血小板對腫瘤細胞無明顯影響,提示血小板可作為安全、高效的藥物載體。
2、本發明制備的攜載柔紅霉素連接cd22單抗的血小板靶向載體,藥物釋放曲線結果顯示由靶向血小板包載的藥物在腫瘤組織的酸性環境中釋放較多且具有緩釋作用,而在中性和堿性環境中的釋放明顯減少如圖4所示,因此降低了化療藥物對機體的毒副作用,并延長了藥物在體內的半衰期。
3、cck-8實驗結果顯示:與裸藥相比,攜載柔紅霉素的血小板載藥體系和攜載柔紅霉素連接cd22單抗的血小板靶向載藥體系體外作用于人類淋巴瘤細胞株raji細胞株后,對細胞生長的抑制作用更加明顯;并且后者抑制效果更顯著。
4、通過流式細胞術和dapi染色,發現與裸藥相比,攜載柔紅霉素的血小板載藥體系和攜載柔紅霉素連接cd22單抗的血小板靶向載藥體系體可促進raji細胞的凋亡,且后者效果更顯著。并且用流式細胞術檢測到血小板靶向載藥體系顯著增加了腫瘤細胞內的藥物濃度,從某種程度上解釋了由血小板攜載后的柔紅霉素抗腫瘤作用增加的原因。
實施例2
一種攜載環磷酰胺連接cd22單抗的血小板載藥體系的制備方法,該方法包括如下步驟:
第一步:在環境溫度為20±5℃的室溫條件下,在取得的全血中加入重量百分比為4%檸檬酸鈉溶液抗凝,全血與檸檬酸鈉溶液的體積比為10:1,1200rpm離心8min后得到血小板豐富血漿;
第二步:血小板豐富血漿以3600rpm離心12min,并用pbs緩沖液洗滌三次,使其不再含有血漿及其他血液成分,棄去上清,得到洗滌血小板,控制血小板計數為(2.5-3.0)×105/ul。
第三步:將洗滌血小板500μl的重懸液與10μlmbs試劑在37±0.5℃的避光環境中震蕩反應1.5小時,3600rpm離心洗滌2次,每次6分鐘,得到表面修飾(馬來酰亞胺基團)指向巰基的血小板;將抗cd22單抗與traut’s試劑以濃度比50:1混合,在37±0.5℃的避光環境中震蕩反應1.5小時,然后3300rpm超濾離心30min,得到抗富含巰基的cd22單抗。
第四步:將表面修飾(馬來酰亞胺基團)指向巰基的血小板與富含巰基的抗cd22單抗混合,在37±0.5℃的避光環境中震蕩反應12小時,并以3600rpm,6min離心洗滌2次,得到連接cd22單抗具有主動靶向淋巴瘤細胞功能的血小板。
第五步:將0.05mmol/l的環磷酰胺與制得的連接cd22單抗的血小板混合,環磷酰胺與血小板的體積比為2:1,輕輕將其吹打至混合均勻。將混合物在37±0.5℃的避光環境中以100rpm震蕩反應1.5小時,然后通過瓊脂糖凝膠2b分離柱分離,再用pbs緩沖液以3600rmp離心洗滌2次,每次6分鐘,即得到新型攜載環磷酰胺連接cd22單抗的血小板靶向載藥體系。
通過高效液相色譜法定量計算其包封率和包載率,分別為41.3±3.4%和82.4±2.7%,表明血小板靶向載藥體系對烷化劑類抗腫瘤藥物具有較高的包封及包載率。
本發明按照上述實施例進行了說明,應當理解,上述實施例不以任何形式限定本發明,凡采用等同替換或等效變換方式所獲得的技術方案,均落在本發明的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!