一種治療腫瘤的藥物組合的制作方法
本發明涉及一種治療腫瘤的藥物組合,屬于基因修飾細胞及腫瘤治療技術領域。
背景技術:
原發性肝癌(hepatocellularcarcinoma,簡稱:hcc)居惡性腫瘤發病率的第五位,全球每年死亡人數約100萬。目前,大部分原發性肝癌患者缺乏有效的治療手段,總的生存率僅為3%-5%。肝移植雖已成為治療原發性肝癌的重要手段,但供體短缺、手術損傷、免疫排斥以及費用高昂等問題構成了肝臟器官移植技術發展的主要障礙。因此,有必要探索一種新的、有效治療途徑。隨著分子生物學、基因工程技術及免疫學的飛速發展,以免疫治療為基礎的生物治療已顯示出良好的應用前景。
近年來,嵌合抗原受體(chimericantigenreceptor,car)修飾細胞為基礎的腫瘤過繼免疫治療取得重大進展。修飾后的細胞不僅具有向腫瘤細胞的殺傷能力,且可克服腫瘤局部免疫抑制微環境和打破宿主免疫耐受的狀態。car的結構一般包括識別腫瘤表面抗原的單鏈抗體(scfv)、跨膜區以及細胞胞內的活化增殖信號域。表達car的t細胞可通過scfv直接識別并結合腫瘤細胞表面的腫瘤相關抗原,car將信號傳入t細胞內,激活t細胞分泌細胞因子包括穿孔素、顆粒酶、inf-γ、tnf-α等,從而發揮殺傷腫瘤細胞的作用。因此,car-t細胞是mhc非限制性的,其應用的關鍵是確定一種腫瘤相關抗原,在腫瘤細胞表面高表達,而在正常組織中無表達或者低表達。
甲胎蛋白(alpha-fetoprotein,簡稱:afp)是胎兒時期肝臟內合成的一種糖蛋白,成人后血清中水平很低,發生惡變的肝細胞則又可恢復其合成的能力,其在70%-80%的原發性肝癌(hcc)中有較高的表達水平。研究證實將表達mafp基因的小鼠肝癌細胞株hepa1-6接種c57bl/6j小鼠,再用插入afp基因的質粒dna免疫小鼠,結果發現這種治療性的免疫afp質粒dna能誘發較強的特異性ctl免疫反應。還有研究應用afp來源的免疫優勢多肽疫苗治療iv期hcc患者,6例患者中5例顯示afp多肽在體內具有免疫原性,能在血清afp水平較高的患者中刺激抗原特異性t細胞。因此,afp作為肝癌細胞的特異性抗原,可作為car-t細胞抗腫瘤治療的一個理想靶點。
間充質干細胞(mesenchymalstemcells,簡稱:mscs)是來自于中胚層,并且可以向三個胚層分化的一類干細胞,在組織工程等方面有廣泛的用途,是國內外廣泛關注的一類細胞。目前從臍帶的不同的組織部位都獲得了間充質干細胞,而其主要來源是血管間的華通膠基質。與骨髓間充質干細胞相比,人臍帶間充質干細胞(humanumbilicalcordmesenchymalstemcells,簡稱:hucmscs)以其易得、原始、增殖力強、免疫原性低、不涉及法律倫理等優勢而越來越受到人們的重視。
肝細胞生長因子(hepatocytegrowthfactor,簡稱:hgf)是一種肝細胞特有的血小板衍生促有絲分裂劑,可通過多個信號通路促進細胞增殖,并能促使原代培養肝細胞dna合成和細胞分裂,并且作為一種可以誘導上皮細胞分散(細胞離散和運動)的成纖維細胞衍生因子,能誘導細胞增殖、分散、遷移、器官形態形成、血管發生等一系列生物效應,對組織修復和胚胎發育起重要作用。
技術實現要素:
本發明提供一種治療腫瘤的藥物組合,以antiafpcar-t細胞對腫瘤進行特異性識別以及殺傷,聯合msc-hgf增強人體免疫功能并促進組織再生修復,從而達到在一定程度上強殺傷腫瘤細胞的效果以應用于相應腫瘤疾病的預防和治療。
本發明提供一種治療腫瘤的細藥物合,包括antiafpcar-t細胞,和人源肝細胞生長因子過表達的人臍帶間充質干細胞msc-hgf。
在本申請的方案中,所述antiafpcar-t細胞和msc-hgf,二者作為整體稱作本發明的治療腫瘤的藥物組合,該治療腫瘤的藥物組合在施用過程中,antiafpcar-t細胞用于對腫瘤細胞進行特異性識別以及殺傷,msc-hgf用于增強人體免疫功能并促進組織再生修復。
本發明的治療腫瘤的藥物組合是一種生物制劑,可以以注射制劑的形式實施具體治療方式,例如將其用生理鹽水懸浮后制成注射液的形式對患者進行注射。
在本發明所提供的方案中,腫瘤為肝腫瘤。
在本發明所提供的方案中,所述antiafpcar-t細胞在t細胞內表達scfv–igd–cd28–ox40–cd3ζ融合蛋白;所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述scfv用于結合所述afp蛋白,并且所述scfv的氨基酸序列為所述scfv–igd–cd28–ox40–cd3ζ融合蛋白的第一序列,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白的第一序列為:
evqlvqsgaevkkpgesltisckasgysfpnywitwvrqmsggglewmgridpgdsyyttynpsfqghvtisidkstntaylhwnslaasdtamyycaryyvslvdiwgqgtlvtvssggggsggggsggggsqsvltqpakvsgspgqkitisctgtssdvggynyvswyqqhpgkapklmiydvnnrpsevsnrfsgaksgntasltisglqaedeadyycssyttgsrsvfgggtkltvlg
該antiafpcar-t細胞以afp為靶點,具體地,所述antiafpcar-t細胞的嵌合抗原受體car包括胞膜外抗原結合區、鉸鏈區和胞內信號傳導區,所述胞膜外抗原結合區為scfv,所述鉸鏈區為igd,所述胞內信號傳導區為cd28–ox40–cd3ζ。圖1為是本發明的治療腫瘤的藥物組合中的antiafpcar設計示意圖,請參考圖1。
進一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述igd的氨基酸序列為第二序列。
具體地,第二序列為:
tftcfvvgsdlkdahltwevagkvptggveegllerhsngsqsqhsrltlprslwnagtsvtctlahpslppqrlmalrepaaqapvklstnllassdppeaa
進一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述cd28的氨基酸序列為第三序列。
具體地,第三序列為:
fwvlvvvggvlacysllvtvafiifwvrskrsallhsdymnmtprrpgptrkhyqpyapprdfaayrs
進一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述ox40的氨基酸序列為第四序列,所述cd3ζ的氨基酸序列為第五序列。
具體地,第四序列為:
rrdqrlppdshkppgggsfrtpiqeeqadahstlaki
具體地,第五序列為:
rvkfsrsaeppayqqgqnqlynelnlgrseeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
進一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,
所述scfv–igd–cd28–ox40–cd3ζ融合蛋白的氨基酸序列為第六序列。
具體地,第六序列為:
evqlvqsgaevkkpgesltisckasgysfpnywitwvrqmsggglewmgridpgdsyttynpsfqghvtisidkstntaylhwnslkasdtamyycaryyvslvdiwgqgtlvtvssggggsggggsggggsqsvltqpasvsgspgqsitisctgtsskvggynyvswyqqhpgkapklmiydvnnrpsevsnrfsgsksgntasltisglqaedeadyykssyttgsravfgggtkltvlgtftcfvvgsdlkdahltwevagkvptggveegllerhsngsqsqhsrltlpralwnagtsvtctlnhpslppqrlmalrepaaqapvklslnllassdppeaafwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrrdqrlppdahkppgggsfrtpiqeeqadahstlakirvkfsrsaeppakqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
進一步地,所述msc-hgf中,所述人源肝細胞生長因子的氨基酸序列為所述msc-hgf的第一序列,所述msc-hgf的第一序列為:
mwvtkllpalllqhvllhllllpiaipyaegqrkrrntihefkksakttlikidpalkaktkkvntadqcanrctrnkglpftckafvfdkarkqclwfpfnsmssgvkkefghefdlyenkdyirnciigkgrsykgtvsitksgikcqpwssmiphehsflpssyrgkdlqenycknprgeeggpwcftsnpevryevcdipqcsevecmtcngesyrglmdhtesgkicqrwdhqtphrhkflperypdkgfddnycrnpdgqprpwcytldphtrweycaiktcadntmndtdvpletteciqgqgegyrgtvntiwngipcqrwdsqyphehdmtpenfkckdlrenycrnpdgsespacfttdpnirvgycsqipncdmshgqdcyrgngknymgnlsqtrsgltcsmwdknmedlhrhifwepdasklnenycrnpdddahgpwcytgnplipwdycpisrcegdttptivnldhpeiscaktkqlrvvngiptrtnigwmvslryrnkhicggslikeswvltarqcfpsrdlkdyeawlgihdvhgrgdekckqvlnvsqlvygpegsdlvlmklarpavlddfvstidlpnygctipektscsvygwsytglinydgllrvahlyimgnekcsqhhrgkvtlneseicagaekigsgpwegdyggplvceqhkmrmvlgvivpgrgcaipnrpgifvrvayyakwihkiiltykvpqs。
進一步地,所述antiafpcar-t細胞通過第一慢病毒感染t淋巴細胞獲得,所述第一慢病毒通過攜帶有所述scfv–igd–cd28–ox40–cd3ζ融合蛋白的慢病毒表達載體感染293t細胞得到。
進一步地,所述msc-hgf通過第二慢病毒感染所述人臍帶間充質干細胞獲得,所述第二慢病毒通過帶有所述人源肝細胞生長因子序列慢病毒表達載體感染293t細胞得到。
本發明的所述藥物組合中的antiafpcar-t細胞和msc-hgf均為單位制劑。所述單位制劑為滿足一次給藥所需有效成分的制劑,如一單位(針)針劑等。患者一次施用所需的藥物的量可以方便地通過計算患者的體重和該患者一次用藥所需單位體重劑量的乘積得到。
更進一步的,根據申請人針對小鼠的實驗,針對人的antiafpcar-t細胞單位制劑中可以包括1×107-10×108個antiafpcar-t細胞,所述msc-hgf單位制劑中可以包括1×106-10×107個msc-hgf。
根據本發明的方案,可以根據需要控制治療腫瘤的藥物組合中的antiafpcar-t細胞用量,方便對不同階段的腫瘤患者的給藥。所述antiafpcar-t細胞的量可以根據腫瘤種類,以及所要治療的腫瘤患者的患病階段,通過適當摸索而確定。一般在應用過程中,該藥物組合中的antiafpcar-t細胞的量為msc-hgf的量的10倍。
本發明的治療腫瘤的藥物組合中,antiafpcar-t細胞將afp抗體用于car-t細胞的構建,從而能夠對afp蛋白高表達的腫瘤細胞進行高效識別與結合;msc-hgf中,hgf可以誘導msc向特定組織樣細胞分化,促進組織再生和修復。因此本發明的治療腫瘤的藥物組合能夠通過識別環節、殺傷環節以及修復環節對癌癥實施高效治療。
附圖說明
圖1為是本發明的治療腫瘤的藥物組合中的antiafpcar設計示意圖;
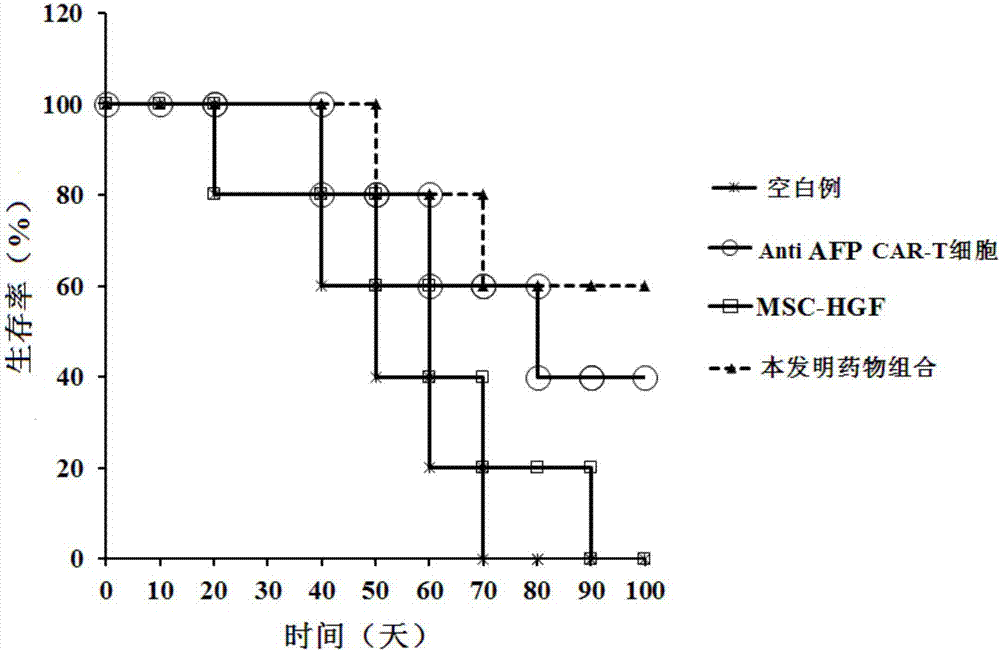
圖2是本發明的治療腫瘤的藥物組合治療肝癌(hepg-2)移植瘤模型小鼠后小鼠生存期示意圖。
具體實施方式
為使本發明的目的、技術方案和優點更加清楚,下面將結合本發明的實施例,對本發明實施例中的技術方案進行清楚、完整地描述,顯然,所描述的實施例是本發明一部分實施例,而不是全部的實施例。基于本發明中的實施例,本領域普通技術人員在沒有做出創造性勞動前提下所獲得的所有其他實施例,都屬于本發明保護的范圍。
實施例1
antiafpcar-t細胞的制備
1、構建慢病毒表達載體
通過常規的基因工程手段,合成scfv–igd–cd28–ox40–cd3ζ融合蛋白基因序列,將scfv–igd–cd28–ox40–cd3ζ融合蛋白基因序列克隆到慢病毒表達載體上,獲得scfv–igd–cd28–ox40–cd3ζ慢病毒表達載體pgreenpuro-car。其中,scfv–igd–cd28–ox40–cd3ζ融合蛋白的各序列如前所述。
2、慢病毒包裝
1)用質量分數為10wt%胎牛血清(fetalbovineserum,簡稱:fbs)的1640培養基培養293t細胞;
2)將293t細胞以3x105/cm2的密度傳至直徑15cm的培養皿中培養20h,保證轉染時細胞匯合度為80-90%;
用不含血清的1640培養基換液,備用;
3)取兩個ep管,分別在兩個ep管中加入1ml1640,將慢病毒載體pgreenpuro-car與pmdlgprre、prsv-rev和pmd2.g質粒按照摩爾比1:1:1:1于其中一個ep管中混勻;在另一個ep管中加入150ullipo2000,混勻放置5min;將混有lipo2000的1640加入含有質粒的ep管中,混勻得混合液,室溫放置20min,然后將混合液逐滴加入上述2)中制備的細胞培養皿中,繼續培養4h后,用含10%fbs的1640培養基更換培養液,繼續培養48h后收集細胞上清液,獲得被scfv–igd–cd28–ox40–cd3ζ融合蛋白包裝的慢病毒。
3、慢病毒純化
將2中獲得的被包裝的慢病毒用0.22μm過濾膜過濾,濾液收集在50ml超濾管中,以3000g/min的速度離心45min;將剩余的上層病毒濃縮液轉移至ep管,放-80℃保存備用。
4、cd8+t細胞的分離
1)全血倒入50ml離心管,室溫離心20分鐘,控制離心力ref為700g(普通離心);
2)取上述離心下部細胞成分,加杜氏磷酸鹽緩沖液dpbs至50ml;
3)分別取25ml上述液體加到20ml人淋巴細胞分離液,將離心管室溫離心15分鐘,控制離心力ref為800g;
5)取白膜層細胞,加入dpbs,補足至50ml;
6)離心10分鐘,控制離心力ref為600g,棄上清液,得外周血單個細胞(peripheralbloodmononuclearcell,簡稱:pbmc);
7)采用cd8+t細胞磁珠分選試劑盒分選cd8+t細胞。
5、慢病毒載體感染t淋巴細胞
用質量分數為10wt%fbs的rpmi1640完全培養基培養cd8+t細胞,第一天加入抗cd3單克隆抗體活化;第三天加入150moi的3中純化后的慢病毒(antiafpcar),16h后將培養基更換為含有50iu/ml重組人il-2的rpmi1640完全培養基,繼續培養10-20天,得到antiafpcar-t細胞。
實施例2
msc-hgf的制備
1、構建慢病毒表達載體
通過常規的基因工程手段,合成hgf融合蛋白基因序列,將hgf基因序列克隆到慢病毒表達載體上,獲得hgf慢病毒表達載體pgreenpuro-hgf。其中,hgf序列如前所述。
2、慢病毒包裝
1)用質量分數為10wt%胎牛血清(fetalbovineserum,簡稱:fbs)的1640培養基培養293t細胞;
2)將293t細胞以3x105/cm2的密度傳至直徑15cm的培養皿中培養20h,保證轉染時細胞匯合度為80-90%;
用不含血清的1640培養基換液,備用;
3)取兩個ep管,分別在兩個ep管中加入1ml1640,將慢病毒載體pgreenpuro-hgf與pmdlgprre、prsv-rev和pmd2.g質粒按照摩爾比1:1:1:1于其中一個ep管中混勻;在另一個ep管中加入150ullipo2000,混勻放置5min;將混有lipo2000的1640加入含有質粒的ep管中,混勻得混合液,室溫放置20min,然后將混合液逐滴加入上述2)中制備的細胞培養皿中,繼續培養4h后,用含10%fbs的1640培養基更換培養液,繼續培養48h后收集細胞上清液,獲得被hgf氨基酸序列包裝的慢病毒。
3、慢病毒純化
將2中獲得的被包裝的慢病毒用0.22μm過濾膜過濾,濾液收集在50ml超濾管中,以3000g/min的速度離心45min;將剩余的上層病毒濃縮液轉移至ep管,放-80℃保存備用。
4、人臍帶間充質干細胞hucmscs的分離培養
臍帶標本取自健康足月妊娠產婦的新生兒臍帶(合作醫院產科提供,經醫院倫理委員會批準同意,產婦簽署知情同意書)。
將無菌條件下取得的新鮮足月剖宮產胎兒臍帶剪切成1~2cm大小的片段,放入培養皿中,并浸泡在生理鹽水中,洗凈殘留液,剔除臍帶動靜脈血管避免內皮細胞污染,取出其中的華通氏膠(wharton’sjelly)剪碎成大小約1mm3小片段,以含10%fbsdmem/f12培養基重懸,接種于25cm2的培養瓶中,放置在37℃、5%co2的培養箱中培養。期間注意觀察細胞形態變化。1周后首次換液,加入10ml完全培養基繼續培養,此后3~4d換液一次。
5、慢病毒載體感染hucmscs
1x106hucmscs加入150moi的3中純化的慢病毒(hgf),6h后更換為完全培養基,繼續培養3天,獲得msc-hgf。
實施例3
本發明的治療腫瘤的藥物組合(antiafpcar-t細胞+msc-hgf)的制備
利用20ml生理鹽水將1×107-antiafpcar-t細胞制成antiafpcar-t細胞單位制劑,利用20ml生理鹽水將1×106個msc-hgf制成msc-hgf單位制劑。混合antiafpcar-t細胞單位制劑與msc-hgf單位制劑,得到本發明的治療腫瘤的藥物組合。
實施例4
本發明的治療腫瘤的藥物組合對腫瘤細胞的殺傷作用
取6周齡雌裸鼠40只,其中20只裸鼠右腋下皮下注射5x106hepg-2(肝癌)細胞,待腫瘤長到60mm3大小,每種腫瘤模型隨機分成4組:對照組、antiafpcar-t細胞組、msc-hgf細胞組、antiafpcar-t細胞+msc-hgf治療組;對照組尾靜脈注射生理鹽水200ul/次,每周2次;antiafpcar-t細胞組尾靜脈注射antiafpcar-t細胞(實施例1制備)1×107個/次,每周2次;msc-hgf細胞組尾靜脈注射msc-hgf細胞(實施例2制備)1×106個/次,每周2次;antiafpcar-t細胞+msc-hgf治療組尾靜脈注射antiafpcar-t細胞+msc-hgf細胞(實施例3制備)),每周2次;統計100天內小鼠生存狀態,做生存率曲線。圖2是本發明的治療腫瘤的藥物組合治療肝癌(hepg-2)移植瘤模型小鼠后小鼠生存期示意圖。
圖2結果表明,本發明的藥物組合(antiafpcar-t細胞+msc-hgf)可明顯延長afp高表達的肝癌移植瘤小鼠模型的生存期。
最后應說明的是:以上各實施例僅用以說明本發明的技術方案,而非對其限制;盡管參照前述各實施例對本發明進行了詳細的說明,本領域的普通技術人員應當理解:其依然可以對前述各實施例所記載的技術方案進行修改,或者對其中部分或者全部技術特征進行等同替換;而這些修改或者替換,并不使相應技術方案的本質脫離本發明各實施例技術方案的范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!