一種制備自噬小體型瘤苗的培養基添加劑及其制備方法與流程
本發明涉及醫藥技術領域,尤其是一種用于制備自噬小體型亞細胞腫瘤疫苗的細胞培養基添加劑凍干粉及其制備方法。
背景技術:
腫瘤細胞代謝產生的蛋白可分為長壽命蛋白和短壽命蛋白兩大類,前者平均半衰期長,結構穩定,主要通過自噬-溶酶體途徑降解;后者平均半衰期短,主要通過泛素-蛋白酶體途徑降解。研究表明,腫瘤細胞直接遞呈的抗原多肽有80%以上來源于短壽命蛋白,而短壽命蛋白由于其半衰期極短難以保存下來。對腫瘤細胞應用蛋白酶體抑制劑阻斷腫瘤短壽命蛋白的降解,促使其進入自噬途徑,同時采用自噬誘導劑促進自噬小體形成,并以弱堿性藥物抑制溶酶體功能,阻止溶酶體對自噬小體中蛋白的降解。在此基礎上,收集富含短壽命蛋白信息的自噬小體,可作為腫瘤疫苗,即自噬小體型亞細胞腫瘤疫苗。
蛋白酶體抑制劑的代表藥物為硼替佐米,其通過結合蛋白酶體20S催化亞單位的不同位點,能選擇性地抑制一些特定蛋白的降解,使得細胞周期不能有序地進行。硼替佐米對蛋白酶體的抑制作用是可逆的,在經過72小時處理后大多數蛋白酶體的活性都可以恢復正常。泛素化的靶蛋白(包括錯誤翻譯、錯誤折疊、突變或變性的蛋白等)除能夠通過泛素-蛋白酶體途徑得以降解外,還能與p62蛋白C端的的泛素相關結構域發生結合,并通過p62蛋白N端的Bem 1結構域發生自我聚集;該聚集體能通過p62蛋白上的LRS/LIR結構域與LC3結合并形成復合物、并由LC3介導形成自噬小體,最后自噬小體與溶酶體融合完成蛋白的降解。
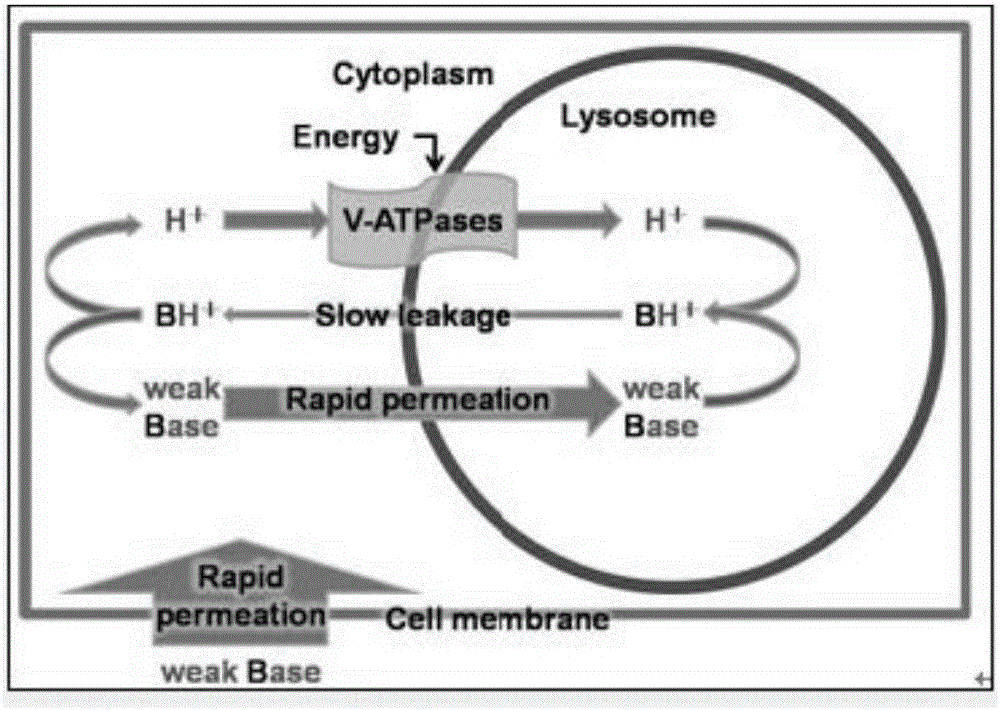
弱堿性藥物氯化銨(Ammonium chloride)、氯喹(Chloroquine,CQ)、羥氯喹(Hydroxychloroquine,HCQ)等可靶向濃集于溶酶體,通過上調溶酶體內pH值,抑制溶酶體相關酸性水解酶的活性,阻斷溶酶體對自噬體的代謝。巴弗洛霉素A1(Bafilomycin A1)是液泡型H+-ATPase(Vacular H+-ATPase,V-ATPase)抑制劑,通過抑制溶酶體膜上的V-ATPase活性,阻止H+由細胞質向溶酶體內的跨膜轉運,影響溶酶體的酸化,抑制溶酶體的功能,阻斷溶酶體對自噬體的胞內消化作用。氯喹口服后,腸道吸收快而充分,服藥后l-2小時血藥濃度達峰值,約55%的藥物在血中與血漿成分結合,血藥濃度維持較久,半衰期為2.5-10天。氯喹在肝、脾、腎、肺中的濃度高于血漿濃度達200-700倍。溶酶體內的pH為酸性,有利于弱堿性藥物氯喹的濃集,濃集的氯喹消耗了溶酶體內的H+,因此可提高溶酶體內的pH,抑制溶酶體內酸性水解酶的活性,而自噬體和溶酶體的融合及融合后被溶酶體內的酸性水解酶降解是自噬代謝途徑的關建環節,因此氯喹具有靶向抑制自噬的作用。
自噬(Autophagy),又稱Ⅱ型程序性細胞死亡,是廣泛存在于真核細胞中的生命現象,包括大自噬(Macroautophagy)、小自噬(Microautophagy)和分子伴侶介導的自噬(Chaperone-mediated autophagy)三種形式。自噬參與調控細胞的發育、分化、成分更新及組織重塑等生理過程,對維持蛋白質代謝平衡及細胞內環境穩定具有重要意義。自噬表現為細胞質中出現大量包裹著細胞質和細胞器的雙層膜囊泡結構,即自噬體(Autophagosome),其與溶酶體融合形成自噬溶酶體,通過溶酶體水解酶降解囊泡內的物質和內層膜而發揮自噬作用。微管相關蛋白1輕鏈3(microtubule-associatedprotein 1 light chain 3,MAP1-LC3,LC3)是目前觀察自噬現象是否存在、研究自噬活性較為可靠的生物學標志物。細胞自噬未發生時,LC3經過加工成為胞漿可溶性LC3Ⅰ。細胞發生自噬時,細胞內LC3的含量及LC3-Ⅰ向LC3-Ⅱ的轉化均明顯增加。因此LC3-Ⅱ的含量或LC3-Ⅱ/LC3-Ⅰ的比例與自噬泡的數量呈正相關,在某種程度上反映了細胞的自噬活性。
細胞內有兩條信號通路與自噬調控有關:
1、依賴mTOR途徑的信號通路
絲氨酸-蘇氨酸激酶(mTOR)是主要的自噬負性調節器。mTOR的活性取決于多種上游信號的輸入,這些上游信號包括能量狀態、營養狀態、氨基酸和生長因子等。當營養缺乏、生長因子信號減弱以及ATP濃度減少時,mTOR都會被抑制。因此在饑餓時,mTOR被抑制,其抑制自噬體形成的作用也解除了,因此自噬體的生產就會增多。自噬誘導劑雷帕霉素是一種親脂的大環內酯類抗生素,可通過抑制mTOR的活性來誘導自噬。
2、非mTOR依賴的信號通路
情緒穩定劑鋰劑可通過非mTOR依賴的信號通路誘導自噬,通過抑制肌醇單磷酸酶來誘導自噬。抑制此酶的活性可以阻止肌醇回收再利用,這就導致了細胞肌醇耗竭,并抑制了磷酸肌醇循環。丙戊酸鈉和卡馬西平是精神穩定藥物,可以通過抑制肌醇合成來降低細胞內肌醇三磷酸IP3的水平,從而影響細胞自噬水平。
海藻糖也能夠激活細胞自噬,是一種新的非mTOR依賴的自噬誘導劑,其具體作用于哪個信號通路目前尚不明楚。由于海藻糖具有無毒性和高溶解度的特點,是一種很有前途的細胞自噬誘導劑,且海藻糖誘導自噬的作用能與雷帕霉素(依賴mTOR信號通路的自噬激活劑)的藥理作用產生明顯的疊加或累積效應。因此,同時聯合應用兩種自噬誘導藥物,其中一種調節依賴mTOR途徑的自噬通路,一個調節不依賴mTOR的信號通路,可以更好的起到調控自噬的作用,降低單用一種藥物的劑量。
中國發明專利CN 102499983 B公開了HepG2.2.15細胞自噬小體在制備HBV治療性疫苗中的應用;中國發明專利CN 102430118 B公開了H22肝癌細胞自噬小體DRibbles在制備肝癌治療性疫苗中的應用;中國發明專利申請公布說明書CN 103463631 A公開了一種基于Hepa1-6肝癌細胞自噬小體-DRibbles的B細胞疫苗及其制備方法。三者所描述的細胞處理方法是待腫瘤細胞生長良好后,加入雷帕霉素、萬珂、和氯化銨,三者的加入量分別為100nmol/L、200nmol/L和30mmol/L,干預16小時,誘導細胞自噬小體。考慮到雷帕霉素的靶點mTOR在生物體內有許多復雜的重要功能,如調節核糖體發生和蛋白質的翻譯等,在誘導腫瘤細胞發生自噬的同時可能不利于細胞內某些腫瘤抗原的合成,最終影響到自噬小體型亞細胞腫瘤疫苗的質量,加之雷帕霉素對機體還有免疫抑制的不良影響,所以有必要開發新型無雷帕霉素影響的、專門用于制備自噬小體型亞細胞腫瘤疫苗的細胞培養基添加劑組合物。目前,尚沒有專門用于制備自噬小體型亞細胞腫瘤疫苗的細胞培養基添加劑組合物凍干粉制劑的公開報道。
前述的相關領域的實例及其局限性意在說明的目的,并不排除存在其它實例及局限性。本領域技術人員在閱讀本說明書和研究附圖后,會明悉相關領域的其它局限性。
附圖說明
圖1為V-ATPase抑制劑和弱堿性藥物抑制溶酶功能模式圖。
圖2為激光掃描共聚焦顯微鏡觀察自噬誘導培養添加劑對HepG2細胞的自噬誘導作用。
圖3為Western blot檢測自噬誘導培養添加劑對A549細胞的自噬誘導作用。
技術實現要素:
本發明的目的提供一種制備自噬小體型瘤苗的培養基添加劑及其制備方法,解決上述現有技術問題中的一個或者多個。
為解決上述問題,本發明的技術方案為:一種制備自噬小體型瘤苗的培養基添加劑,其創新點在于:凍干粉制劑包含一組組合物;組合物包含蛋白酶體抑制劑、自噬誘導劑、溶酶體腔堿化劑、賦形劑和抗氧化劑;蛋白酶體抑制劑是硼替佐米、MG132、乳胞素、2-aminobenzylstatine、Ritonavir、Aclacinomycin、Eponemycin、MLN-519、CEP-1612、CVT-634、TMC-95A、TMC-95B、TMC-95C、TMC-95D、金雀異黃素中的任意一種;自噬誘導劑包括mTOR依賴的信號通路的自噬誘導劑和不依賴mTOR的自噬途徑的自噬誘導劑,以及納米材料自噬誘導劑;mTOR依賴的信號通路的自噬誘導劑為雷帕霉素、40-O-(2-羥乙基)-雷帕霉素、Torkinib、Torin 1中的任意一種;不依賴mTOR的自噬途徑的自噬誘導劑是鋰劑、海藻糖等中的一種;納米材料自噬誘導劑是Fe2O3納米晶體、Fe3O4納米晶體、MnO納米晶體等中的一種;自噬誘導劑還包括具有自噬誘導作用的三氧化二砷中的任意一種;溶酶體腔堿化劑是氯化銨、氯喹、羥氯喹等弱堿性藥物中的一種;賦形劑是指海藻糖、甘露糖中的一種;抗氧化劑是亞硫酸鈉中的一種。
在一些實施方式中,鋰劑是丙戊酸鈉、卡馬西平等中的一種。
在一些實施方式中,硼替佐米,使每份自噬誘導培養添加劑加入總量為500ml的腫瘤細胞培養體系后,硼替佐米的工作濃度為150-200nmol/L。
在一些實施方式中,海藻糖,使每份自噬誘導培養添加劑加入總量為500ml的腫瘤細胞培養體系后,海藻糖的工作濃度為50-100mmol/L。
在一些實施方式中,所述氯喹,使每份自噬誘導培養添加劑加入總量為500ml的腫瘤細胞培養體系后,氯喹的工作濃度為20-80μmol/L。
一種制備自噬小體型瘤苗的培養基添加劑的制備方法,其創新點在于:包括如下步驟:
a.稱取33.0mg硼替佐米、12.0g海藻糖、8.0mg氯喹,混合后,加50ml注射用水,攪拌直至完全溶解。
b.藥液經0.22μm微孔濾膜除菌過濾,灌裝于50ml西林瓶中,半加膠塞,放入凍干機中凍干。
c.先將溫度降至-8℃并保溫90分鐘,之后迅速降溫至-40℃保溫180分鐘,冷阱降溫至-40℃后開始抽真空,緩慢提高擱板溫度至-10℃,保溫18小時,再次提高擱板溫度至25℃,真空度維持在25Pa,直至制品水分合格后凍干結束,凍干箱回填氮氣至常壓。全壓塞出箱,軋蓋、包裝即得,制得的每份自噬誘導培養添加劑凍干粉可用于總量為500ml的腫瘤細胞培養體系。
本發明具有如下突出的優點:
1、本發明所述的添加劑組合物中含有蛋白酶體抑制劑、溶酶體腔堿化劑、自噬誘導劑,三者協同,一方面,可同時抑制腫瘤細胞的蛋白酶體降解途徑和自噬溶酶體降解途徑,使腫瘤抗原得以保存;另一方面,誘導自噬小體形成,使大量腫瘤抗原保存在自噬小體中,通過提取這些自噬小體,即可制備自噬小體型亞細胞腫瘤疫苗;
2、本發明所述的添加劑組合物中含有硼替佐米,為蛋白酶體抑制劑;
3、本發明所述的添加劑組合物中含有氯喹,發揮抑制溶酶體活性的作用;
4、本發明所述的添加劑組合物中含有海藻糖,其一,海藻糖作為不依賴mTOR自噬途徑的自噬誘導劑可促進腫瘤細胞自噬;其二,海藻糖作為蛋白質保護劑可在自噬小體型亞細胞腫瘤疫苗制備過程中可穩定自噬小體膜、保護腫瘤抗原蛋白;其三,海藻糖可作為本發明所述凍干粉制劑的賦形劑;
5、本發明將用于制備自噬小體型亞細胞腫瘤疫苗的細胞培養基專用添加劑組合制備成凍干制劑,容易保存,使用方便,便于質控,解決了多種藥物配置復雜、配置所需時間長,環節多,容易污染的弊端,可顯著提高自噬小體型亞細胞腫瘤疫苗的制備效率,降低工作人員勞動強度。
具體實施方式
下面結合說明書附圖,對本發明進行進一步詳細的說明。
實施例1:制備自噬小體型亞細胞腫瘤疫苗的細胞培養基添加劑凍干粉制劑,稱取33.0mg硼替佐米、12.0g海藻糖、8.0mg氯喹,混合后,加50ml注射用水,攪拌直至完全溶解。藥液經0.22μm微孔濾膜除菌過濾,灌裝于50ml西林瓶中,半加膠塞,放入凍干機中凍干;先將溫度降至-8℃并保溫90分鐘,之后迅速降溫至-40℃保溫180分鐘,冷阱降溫至-40℃后開始抽真空,緩慢提高擱板溫度至-10℃,保溫18小時,再次提高擱板溫度至25℃,真空度維持在25Pa,直至制品水分合格后凍干結束,凍干箱回填氮氣至常壓。全壓塞出箱,軋蓋、包裝即得。
實施例2:自噬誘導培養基添加劑凍干粉的復溶
根據制備自噬小體型亞細胞腫瘤疫苗所用腫瘤細胞的特性,選用合適的雙無培養液50ml用于對自噬誘導培養添加劑凍干粉的復溶,輕輕振蕩直至完全溶解,即為10×自噬誘導培養添加劑母液。按比例加入腫瘤細胞培養體系,使硼替佐米終濃度為172nmol/L,海藻糖終濃度為70mmol/L,氯喹終濃度為50μmol/L,即可用于制備自噬小體型亞細胞腫瘤疫苗。
實施例3:激光掃描共聚焦顯微鏡觀察自噬誘導培養添加劑對HepG2細胞的自噬誘導作用
實驗方法:pEGFP-LC3質粒的轉染:將5μg pEGFP-LC3質粒稀釋于250μlPBS中,輕輕混勻,將5μl GenEscort試劑稀釋于250μl PBS中,充分混勻。然后將稀釋好的250μl GenEscort試劑加入稀釋過的250μl pEGFP-LC3質粒溶液中混合均勻,室溫放置15分鐘,獲得500μl轉染復合物。然后將500μl轉染復合物平均加入預先鋪滿HepG2細胞的六孔板中。待細胞生長5個小時后,用滴管吸出液體,每孔加入4ml培養基繼續培養24小時。將轉染成功的細胞轉入激光共聚焦專用培養皿,待細胞貼壁后,更換新鮮培養液,對照組不做處理,藥物誘導組按比例加入復溶的自噬誘導培養基添加劑,誘導培養18h后置激光掃描共聚焦顯微鏡下檢測腫瘤細胞的自噬情況。
實驗結果:本實驗中將轉染了pEGFP-LC3的HepG2細胞用添加了自噬誘導培養基添加劑的培養基誘導培養18小時,然后在激光掃描共聚焦顯微鏡下觀察胞漿內自噬泡數量的變化。結果發現,自噬誘導培養基添加劑藥物誘導18小時后,實驗組細胞的胞漿內較對照組出現了較多EGFP-LC3標記陽性的、呈綠色熒光的自噬泡。
實施例4:Western blot檢測LC3Ⅱ的表達,觀察自噬誘導培養添加劑對A549細胞的自噬誘導作用
實驗方法:將A549細胞接種于6孔培養板,待細胞生長至90%密合度后,更換新鮮培養液,對照組不做處理,藥物誘導組按比例加入復溶的自噬誘導培養基添加劑,誘導培養18h后,RIPA裂解法提取細胞總蛋白,測定蛋白濃度后,進行SDS-PAGE電泳,將蛋白轉至PVDF膜,室溫封閉2小時,鼠抗人LC3一抗4℃孵育過夜;洗膜3次,每次10分鐘,加入HRP標記的羊抗鼠IgG二抗,室溫孵育2小時;洗膜3次,每次10分鐘,ECL法顯色,掃描觀察LC3反應條帶。
實驗結果:本實驗結果顯示,對于A549細胞,經添加了自噬誘導培養基添加劑的培養基誘導培養18小時后,LC3-Ⅱ的表達量較對照組明顯升高,代表細胞具有較高的自噬水平。
以上所述僅是本發明的優選方式,應當指出,對于本領域普通技術人員來說,在不脫離本發明創造構思的前提下,還可以做出若干相似的變形和改進,這些也應視為本發明的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!