人hsa?miR?124a?3pPCR檢測方法及其在DS妊娠風險預測中的應用與流程
本發明屬于分子生物學技術領域,具體涉及一種人hsa-mir-124a-3ppcr檢測方法及其在ds妊娠風險預測中的應用。
背景技術:
唐氏綜合征(down'ssyndrome,ds)是人類最常見的一種導致新生兒智力缺陷和發育障礙的遺傳性疾病,也稱為21-三體綜合征(trisomy21,t21)或者先天愚型,其在出生胎兒中的發病率大約為1/700,而我國ds的發生率約為(1.53-2.40)/萬。大多數ds胎兒在宮內即停止發育或引發流產,因此,ds實際發病率應遠高于1/700。并且隨著婦女妊娠年齡的增大,尤其是我國現階段人口生育政策的變化,大齡或高齡孕婦增多以及輔助生育技術的進一步推廣和應用,ds發病率有繼續升高的趨勢。ds患兒除了智力缺陷外,還常伴有先天性心臟病、甲狀腺疾病、精神和體格發育遲滯以及器官和組織的多發性畸形等疾病。目前,做好ds患兒的產前早期篩查,避免其出生是最有效的預防ds方案。
ds的產前檢查方案主要分為無創產前檢查(noninvasiveprenataltesting,nipt)和有創產前檢查,其中nipt主要包括唐氏篩查和無創dna檢測,有創性檢查主要包括羊膜腔液體穿刺檢查、絨毛膜穿刺檢查和胎兒臍帶血檢查。唐氏篩查是目前應用最廣的ds產前篩查手段,主要結合了超聲檢查和孕婦血清標志物檢驗。唐氏篩查安全性高,但是特異性較差,雖然胎兒頸項透明層(nuchaltranslucency,nt)>2.5mm時,ds患病率高達84%,但是仍不能達到確診的要求,唐氏篩查高危的孕婦仍然需要后續檢查確診。無創dna檢測是近年來興起的ds產前檢測手段,又稱為無創產前dna檢查或者無創胎兒染色體非整倍體檢查,主要依靠檢測母體血液中胎兒游離dna(cellfreefetaldna,cffdna),并對其進行序列分析以獲得胎兒的遺傳信息,從而診斷ds、帕陶氏綜合征(patausyndrome,ps)和愛德華綜合征(edwardssyndrome,es),其安全性和靈敏度均較高,但是檢查費用較高,技術操作復雜,檢查周期較長,目前衛生主管部門對其實行資質認證管理,多在第三方的醫療檢測機構應用,不易在臨床特別是基層醫療機構推廣。羊膜腔液體穿刺檢查、絨毛膜穿刺檢查和胎兒臍帶血檢查均通過侵襲性操作獲得胎兒脫落細胞并對其進行染色體核型分析,達到確診的目的,雖特異性較高,但是侵襲性操作對操作者的臨床經驗要求高,且有1%導致流產的機率。目前,染色體核型分析雖然是產前診斷ds的金標準,但是其檢測技術復雜、條件要求高且檢測周期長,故僅局限于唐氏篩查的高危孕婦。因此,建立一種安全、價格合理又特異的ds產前檢測手段仍舊是產前診斷領域探索的方向,而與cffdna同屬于血液常見分子的微小rna(micrornas,mirna)分子開始引起人們的重視。
mirna是一類長度約為20-25個堿基的非編碼rna小分子,其主要生理作用是調控基因的表達。mirna可以耐受血液中rna酶的降解,可以在循環血液中長期穩定的存在,同時mirna還可以耐受外界強酸、強堿的處理,為mirna的檢測帶來了方便。此外,mirna還具有很強的組織和器官的特異性,為其成為理想的疾病循環血液學標志物奠定了堅實的基礎。目前研究顯示,健康胎兒和唐氏患兒孕中期母體血漿存在135種表達差異的mirna分子,其中,hsa-mir-124a-3p是表達量顯著性升高的mirna分子中差異值最大的分子。
技術實現要素:
針對以上問題,本發明提供一種操作簡單、結果準確可靠的人hsa-mir-124a-3ppcr檢測方法及其在ds妊娠風險預測中的應用。
本發明實現其目的所采用的技術方案如下:
一種人hsa-mir-124a-3ppcr檢測方法,包括如下步驟:
1)提取待測人血漿樣品的總rna;
2)對提取的rna利用rt-qpcr進行檢測:
a、rt反應:rt引物序列為:
5′-gtcgtatccagtgcgtgtcgtggagtcggcaattgcactggatacgacggcattc-3′,rt反應程序:16℃30min,42℃30min,85℃5min;
b、qpcr反應:qpcr反應程序為:50℃2min,95℃10min;95℃15s,60℃60s,35個循環;
3)建立標準曲線,計算待測樣品中的hsa-mir-124a-3p濃度。
在上述技術方案中,rt反應體系為:rt反應混合物7μl、0.1pmol/μl的hsa-mir-124a-3p標準品5μl、100pmol/μl的rt引物3μl,其中rt反應混合物由如下組分組成:0.15μldntps、1μl50u/μl的multiscribetmreversetranscriptase、1.5μl10×reversetranscriptionbuffer、0.19μl20u/μl的rnaseinhibitor、4.16μlrnase-freewater;qpcr反應體系由如下組分組成:1μl
一種上述的人hsa-mir-124a-3ppcr檢測方法在ds妊娠風險預測中的應用,將采用權利要求1所述的方法測得的待測樣品的hsa-mir-124a-3p濃度應用到ds妊娠風險預測中,將10-5至10-3pmol/μl確定為權利要求1所述的檢測方法的ds高危風險的區間值。
本發明的有益效果是:成功構建了血漿hsa-mir-124a-3p的rt-qpcr檢測方法,該方法的檢測線性范圍寬、檢測靈敏度高、檢測特異性、重復性較好,可用于臨床標本中微量hsa-mir-124a-3p的定量檢測。同時檢測hsa-mir-124a-3p的rt-qpcr方法具有操作相對簡單、檢測快速、成本低廉等優點,有望應用于ds的產前篩查。本發明實驗證明hsa-mir-124a-3p在ds妊娠風險預測的價值比常規血清唐氏篩查方法高,為hsa-mir-124a-3p在ds妊娠產前篩查中的應用奠定了基礎。
附圖說明
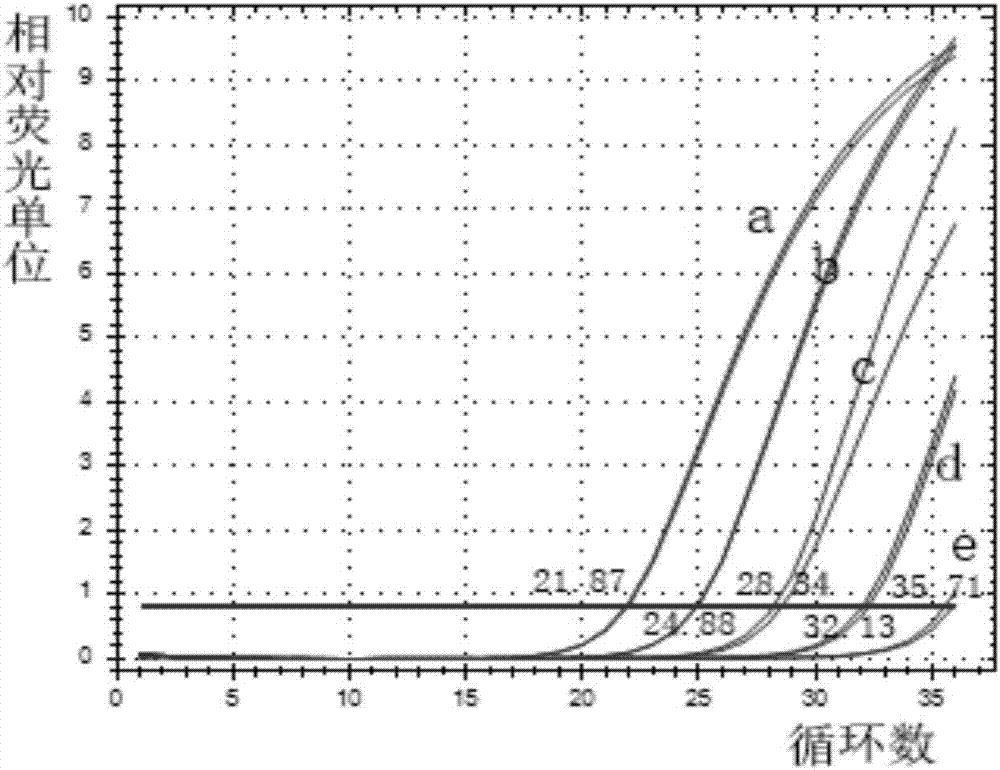
圖1是不同濃度hsa-mir-124a-3p逆轉錄cdna的qpcr擴增曲線圖,其中,曲線a、b、c、d、e分別為10-2、10-3、10-4、10-5和10-6pmol/μl的hsa-mir-124a-3p逆轉錄cdna的擴增曲線。
圖2是hsa-mir-124a-3pqpcr標準曲線圖。
圖3是hsa-mir-124a-3prt-qpcr檢測方法的靈敏度、特異性及重復性檢測圖,其中,圖a、b、c分別為30、35、40個循環時hsa-mir-124a-3p標準品實驗組和rnase-freewater陰性對照組的擴增曲線。
圖4是hsa-mir-124a-3p診斷ds妊娠的roc曲線圖。
圖5是hsa-mir-124a-3p檢測法和血清唐氏篩查的ds風險預測roc曲線圖,其中,a、b分別為hsa-mir-124a-3p檢測法和唐氏篩查的ds風險預測roc曲線。
具體實施方式
下面結合實施例對本發明作進一步說明,但并不因此而限制本發明。
相關試劑
(1)逆轉錄試劑:multiscribetmreversetranscriptase(50u/μl)、10×reversetranscriptionbuffer、dntpmix(100mmtotal)、rnaseinhibitor(20u/μl)均購于上海市愛普拜斯應用生物系統貿易有限公司;hsa-mir-124a-3p逆轉錄引物由上海市生物工程有限公司合成;tebuffer由上海市聰誠實業有限公司提供。
(2)熒光定量pcr擴增試劑:
(3)血漿mirna提取試劑:trzolls購自上海玉博生物科技有限公司。
(4)逆轉錄試劑:multiscribetmreversetranscriptase(50u/μl)、10×reversetranscriptionbuffer、dntpmix(100mmtotal)、rnaseinhibitor(20u/μl)均購于上海市愛普拜斯應用生物系統貿易有限公司;hsa-mir-124a-3p逆轉錄引物由上海市生物工程有限公司合成;u6snrna逆轉錄引物由賽默飛世爾科技公司提供;tebuffer由上海市聰誠實業有限公司提供。
(5)熒光定量pcr擴增試劑:
(6)唐氏篩查試劑:afp、βhcg和ue3檢測試劑盒由羅氏公司提供。
(7)其他試劑:hsa-mir-124a-3p標準品由大連寶生物工程有限公司合成。
實施例1、hsa-mir-124a-3p的rt-qpcr檢測
一、hsa-mir-124a-3prt反應
(1)hsa-mir-124a-3p標準品的合成:登錄http://www.mirbase.org/網站,獲取hsa-mir-124a-3p的堿基序列為5′-uaaggcacgcggugaaugcc-3′(如seqidno:1所示)。將獲得的hsa-mir-124a-3p序列送至大連寶生物工程有限公司合成hsa-mir-124a-3p標準品(12.8nmols)。
(2)不同濃度hsa-mir-124a-3p標準品的配制:將1.28mlrnase-freewater加入12.8nmol數的hsa-mir-124a-3p標準品中,配制成10pmol/μl的hsa-mir-124a-3p標準品溶液,作為標準品的儲存液。然后繼續用rnase-freewater將10pmol/μl的hsa-mir-124a-3p標準品以10倍濃度梯度稀釋至1和0.1pmol/μl2種濃度。
(3)hsa-mir-124a-3prt引物的設計:將hsa-mir-124a-3p序列中的u全部替換為t,得到序列為5′-taaggcacgcggtgaatgcc-3′,其互補序列為5′-ggcattcaccgcgtgcctta-3′,將其5′端的7個堿基做為rt引物粘附序列,可得rt引物5′-gtcgtatccagtgcgtgtcgtggagtcggcaattgcactggatacgacggcattc-3′(如seqidno:2所示)。
(4)hsa-mir-124a-3prt反應混合物的配制:各組分比例如表1所示:
表1rt反應混合物配制比例
(5)hsa-mir-124a-3prt反應
hsa-mir-124a-3prt反應體系:rt反應混合物7μl、hsa-mir-124a-3p(0.1pmol/μl)5μl、rt引物(100pmol/μl)3μl。
hsa-mir-124a-3prt反應程序:16℃30min,42℃30min,85℃5min,4℃保存。
二、hsa-mir-124a-3pqpcr反應
(1)qpcr反應體系的配制:以hsa-mir-124a-3prt反應產物為陽性實驗組、以相同量的rnase-freewater為陰性對照組,分別配制qpcr反應體系(表2)。
表2qpcr反應體系
(2)qpcr反應程序設置:如表3所示。
表3qpcr反應程序
(3)hsa-mir-124a-3p標準品的質量驗證:觀察實驗組和對照組的擴增曲線和循環閾值(cyclethreshold,ct),驗證hsa-mir-124a-3p標準品的完整性。
三、hsa-mir-124a-3prt-qpcr檢測方法標準曲線的建立和評價
將hsa-mir-124a-3p標準品稀釋為1×10-1、1×10-2、1×10-3、1×10-4、1×10-5、1×10-6pmol/μl等濃度,分別在同樣條件下進行qpcr擴增反應,發現標準品濃度在1×10-2至1×10-6pmol/μl范圍時,其對應的擴增曲線呈典型的對數擴增(如圖1所示),且兩相鄰擴增曲線的間距較為接近,故以1×10-2、1×10-3、1×10-4、1×10-5和1×10-6pmol/μl這五種濃度的對數值(lg值)為橫坐標,對應擴增曲線的ct值為縱坐標,作標準曲線(如圖2所示)。從圖中觀察發現,標準曲線的ct值與起始濃度存在良好的線性關系,經計算可得r2=0.998>0.98,說明標準曲線的線性程度符合要求,故將1×10-2至1×10-6pmol/μl定為hsa-mir-124a-3prt-qpcr檢測方法的線性范圍。計算兩相鄰循環數差值分別為3.01、3.46、3.79、3.58,其相鄰循環稀釋濃度分別為8.06、11.00、13.83、11.96,均值為11.21與標準品的實際稀釋濃度倍數10相接近。計算可得qpcr擴增效率為93.3%,介于90%-105%之間,說明反應條件已優化。
四、hsa-mir-124a-3prt-qpcr方法學評價
分別用建立的hsa-mir-124a-3prt-qpcr方法檢測hsa-mir-124a-3p標準品為模板的陽性實驗組和相同量的rnase-freewater的陰性對照組,發現該方法能夠重復且穩定檢測出hsa-mir-124a-3p的最低濃度為1×10-6pmol/μl。分別在30、35、40循環數下用hsa-mir-124a-3prt-qpcr檢測hsa-mir-124a-3p標準品和rnase-freewater的陰性對照組,發現該方法能夠特異的檢測出hsa-mir-124a-3p的循環數為35(如圖3所示,其中實驗組和對照組分別設有2個平行管)。此外,平行管擴增曲線顯示二者ct值差異較小,說明本方法重復性好。
實施例2、母體血漿hsa-mir-124a-3p在唐氏綜合征產前篩查中的臨床應用
一、血漿中總rna的提取
臨床標本收集及分組:收集第三軍醫大學第一附屬醫院婦產科產前診斷中心20~35歲妊娠健康胎兒的妊娠中期(13-27周)孕婦血漿36例為正常對照組;確診妊娠ds胎兒的妊娠中期孕婦血漿11例為ds妊娠組;血液標本采用edta抗凝,在25℃條件下3000r/min,離心3min后吸取上層血漿,-80℃儲存備用。提取血漿中總rna。
二、rt-qpcr反應
按照實施例1中的方法對提取的血漿rna進行rt-qpcr方法檢測各組臨床標本中的hsa-mir-124a-3p的含量。同時以相同量的rnase-freewater為陰性對照,加入u6snrnart反應產物作為實驗內參陽性對照,每個樣品設置2個平行檢測管。利用u6snrna內參在相同量的樣本中表達較為一致的特點,對計算所得hsa-mir-124a-3p濃度進行校正。
三、基于時間分辨熒光免疫分析的血清唐氏篩查實驗
(1)用碘伏消毒肱靜脈表面皮膚,抽取本研究所有標本來源孕婦孕中期空腹靜脈血5ml,不抗凝,在25℃條件下3000r/min,離心3min,吸取上層血清,-80℃儲存備用。
(2)在96孔微孔板第一孔中加入βhcg標準品25μl,然后依次分別加入25μl待測血清,所有加樣孔內均加入抗βhcg試劑稀釋液200μl。
(3)另取一96孔微孔板,在第一孔中加入afp標準品25μl,然后依次分別加入25μl待測血清,所有加樣孔內均加入抗afp試劑稀釋液200μl。
(4)將兩個微孔板緩慢震蕩3h,震蕩期間分別洗板6次。
(5)再取一96孔微孔板,第一孔中加入ue3標準品100μl,然后依次分別加入100μl待測血清,緩慢震蕩15min后所有加樣孔內均加入100μlue3示蹤稀釋液,緩慢震蕩1h,震蕩期間分別洗板6次。
(6)在三個微孔板的反應孔中依次加入增強液200μl,緩慢震蕩5min,預熱時間分辨免疫熒光分析儀15min后,上機檢測afp、βhcg和ue3的濃度。
(7)篩查報告:將孕婦的胎數,人種,年齡,體重,孕周,是否胰島素依賴型糖尿病,afp、hcg和ue3檢查結果輸入產前篩查軟件,得到唐氏篩查報告。記錄血清唐氏篩查報告為ds妊娠高風險和低風險的孕婦信息。
四、染色體核型分析
(1)以0.6mm內徑的長針,在超聲波的引導下,穿過孕婦腹部,經過子宮壁,到達羊膜腔,然后抽取20ml羊水,1500r/min,離心10min,吸取上清液作其他檢驗,將余下0.5ml沉淀輕柔吹打混勻后接種在含有0.9ml小牛血清和2.1mlf10培養液的培養瓶中,搖勻,37℃培養6d后更換培養液,37℃培養6d后加入秋水仙堿,搖勻,使秋水仙堿的終濃度達到3μg/ml,繼續37℃孵育4h。
(2)取出細胞懸液,0.002%的胰蛋白酶溶液2ml中消化5min,1500r/min,離心5min,棄去上清后加入0.4%枸櫞酸鈉和0.4%氯化鉀比例為1:1溶液5滴,37℃孵育5min。
(3)取出離心管,加入甲醇和冰醋酸比例為3:1的固定液7滴,輕柔吹打混勻,1500r/min,離心5min,棄去上清后再加入甲醇和冰醋酸比例為3:1的固定液4ml,輕柔吹打混勻,靜置40min,再次1500r/min,離心5min,棄去上清后加入甲醇和冰醋酸比例為3:1的固定液2ml,輕柔吹打混勻,靜置20min。1500r/min,離心5min,棄去上清后將加3滴固定液將沉淀制成混懸液。
(4)將2滴上述混懸液滴在處理后的載玻片上,輕柔吹氣,使混懸液均勻分布并晾干。將載玻片置于90℃烤箱拷片45min后放入0.002%的胰蛋白酶溶液中消化60s,隨后用giemsa染液染色5min,流水沖洗載玻片并在空氣中晾干。
(5)在顯微鏡下觀察染色體條帶,并對其進行計數。其中46,xn表示染色體核型正常的胎兒,n代表x或y染色體中的一條。47,xn,+21代表多了一條21號染色體的ds胎兒。
五、統計學分析
(1)將所有的檢測結果錄入excel表,建立數據庫,應用spss23.0統計軟件對健康胎兒和ds患兒母體血漿hsa-mir-124a-3p檢測結果進行獨立樣本t檢驗,計算二者均數倍值,將所得結果與前期研究結果相比較。
(2)以染色體核型分析作為金標準,將hsa-mir-124a-3p的檢測結果以10-8至10-7pmol/μl作為程度1,10-7至10-6pmol/μl作為程度2,依次類推,以10倍濃度區間內結果出現的次數作為頻數,作roc曲線,選擇約登指數(youdenindex,yi)最大值所對應的頻數對應的hsa-mir-124a-3p濃度范圍作為rt-qpcr檢測方法預測孕中期ds高危風險的區間值。
(3)以染色體核型分析作為金標準,分別作唐氏篩查和rt-qpcr檢測方法預測ds風險的結果作roc曲線,比較二者預測ds風險的價值。
六、結果
1、健康胎兒和ds胎兒母體血漿hsa-mir-124a-3p檢測結果的比較
利用hsa-mir-124a-3prt-qpcr檢測方法分別對36例健康胎兒和11例ds患兒母體血漿hsa-mir-124a-3p的表達水平進行了檢測(表4)。已知hsa-mir-124a-3prt-qpcr檢測方法的檢測下限為1×10-6pmol/μl,因實際檢測了200μl血漿中hsa-mir-124a-3p濃度,故臨床應用檢測下限為1×10-8pmol/μl。若將正常組低于檢測下限的值假定為1×10-8pmol/μl,對正常組和ds組hsa-mir-124a-3p濃度進行獨立樣本t檢驗可得:p=0.021<0.05,說明正常組和ds組hsa-mir-124a-3p濃度差異存在統計學意義,正常組hsa-mir-124a-3p濃度顯著小于ds組hsa-mir-124a-3p濃度,與前期研究結果符合。另外,經計算可得正常組和ds組hsa-mir-124a-3p濃度均值差異倍數為:1659.7459,對比前期研究差異倍數918.7662,本研究所得差異倍數偏大,分析原因可能是與前期研究采用檢測方法不同所致。
表4健康胎兒和ds患兒母體血漿hsa-mir-124a-3p濃度
2、hsa-mir-124a-3p預測ds妊娠高危風險的區間值
以染色體核型分析作為金標準,將hsa-mir-124a-3p10-8至10-7pmol/μl作為程度1,10-7至10-6pmol/μl作為程度2,依次類推,以10倍濃度區間內結果出現次數作為頻數繪制表5,再根據表5結果作對應的roc曲線(圖4),根據統計學分析結果可得該roc曲線的標準誤為0.042,p=0.000,95%的置信區間為(0.833,0.998),roc曲線下面積為0.915。計算可得該roc曲線最大的yi為0.735,而其所對應的程度為4.5,說明hsa-mir-124a-3p濃度在10-5至10-3pmol/μl時對ds的診斷價值最大,故將10-5至10-3pmol/μl定為hsa-mir-124a-3prt-qpcr檢測方法預測ds高危風險的區間值。
表5rt-qpcr檢測結果
3、hsa-mir-124a-3prt-qpcr檢測方法與唐氏篩查的比較
由上述結果分析可知,將孕中期婦女血漿hsa-mir-124a-3p濃度在10-5至10-3pmol/μl區間者定為ds高風險。以此作為ds妊娠高危風險區間值,并以染色體核型分析作為金標準,將血清唐氏篩查結果與hsa-mir-124a-3p檢測結果進行比較(表6)。同時分別對hsa-mir-124a-3p檢測和唐氏篩查的ds風險預測情況作roc曲線(圖5)。其中rt-qpcr法相應的標準誤為0.093,p=0.006,95%的置信區間為(0.594,0.959),曲線下面積為0.777,表示rt-qpcr法對ds風險預測中等。而唐氏篩查相應的標準誤為0.097,p=0.171,95%置信區間為(0.448,0.827),曲線下面積為0.638,表示其風險預測價值較低。結果提示hsa-mir-124a-3p在ds妊娠風險預測的價值比常規血清唐氏篩查方法高。
表6血清唐氏篩查和hsa-mir-124a-3p檢測的結果比較
序列表
<110>中國人民解放軍第三軍醫大學第一附屬醫院
<120>人hsa-mir-124a-3ppcr檢測方法及其在ds妊娠風險預測中的應用
<130>1
<160>2
<210>1
<211>20
<212>rna
<213>人工序列
<223>hsa-mir-124a-3p
<400>1
uaaggcacgcggugaaugcc20
<210>2
<211>55
<212>dna
<213>人工序列
<223>rt引物
<400>2
gtcgtatccagtgcgtgtcgtggagtcggcaattgcactggatacgacggcattc55
- 還沒有人留言評論。精彩留言會獲得點贊!