一種自組裝高效光催化劑及其制備方法和應用與流程
本發明屬于光催化水解制氫領域,具體地涉及一種具有可見光高光催化活性的上轉換發光材料(Y2SiO5:Pr3+,Li)與納米混合型鈣鈦礦(NaNbxTa1-xO3)結合同時負載貴金屬鉑(Pt)的自組裝高效光催化劑及其制備方法和在光催化水解制氫中的應用。
背景技術:
近年來,全球能源需求不斷增長,供需矛盾進一步惡化。煤、石油、天然氣等常規能源是目前全球消耗的最主要能源,但使用過程中會新增大量溫室氣體CO2,同時可能產生一些有污染的煙氣,威脅全球生態。從另一方面看,隨著人類的不斷開采,化石能源的枯竭是不可避免的,大部分化石能源本世紀將被開采殆盡,所以將會帶來嚴重的能源危機。能源是經濟和社會發展的動力,是社會經濟發展目標能否實現的具體保證,因此,開發清潔可再生能源已經迫在眉睫。
近些年,世界各地都致力于發展新型環保能源,例如太陽能、核能、地熱能、風能、海洋能和氫能等。其中氫能被公認為是未來最有潛力的能源之一,氫具有高揮發性、高能量,是能源載體和燃料,同時氫在工業生產中也有廣泛應用。現在工業每年用氫量為5500億立方米,氫氣與其它物質一起用來制造氨水和化肥,同時也應用到汽油精煉工藝、玻璃磨光、黃金焊接、氣象氣球探測及食品工業中。液態氫可以作為火箭燃料,因為氫的液化溫度在-253℃。由此可以看出,氫能正逐漸取代其他能源成為能源科學界的熱點。因此,氫能正是一種在常規能源危機的出現、環境污染問題日益嚴重以及在開發新能源的背景下人們期待的新的清潔能源。
眾所周知,氫能有許多令人滿意的優點。現有技術中可以利用電解水、熱裂解等方法制取氫氣,但是成本極高。近年來,利用光解水制氫已經收到了廣泛的關注,在利用半導體分解水方面也做出了巨大的努力。其中,NaTaO3是被研究最為廣泛的催化劑之一,它在光解水制備氫氣和氧氣方面有著誘人的前景。但是由于NaTaO3的帶隙較寬,只有在紫外光照射下才能產生高的光催化活性。令人遺憾的是太陽光中僅有不足4.0%的紫外光,因此大大降低了光催化制氫的效果并限制了它的實際應用。因此,發明一種具有可見光高光催化活性的光催化劑變得尤為重要。
技術實現要素:
為了解決納米NaTaO3作為光催化分解水制氫的重要催化劑光催化效率不高,僅能吸收太陽光中不足4%的紫外光照射的問題,本發明提供一種將上轉換紫外發光材料(Y2SiO5:Pr3+,Li)與納米光催化劑(NaNbxTa1-xO3)結合,同時負載貴金屬Pt的自組裝高效光催化劑,該催化劑可大幅度提高光催化水解制氫的效率。
本發明采用的技術方案是:一種自組裝高效光催化劑,所述的自組裝高效光催化劑是Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3,其中,x=0-0.5,Y2SiO5:Pr3+,Li與NaNbxTa1-xO3的質量比為0.0-1.0:1.0,鉑的負載量為0.2-0.3%。
優選的,所述的自組裝高效光催化劑是Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3,其中,x=0.5,Y2SiO5:Pr3+,Li與NaNbxTa1-xO3的質量比為0.4:1.0,鉑的負載量為0.25%。
上述的一種自組裝高效光催化劑的制備方法,方法如下:將適量的Y2SiO5:Pr3+,Li/NaNbxTa1-xO3與氯鉑酸混合,加入適量的甲醇,在室溫下,超聲分散30-60min,加熱煮沸30-60min,干燥,將所得的固體混合物研磨,隨后在200-300℃煅燒3.0-3.5h,得到Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3。
上述的一種自組裝高效光催化劑的制備方法,所述的Y2SiO5:Pr3+,Li/NaNbxTa1-xO3的制備方法為:將適量的固體Ta2O5、Nb2O5與固體NaOH混合,將所得的混合物加入到蒸餾水中,充分攪拌30-60min,加入Y2SiO5:Pr3+,Li,再充分攪拌30-60min,然后將所得的懸濁液加入到聚四氟乙烯反應釜中,在150-200℃下恒溫加熱15.0-16.0h,得到的產物用去離子水和乙醇洗滌,干燥,得到Y2SiO5:Pr3+,Li/NaNbxTa1-xO3。
上述的一種自組裝高效光催化劑的制備方法,所述的Y2SiO5:Pr3+,Li的制備方法為:按化學分子式Y2SiO5:Pr3+,Li中各元素配比取料,將Y2O3和Pr6O11溶解在濃硝酸中,并磁力加熱攪拌直至無色透明,蒸發出多余的硝酸,然后加入LiNO3、乙醇、蒸餾水和四乙氧基硅烷,在室溫下攪拌5-30min,升溫至60-80℃,加熱攪拌至溶液呈透明凝膠,將透明凝膠在80℃烘箱中烘干,然后在1000-1200℃煅燒3.0-4.0h,得Y2SiO5:Pr3+,Li。
上述的一種自組裝高效光催化劑在光催化水解制氫中的應用。方法如下:將上述的自組裝高效光催化劑加入到甲醇水溶液中,在可見光下,照射5.0-6.0h。
本發明的自組裝高效光催化劑Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3在可見光照射下分解水制氫的原理:由于NaNbxTa1-xO3的能帶較寬,只能吸收紫外光。所以當可見光直接照射NaNbxTa1-xO3時,幾乎不能激發NaNbxTa1-xO3粒子產生電子-空穴對,而當可見光照射到Y2SiO5:Pr3+,Li后,由于Y2SiO5:Pr3+,Li在可見光(低能量的光)照射下基態光子能夠被逐級激發到更高的能級,然后這些光子再躍遷回基態后發射出紫外光(高能量的光),這些紫外光能有效地激發Y2SiO5:Pr3+,Li周圍的NaNbxTa1-xO3粒子,經過激發的NaNbxTa1-xO3價帶(VB-band)上的電子可以傳遞到導帶(CB-band)上,從而形成具有高能量的電子-空穴對,這些載流子易復合湮滅而釋放光或熱,沒有湮滅的光生電子和空穴使NaNbxTa1-xO3表現出光催化性能。光催化分解水制氫的機理在于吸附在催化劑表面的H+被遷移到催化劑表面的光生電子還原生成H2,同時吸附在催化劑表面的OH-被遷移到催化劑表面的光生空穴氧化生成O2,其本質是一個氧化還原過程。因此,光催化分解水制氫的產物為H2和O2。為了提高光催化分解水制氫的效率和純度,本發明加入了貴金屬Pt和電子犧牲劑甲醇,其中加入貴金屬Pt的目的是增加NaNbxTa1-xO3表面的產氫活性位點,抑制光生電子-空穴對的復合;而加入電子犧牲劑甲醇的目的在于消耗NaNbxTa1-xO3產生的空穴,使反應向有利于生成氫氣的方向進行。為了最大限度的給NaNbxTa1-xO3提供紫外光,使其光催化效率得到大幅度的提高,本發明,利用寬波短光譜吸收上轉換紫外發光材料Y2SiO5:Pr3+,Li,通過最大限度地把太陽光中的可見光轉變成紫外光的原理來制備具有更高光催化水解制氫性能的新型Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3光催化劑。
本發明的有益效果:本發明制備了一種新型的自組裝高效光催化劑(Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3),此催化劑性質穩定,耐高溫,有較高的光電轉換效率,與單純的Pt-NaTaO3相比,此催化劑在太陽光的照射下水解制氫的效率有了大幅度提高。值得關注的是在上轉換發光材料(Y2SiO5:Pr3+,Li)的加入下,使Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3納米光催化劑不僅可以吸收紫外光,還可以將吸收的可見光轉化為紫外光,提高光催化制氫活性。為了更好地利用轉化來的不連續的紫外光,通過加入不同比例的Nb來調節NaTaO3的帶隙,使NaNbxTa1-xO3的吸收光與轉換發光材料(Y2SiO5:Pr3+,Li)的發射光實現完美對接。可以大幅度的提高NaTaO3光催化水解制氫的效率。
附圖說明
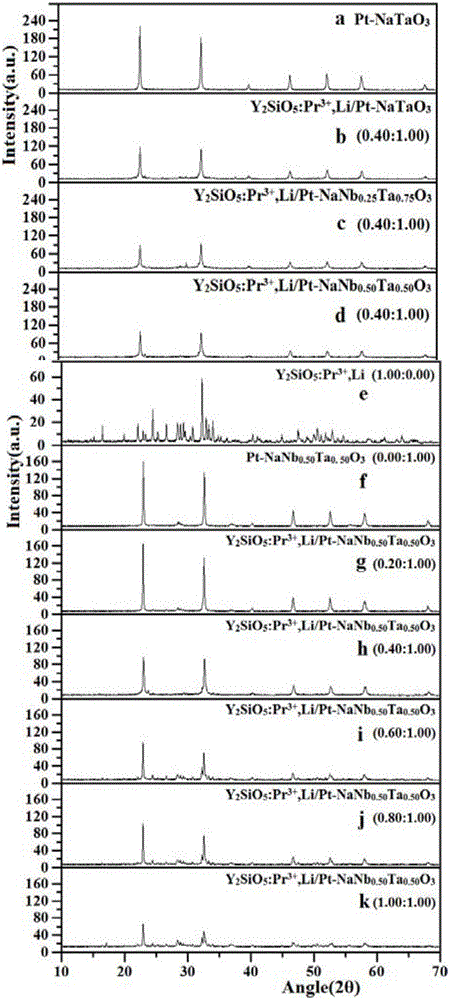
圖1是X粉末衍射(XRD)圖;
其中,a:Pt-NaTaO3;
b-d:x=0,0.25,0.5;Y2SiO5:Pr3+,Li與NaNbxTa1-xO3的質量比為0.4:1.0;
e-k:x=0.5;Y2SiO5:Pr3+,Li與NaNb0.5Ta0.5O3的質量比分別為1.0:0.0,0.0:1.0,0.2:1.0,0.4:1.0,0.6:1.0,0.8:1.0,1.0:1.0。
圖2是掃描電鏡(SEM)照片。
圖3是能量彌散X射線分析(EDAX)圖片。
圖4a是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3的X射線光電子能譜(XPS)圖片。
圖4b是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Ta 4f)的X射線光電子能譜(XPS)圖片。
圖4c是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Li 1s)的X射線光電子能譜(XPS)圖片。
圖4d是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Si 2p)的X射線光電子能譜(XPS)圖片。
圖4e是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Y 3d)的X射線光電子能譜(XPS)圖片。
圖4f是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Nd 3d)的X射線光電子能譜(XPS)圖片。
圖4g是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(O 1s)的X射線光電子能譜(XPS)圖片。
圖4h是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Na 1s)的X射線光電子能譜(XPS)圖片。
圖4i是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Pr 3d)的X射線光電子能譜(XPS)圖片。
圖4j是Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Pt 4f)的X射線光電子能譜(XPS)圖片。
圖5a是Y2SiO5:Pr3+,Li的紫外可見吸收光譜圖片。
圖5b是Y2SiO5:Pr3+,Li的光致發光譜(PL)(482nm)圖片。
圖5c是Y2SiO5:Pr3+,Li的光致發光譜(PL)(443nm)圖片。
圖6是光照時間對光催化分解水制氫的影響。
圖7是Y2SiO5:Pr3+,Li與NaNb0.5Ta0.5O3不同質量比對光催化分解水制氫效率的影響。
圖8是催化劑光催化分解水制氫重復使用次數圖。
具體實施方式
實施例1自組裝高效光催化劑Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3
(一)自組裝高效光催化劑Y2SiO5:Pr3+,Li/Pt-NaTaO3(x=0)
(1)上轉換紫外發光材料Y2SiO5:Pr3+,Li納米粉末的制備
取(2.9308g)Y2O3粉末和(0.05972g)Pr6O11粉末加入到過量濃硝酸中,磁力加熱攪拌直至無色透明,蒸發出多余的濃硝酸。取(0.6048g)LiNO3,(10mL)乙醇和(4mL)蒸餾水加入上述溶液中,然后再加入(4.0mL)四乙氧基硅烷,在室溫下磁力攪拌10min,然后升溫到70℃,加熱攪拌至溶液呈透明凝膠,將透明凝膠放入烘箱,恒溫104℃加熱17h,進行烘干得干凝膠,將得到的干凝膠在馬弗爐中1000℃加熱煅燒3h,冷卻至室溫,研磨,得到Y2SiO5:Pr3+,Li納米粉末。
(2)Y2SiO5:Pr3+,Li/NaTaO3納米粉末的制備
稱取(0.876g)Ta2O5固體粉末和(1.6g)NaOH固體加入到(20mL)蒸餾水中,攪拌1.0h,加入(0.4285g)Y2SiO5:Pr3+,Li固體粉末,繼續攪拌1.0h。將所得懸濁液倒入50mL聚四氟乙烯反應釜中,在200℃下恒溫反應15.0h,冷卻至室溫,得到的產物分別用去離子水和乙醇洗滌5次,最后在80℃烘干12h,將得到的固體粉末充分研磨,得到Y2SiO5:Pr3+,Li/NaTaO3納米粉末。
(3)Y2SiO5:Pr3+,Li/Pt-NaTaO3納米光催化劑的制備
于(1.0g)Y2SiO5:Pr3+,Li/NaTaO3納米粉末中加入(40mL)甲醇,在室溫下超聲分散30min。然后向所得的混合物中加入(4.0mL)H2PtCl6·H2O,并在室溫下超聲分散30min,隨后加熱煮沸30min,待溶液冷卻至室溫后,在120℃干燥4.0h至溶劑全部蒸干為止,將所得的固體混合物充分研磨,隨后在300℃煅燒3.0h,冷卻至室溫,得到Y2SiO5:Pr3+,Li/Pt-NaTaO3納米粉末。
(二)自組裝高效光催化劑Y2SiO5:Pr3+,Li/Pt-NaNb0.25Ta0.75O3(x=0.25)
(1)上轉換紫外發光材料Y2SiO5:Pr3+,Li納米粉末的制備
同(一)
(2)Y2SiO5:Pr3+,Li/NaNb0.25Ta0.75O3納米粉末的制備
稱取(0.720g)Ta2O5固體粉末、(0.133g)Nb2O5固體粉末和(1.6g)NaOH固體加入到(20mL)蒸餾水中,攪拌1.0h,加入(0.4285g)Y2SiO5:Pr3+,Li固體粉末,繼續攪拌1.0h。將所得懸濁液倒入50mL聚四氟乙烯反應釜中,在200℃下恒溫反應15.0h,冷卻至室溫,得到的產物分別用去離子水和乙醇洗滌5次,最后在80℃烘干12h,將得到的固體粉末充分研磨,得到Y2SiO5:Pr3+,Li/NaNb0.25Ta0.75O3納米粉末。
(3)Y2SiO5:Pr3+,Li/Pt-NaNb0.25Ta0.75O3納米光催化劑的制備
于(1.0g)Y2SiO5:Pr3+,Li/NaNb0.25Ta0.75O3納米粉末中加入(40mL)甲醇,在室溫下超聲分散30min。然后向所得的混合物中加入(4.0mL)H2PtCl6·H2O,并在室溫下超聲分散30min,隨后加熱煮沸30min,待溶液冷卻至室溫后,在120℃干燥4.0h至溶劑全部蒸干為止,將所得的固體混合物充分研磨,隨后在300℃煅燒3.0h,冷卻至室溫,得到Y2SiO5:Pr3+,Li/Pt-NaNb0.25Ta0.75O3納米粉末。
(三)自組裝高效光催化劑Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(x=0.5)
(1)上轉換紫外發光材料Y2SiO5:Pr3+,Li納米粉末的制備
同(一)
(2)Y2SiO5:Pr3+,Li/NaNb0.5Ta0.5O3納米粉末的制備
稱取(0.530g)Ta2O5固體粉末、(0.319g)Nb2O5固體粉末和(1.6g)NaOH固體加入到(20mL)蒸餾水中,攪拌1.0h,加入(0.4285g)Y2SiO5:Pr3+,Li固體粉末,繼續攪拌1.0h。將所得懸濁液倒入50mL聚四氟乙烯反應釜中,在200℃下恒溫反應15.0h,冷卻至室溫,得到的產物分別用去離子水和乙醇洗滌5次,最后在80℃烘干12h,將得到的固體粉末充分研磨,得到Y2SiO5:Pr3+,Li/NaNb0.5Ta0.5O3納米粉末。
(3)Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3納米光催化劑的制備
于(1.0g)Y2SiO5:Pr3+,Li/NaNb0.5Ta0.5O3納米粉末中加入(40mL)甲醇,在室溫下超聲分散30min。然后向所得的混合物中加入(4.0mL)H2PtCl6·H2O,并在室溫下超聲分散30min,隨后加熱煮沸30min,待溶液冷卻至室溫后,在120℃干燥4.0h至溶劑全部蒸干為止,將所得的固體混合物充分研磨,隨后在300℃煅燒3.0h,冷卻至室溫,得到Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3納米粉末。
(四)檢測
(1)Pt-NaTaO3,Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3(x=0,0.25,0.5),Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3不同質量比的X粉末衍射(XRD)圖片分析
通過X粉末衍射(XRD)圖(圖1(a-d)發現,Pt-NaTaO3與標準NaTaO3的XRD譜圖(ICSD no.98-001-1550)基本一致并且無任何雜峰,說明制備的NaTaO3比較純凈,無雜質。而Y2SiO5:Pr3+,Li/Pt-NaTaO3的XRD譜圖中特征峰的峰強度明顯變弱,并且在Y2SiO5:Pr3+,Li特征衍射峰位子有小的雜峰出現,說明在Pt-NaTaO3中存在著Y2SiO5:Pr3+,Li。同時隨著Nb的加入,2θ=22.90°和2θ=40.20°特征峰越來越平緩,說明少量的Nb進入了NaTaO3的晶格,形成了NaNbxTa1-xO3。
通過(圖1(e-k))可以發現,Y2SiO5:Pr3+,Li與標準Y2SiO5的XRD譜圖(JCPDS:36-1476)基本吻合。隨著向NaNb0.5Ta0.5O3中加入Y2SiO5:Pr3+,Li的量不斷增多,可以發現譜圖中不僅出現了NaNb0.5Ta0.5O3的特征衍射峰,還出現了Y2SiO5:Pr3+,Li的特征衍射峰,而且Y2SiO5:Pr3+,Li的特征衍射峰越來越明顯。說明Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3中不僅存在NaNb0.5Ta0.5O3還同時存在Y2SiO5:Pr3+,Li,而且Y2SiO5:Pr3+,Li的量不斷增多。
(2)Y2SiO5:Pr3+,Li,Pt-NaTaO3,Y2SiO5:Pr3+,Li/Pt-NaTaO3,Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3的掃描電鏡(SEM)照片分析
如圖2所示,由Y2SiO5:Pr3+,Li的掃描電鏡照片可以看出,Y2SiO5:Pr3+,Li是一種不規則的橢球形的微晶。由Pt-NaTaO3掃描電鏡照片可以看到粒徑大約為200nm的均勻的立方狀構型,屬于NaTaO3的典型的晶狀。NaTaO3納米粒子的表面有顏色較淺的顆粒物。說明Pt粒子附著在了NaTaO3納米粒子的表面。掃描電鏡照片Y2SiO5:Pr3+,Li/Pt-NaTaO3中在立方狀的NaTaO3納米粒子的表面除了有顏色較淺的Pt顆粒物外,還附著著顆粒較大的球狀粒子,說明Y2SiO5:Pr3+,Li與NaTaO3納米粒子復合在了一起。同時可以看到明顯的團聚現象,可能是由于后處理的結果。此外,掃描電鏡照片圖Y2SiO5:Pr3+,Li/Pt-NaTaO3和圖片Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3對比可以看出,它們有同樣大小的粒徑,但是在Nb加入后可以更好地維持立方狀形態。
(3)Y2SiO5:Pr3+,Li,Y2SiO5:Pr3+,Li/Pt-NaTaO3,Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3的能量彌散X射線分析(EDAX)圖片分析
如圖3所示,由Y2SiO5:Pr3+,Li能量彌散X射線分析圖片可以看出,Y、Si、O、Pr元素的特征峰組成了上轉光劑Y2SiO5:Pr3+,Li的特征峰。圖中未看到Li元素的特征峰,可能是由于Li元素的含量特別少或者被其他峰掩蓋。此外,圖中給出的原子比與Y2SiO5:Pr3+,Li中各原子的原子比基本一致,說明制備得到的上轉光劑就是Y2SiO5:Pr3+,Li。
由Y2SiO5:Pr3+,Li/Pt-NaTaO3能量彌散X射線分析圖片可以看出,制備的催化劑中包含了Y2SiO5:Pr3+,Li、Pt和NaTaO3,通過計算,催化劑中每種物質的物質的量與當初的投料比基本一致。
由Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3能量彌散X射線分析圖片可以看出,制備的催化劑中包含了Y2SiO5:Pr3+,Li、Pt和NaNb0.5Ta0.5O3,通過計算,催化劑中每種物質的物質的量與當初的投料比基本一致。
(4)Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3的X射線光電子能譜(XPS)圖片分析
如圖4a-圖4j所示,由X射線光電子能譜圖片(圖4a)可以看出,此催化劑包含Y、Si、O、Pr、Li、Pt、Na、Nb和Ta元素。X射線光電子能譜圖片(圖4b~j)表明了Y2SiO5:Pr3+,Li/Pt-Na Nb0.5Ta0.5O3中各元素的化合價和鍵合情況。X射線光電子能譜(圖4f)在206.0eV和206.3eV出峰證明Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3中存在Nb5+,說明Nb5+替代了Ta5+進入了NaTaO3的晶格,與合成的催化劑情況相符。
(5)Y2SiO5:Pr3+,Li的紫外可見吸收光譜(UV-Vis)圖片和光致發光譜(PL)圖片分析
如圖5a-5c所示,由紫外可見吸收光譜圖片(圖5a)可以發現在443nm和482nm有兩個較明顯的吸收峰。表明此上轉換發光材料Y2SiO5:Pr3+,Li在可見光區(400nm~800nm)有吸收,可以吸收可見光。
紫外可見吸收光譜圖片(圖5b,5c))展示了Y2SiO5:Pr3+,Li分別在443nm和482nm的激發下的發射光譜,發射光譜在220-320nm出現了不連續的顯著的發射峰。表明上轉換發光材料Y2SiO5:Pr3+,Li能夠吸收可見光而發射紫外光,可以有效地將可見光轉化為紫外光。
實施例2自組裝高效光催化劑Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3在光催化水解制氫中的應用
(一)光照時間對光催化分解水制氫的影響
實驗條件:200mg的Pt-NaTaO3(鉑的負載量為0.25%)納米粉末、280mg的Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3(x=0,0.25,0.5)(Y2SiO5:Pr3+,Li與NaNbxTa1-xO3的質量比為3:7,鉑的負載量為0.25%)納米粉末和500mL的甲醇水溶液(10%)。在溫度25℃和壓力101325Pa下,用4個105W的三基色(紅,黃,綠)燈模擬太陽光進行光照,光照強度為10.0mW·cm-2,光照時間0.0-5.0h。
結果如圖6所示,隨著光照時間的延長,Pt-NaTaO3與Y2SiO5:Pr3+,Li/Pt-NaNbxTa1-xO3(x=0,0.25,0.5)光催化分解水制得H2的量也隨之增加,Y2SiO5:Pr3+,Li/Pt-NaTaO3產生H2的量明顯多于Pt-NaTaO3產生H2的量,由此可見,加入上轉換發光材料(Y2SiO5:Pr3+,Li)可以大幅度的提高光催化分解水制氫的效率。同時,隨著Nb的加入產生H2的量也在增加,在本實驗中當x=0.5時產氫量達到最大,所以Nb的加入也可以大幅度提高光催化分解水制氫的效率。
(二)Y2SiO5:Pr3+,Li的不同加入量對光催化分解水制氫效率的影響
實驗條件:200mg、240mg、280mg、320mg、360mg、400mg的Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3納米粉末(對應的Y2SiO5:Pr3+,Li與NaNb0.5Ta0.5O3的質量比為0.0:1.0,0.2:1.0,0.4:1.0,0.6:1.0,0.8:1.0和1.0:1.0)和500mL的甲醇水溶液(10%)。在溫度25℃和壓力101325Pa下,用4個105W的三基色(紅,黃,綠)燈模擬太陽光進行光照,光照強度為10.0mW·cm-2,光照時間5.0h。
結果如圖7所示,隨著Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3納米光催化劑中Y2SiO5:Pr3+,Li含量的不斷增加,光催化分解水制得H2的量先增加后減少,當Y2SiO5:Pr3+,Li與NaNb0.5Ta0.5O3的質量比為0.4:1.0時,產生H2的量最多。說明適當的Y2SiO5:Pr3+,Li與NaNb0.5Ta0.5O3的比例可以大幅度的提高光催化劑的活性,使光催化水解制得氫氣的量大幅度增加。
(三)重復利用性考察
280mg的Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(Y2SiO5:Pr3+,Li與NaNb0.5Ta0.5O3的質量比為0.4:1.0,鉑的負載量為0.25%)納米粉末和500mL的甲醇水溶液(10%)。在溫度25℃和壓力101325Pa下,用4個105W的三基色(紅,黃,綠)燈模擬太陽光進行光照,光照強度為10.0mW·cm-2,光照時間0.0-4.0h。記下氫氣的產量,放出氫氣,避光一小時,再重復上述實驗三次。
結果如圖8所示,隨著Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(0.4:1.0)的重復利用次數的增加,產生H2的量稍有減少,幾乎不影響H2的產量。所以可見光光催化劑Y2SiO5:Pr3+,Li/Pt-NaNb0.5Ta0.5O3(0.4:1.0)性質較穩定,重復利用性良好。
- 還沒有人留言評論。精彩留言會獲得點贊!