寬熒光光譜和MRI雙影像功能微球示蹤間充質干細胞及應用的制作方法
本發明涉及納米熒光探針和干細胞技術領域,尤其涉及一種寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞及應用。
背景技術:
目前,骨質疏松癥、骨質疏松性骨折等疾病已經受到廣泛關注的全球性公共健康問題,早期準確的診斷、合理的治療以及治療效果監測對預防或降低骨質疏松導致的脆性骨折至關重要。骨質疏松癥的發病機理尚不明確,一般認為是由于骨穩態平衡被打破,破骨細胞和成骨細胞數目和功能失衡,骨吸收大于骨形成,而最終引起骨質疏松。骨質疏松癥常伴間充質干細胞增殖和成骨分化能力的下降,成骨細胞成骨能力降低。從而導致骨量減少,局部出現骨質疏松性骨缺損。
人臍帶間充質干細胞(mscs)由新生兒臍帶分離培養,來源豐富,取材方便。體外培養、體內植入均有多向分化潛能、增殖分化能力強、免疫原性低等特性,是骨組織工程中修復骨缺損的理想種子細胞。
近年來,尋求植入體內的人間充質干細胞標記和示蹤方法,并且辨別受體中人間充質干細胞的生存情況,仍然是當今觀察和評估干細胞應用于骨缺損修復的熱點研究問題。大量研究表明將人間充質干細胞植入活體內,促進間充質干細胞成骨分化,改善骨質疏松部位的骨結構,有效修復疾病、創傷導致的骨或軟骨缺損,在未來骨質疏松癥的治療中有著廣泛的應用價值。
目前,具有優良光學特性并且運用于光學成像的納米材料包括金納米顆粒、量子點、多孔二氧化硅納米顆粒、納米碳管、聚合物熒光微球等,其中熒光微球示蹤的優越性在于:穩定形態結構,粒徑分布集中(50-300nm);穩定而高效的發光效率;具有優良的生物降解性和生物相容性;小分子熒光素體內代謝率大大降低。因此,熒光微球示蹤在分子影像技術領域得到廣泛關注和高度重視。
熒光共振能量轉移(fret)是指在供體(donor)基團受到激發后,偶極子介導的能量從供體轉向受體(acceptor),光子未曾介入該過程,因此這一過程是非輻射性的。在供體分子被激發后,如果受體分子與供體分子距離合適(小于10nm),處于激發狀態下的供體會將能量轉移給受體,誘使受體激發,在這個轉移過程中,不會涉及到光子的發射和重新吸收。常用的熒光素如香豆素、吖啶橙、羅丹明、藻紅蛋白之間能依次發生fret效應,已被廣泛應用于熒光探針等領域。
技術實現要素:
為解決上述技術問題,本發明的目的是提供一種寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞及應用,本發明的微球能提供寬熒光光譜和mri雙影像功能,減少動物體內應用時的自體背景熒光的干擾,將所制微球與間充質干細胞共培養,可對其進行示蹤,并用于骨缺損、骨質疏松性骨缺損的修復和治療。本申請中,熒光光譜即為公知的熒光發射光譜。
本發明提供了一種寬熒光發射光譜和mri雙影像功能微球示蹤間充質干細胞,間充質干細胞內吞有寬熒光發射光譜和mri雙影像功能微球,寬熒光光譜和mri雙影像功能微球包括以下質量分數的各組分:聚合物70-99.9%,熒光素0.05-20%,釓劑0.05-10%;聚合物為聚乙丙交酯-聚乙二醇共聚物或聚苯乙烯。微球的粒徑為50-300nm。
上述微球中,聚合物作為熒光素和釓劑的載體。優選地,聚乙丙交酯-聚乙二醇共聚物的分子量為10000-100000g/mol,其中聚乙二醇的分子量為2000-5000g/mol,該材料生物相容性好,可降解。聚苯乙烯為交聯的聚苯乙烯微球,其表面還可帶有羧基或氨基。聚苯乙烯微球微球的粒徑為50-200nm,粒徑相對標準偏差<10%。
進一步地,微球表面還偶聯有修飾化合物,修飾化合物為聚精氨酸、聚賴氨酸、聚酰亞胺或聚乙二胺。聚精氨酸的的重復單元為9。聚酰亞胺的分子量可選擇25kg/mol。微球表面的修飾化合物可增加微球進入干細胞的比例,提高微球標記干細胞的熒光亮度。
進一步地,熒光素為香豆素、吖啶橙、羅丹明、藻紅蛋白和吲哚菁綠中的兩種或三種。優選地,熒光素為香豆素和吖啶橙的組合,吖啶橙、羅丹明和藻紅蛋白的組合,藻紅蛋白和吲哚菁綠的組合。熒光素之間能發生熒光共振能量轉移效應(fret)。
進一步地,釓劑為釓-二乙三胺五乙酸(gd-dtpa)。釓劑具有mri成像功能。
進一步地,當聚合物為聚乙丙交酯-聚乙二醇共聚物時,寬熒光光譜和mri雙影像功能微球的制備方法包括以下步驟:
(1)將聚乙丙交酯-聚乙二醇共聚物和熒光素溶解于有機溶劑,作為油相,將釓劑溶于水,作為內水相,將聚丙烯酸和聚乙烯醇溶于水,作為外水相;
(2)通過復乳法利用油相、內水相和外水相制備微球,除盡油相的有機溶劑,得到寬熒光光譜和mri雙影像功能微球。
進一步地,在步驟(1)中,有機溶劑為氯仿、二氯甲烷和二氯乙烷中的一種或幾種。在步驟(2)中,復乳法操作步驟如下:首先將油相、內水相制成初乳,將初乳加入外水相制得水/油/水的復乳,待油相的有機溶劑揮發除盡,即得到熒光和mri雙影像功能微球。
進一步地,當聚合物為聚苯乙烯時,寬熒光光譜和mri雙影像功能微球的制備方法包括以下步驟:
將熒光素和釓劑溶于有機溶劑中,向其中加入聚苯乙烯微球,聚苯乙烯納米微球的粒徑范圍50-200nm,粒徑相對標準偏差<10%;反應24h后除掉有機溶劑,洗滌后,得到寬熒光光譜和mri雙影像功能微球。熒光素為吖啶橙、羅丹明、吲哚菁綠。有機溶劑為氯仿和異丙醇的混合物,二者體積比為1:3。洗滌時,采用酒精和水清洗微球直至上清液無明顯顏色
進一步地,還包括以下步驟:通過氨酯化反應,將微球與修飾化合物的氨基偶聯。
氨酯化反應,可以通過偶聯劑edc(1-(3-二甲氨基丙基)-3-乙基碳二亞胺)輔助進行。也可以通過戊二醛為交聯劑,將修飾化合物的氨基與含氨基的聚苯乙烯微球偶聯。
進一步地,寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞的制備方法包括以下步驟:
將寬熒光光譜和mri雙影像功能微球與細胞培養液混合均勻,得到微球溶液,并在4℃下孵育24h后,加入到已貼壁的間充質干細胞中,在37℃下培養1-4天,用純培養基洗滌,除去未進入間充質細胞的微球,得到寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞。
進一步地,微球溶液的濃度為0.2-1.0mg/ml。
本發明還公開了上述寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞在制備骨缺損修復和/或骨質疏松疾病的示蹤劑和/或治療劑中的應用。在應用過程中,間充質干細胞具有熒光和mri雙影像成像功能。
借由上述方案,本發明至少具有以下優點:
熒光共振能量轉移法(fret)作為1.0-10.0nm距離范圍內的光學分子尺,具有高分辨率、高靈敏度、簡單方便等優點。采用可發生fret效應的熒光素組合,微球的熒光發射光譜變寬,利用供體熒光素的最佳激發波長,通過fret效應使受體熒光素發出更強的熒光,因自體熒光波長距離激發光較近,基于fret效應設計的熒光素組合可發出波長更長的熒光,從而削弱自發熒光的影響,降低體內應用時的背景熒光干擾,使微球熒光信號的體內可分辨度提高。核磁共振(mri)已應用于全身各系統的影像診斷。效果最佳的是顱腦,及其脊髓、心臟大血管、關節骨骼和軟組織等。mri進行定性及半定量的診斷,可作多個切面圖,空間分辨率較高,優于其他x線影像、二維超聲、核素及ct檢查。本發明的微球同時結合了熒光和mri影像的優點。
本發明使用的間充質干細胞(mscs),在含有微球的培養液(mscm)中孵育2-4天后,微球被mscs吞噬且在細胞內均勻分布,該細胞能夠用于體內示蹤。與熒光素和釓劑直接進行細胞標記相比,熒光素和釓劑被聚合物負載后,微球具備低細胞毒性、粒徑分布均勻(160-220nm)、易吞噬、更加穩定而高效地在體內循環、良好的生物降解性和生物相容性、提高圖像信號比等特性,同時,更有利于發揮寬熒光發射光譜素本身優良的熒光穿透特性,降低對生物組織的損傷。
本發明為寬熒光發射光譜素和釓劑在示蹤mscs方面提供了一種直觀簡便、動態無創的方案,能進一步用于深入觀察和證實骨質疏松的發病機制,以及評估mscs在骨質疏松性骨質缺損修復中的應用、骨質疏松的分子影像領域具有廣泛的運用前景。
上述說明僅是本發明技術方案的概述,為了能夠更清楚了解本發明的技術手段,并可依照說明書的內容予以實施,以下以本發明的較佳實施例并配合附圖詳細說明如后。
附圖說明
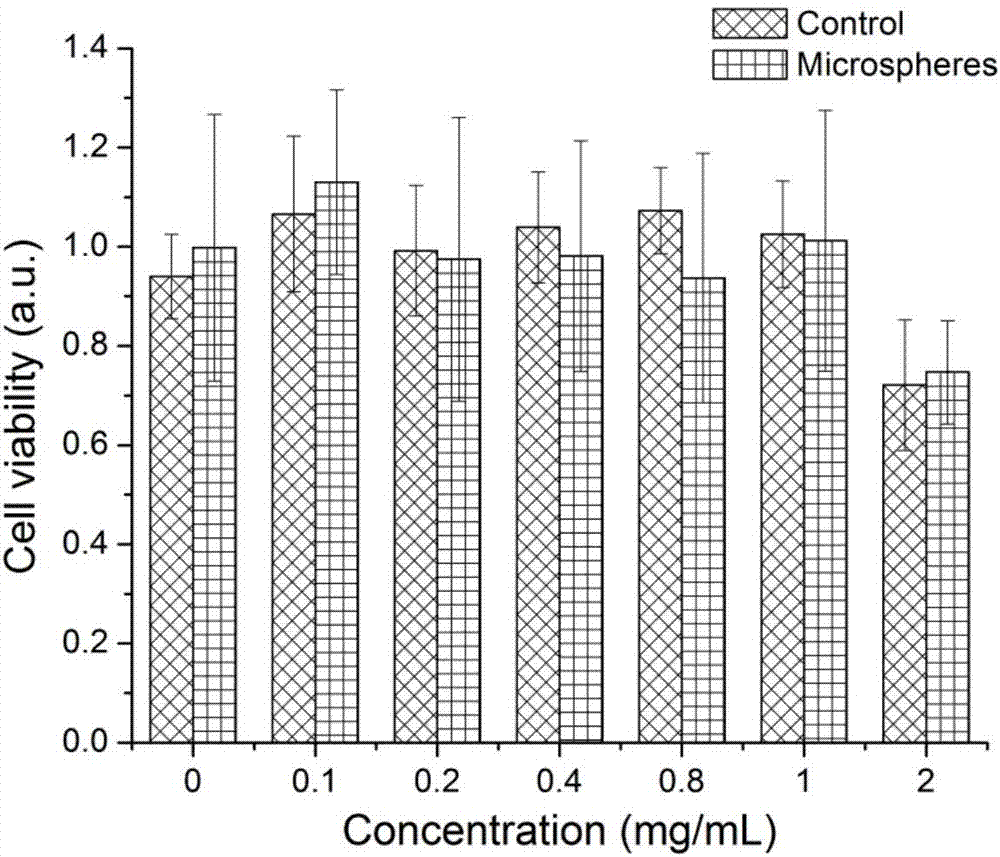
圖1圖示了不同濃度微球溶液對細胞生存率的影響結果;
圖2為使用含本發明微球的培養液培育間充質干細胞后,于單光子激光共聚焦顯微鏡下拍攝的熒光圖片;
圖3為實施例2中對照組于單光子激光共聚焦顯微鏡下拍攝的熒光圖片;
圖4圖示了本發明微球示蹤的間充質干細胞注入大鼠顱骨后的ct掃描結果。
具體實施方式
下面結合附圖和實施例,對本發明的具體實施方式作進一步詳細描述。以下實施例用于說明本發明,但不用來限制本發明的范圍。
本發明使用的間充質干細胞(mscs)為人臍帶來源的間充質干細胞(hucmscs),該細胞能夠提供的強大自我更新能力和增值分化能力。
實施例1
本發明的寬熒光光譜和mri雙影像功能微球的制備方法,包括以下步驟:
(1)稱量5mg吖啶橙、10mg羅丹明和25mg聚乙丙交酯-聚乙二醇共聚物(plga-peg)混合,用1ml氯仿/異丙醇(體積比為1:3)溶液溶解,得到油相。準備100μl100mg/ml的gd-dtpa造影劑水溶液作內水相。
(2)將步驟(1)得到的油相和內水相超聲混合5次,每次2s,(100w,bilon92-ii),得到初乳劑。
(3)向步驟(2)的產物加入4ml聚乙烯醇(pva)水溶液(5wt%),超聲混合5次(2s,100w)形成復乳劑。
(4)將步驟(3)的產物稀釋到聚丙烯酸(paa)水溶液中(5wt%,40ml),室溫下過夜攪拌、避光揮發。
(5)用50ml高速離心管收集步驟(4)含微球溶液,先用無水乙醇清洗一次,高速離心(14500rpm,20min),棄上清,超聲均勻,再加入純水清洗,高速離心(12000rpm,10min),重復2-3次,最終所得沉淀即為寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞。
(6)將步驟(5)得到的微球溶于純水,得到不同濃度的微球水溶液。
上述制備的微球中,包含以下含量的各組分:聚合物70%,熒光素20%,釓劑10%。
實施例2
(1)將hucmscs正常傳代培養,在普通細胞培養皿皿底鋪相應規格爬片。
(2)將微球(如實施例1制備的微球)與mscm培養基混合,配成微球培養液(0.2-1mg/ml),置于培養箱中(37℃,5%co2)孵育24h。
(3)24h后,間充質干細胞貼壁,吸除培養液,加入相同體積的培養液(0.2-1mg/ml),置于培養箱(37℃,5%co2),繼續培養2-4天,優選2天。
微球對mscs細胞的毒性影響如圖1所示,對照組為純聚乙丙交酯-聚乙二醇共聚物微球,在1.0mg/ml濃度以下,對照組和熒光和mri雙功能微球組均未觀察到明顯毒性,濃度為2mg/ml時,兩組細胞死亡率明顯增加,因此使用時,微球濃度范圍在1mg/ml以下為宜。
(4)2-4天后,去除培養液,pbs清洗2遍后,浸沒在5%多聚甲醛中30min,再用pbs清洗兩遍,將皿底爬片,制成玻片標本。
(5)利用nuance多光譜影像系統,紫外光激發,采集圖片。
(6)單光子激光共聚焦顯微鏡下觀察玻片標本,選擇激發光波長488nm,放射波長接收范圍500-545nm(綠色green)和550-580nm(紅色red),采集圖片,結果如圖2所示,圖2表明,微球的熒光素間發生了熒光能量共振轉移,采用488nm激光時,細胞具有極強的紅色熒光。同時以負載吖啶橙的微球被間充質干細胞內吞后的干細胞組作為對照組,按上述方法拍攝熒光圖片(圖3),其熒光亮度(紅光)很弱,與對照組相比,本發明的干細胞的紅色熒光強5-10倍。結合熒光照片數據,微球的濃度在0.2mg/ml以上為佳,可以觀察到較明顯的熒光信號。
因此,結合微球示蹤mscs的熒光強度和毒性數據,使用時,微球的濃度為0.2-1mg/ml為宜。
(7)雙光子激光共聚焦顯微鏡下觀察玻片標本,激發波長880nm,觀察攝片。
(8)取適量微球溶液注入玻璃細管中(直徑2mm,長度10cm,液高2-3cm),進行mri掃描,對比信號強度。
(9)若步驟(7)(8)得到的熒光強度和信號強度達到示蹤標準,將寬熒光光譜和mri雙影像功能微球標記的hucmscs(5×105-5×106)注入大鼠局部骨缺損區域(顱骨),雙光子共聚焦顯微鏡連續動態觀察,比較熒光/信號強弱和分布,mri掃描評估局部骨缺損修復狀況。結果如圖4,與對照組(control)相比,本發明的間充質干細胞骨缺損愈合更好,修復效果更佳。
實施例3
本發明的寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞的制備方法,包括以下步驟:
(1)稱量0.1mg吖啶橙、0.1mg羅丹明和25mg聚乙丙交酯-聚乙二醇共聚物混合,用1ml氯仿/異丙醇(體積比為1:3)溶液溶解,得到油相。準備10μl1mg/ml的gd-dtpa造影劑水溶液作內水相。
(2)將步驟(1)得到的油相和內水相超聲混合5次,每次2s(100w,bilon92-ii),得到初乳劑。
(3)向步驟(2)的產物加入4mlpva水溶液(5wt%),超聲混合5次(2s,100w)形成復乳劑。
(4)將步驟(3)的產物稀釋到paa水溶液中(5wt%,40ml),室溫下過夜攪拌、避光揮發。
(5)用50ml高速離心管收集步驟(4)含微球溶液,先用無水乙醇清洗一次,高速離心(14500rpm,20min),棄上清,超聲均勻,再加入純水清洗,高速離心(12000rpm,10min),重復2-3次,最終所得沉淀即為寬熒光發射光譜和mri雙影像功能微球示蹤間充質干細胞。
(6)將步驟(5)得到的微球溶于純水,得到不同濃度的微球水溶液。
上述制備的微球中,包含以下含量的各組分:聚合物99.9%,熒光素0.05%,釓劑0.05%。
實施例4
羧基化聚苯乙烯微球由bangslab公司提供,粒徑100nm,相對標準偏差(cv)約為5%;向氯仿/異丙醇(1/3)的溶液中加入聚苯乙烯,氯仿/異丙醇溶液中含有2-4mg/ml吖啶橙、2-4mg/ml羅丹明、2-4mg/ml吲哚菁綠和1-10mg/mlgd-dtpa,反應24h并同時揮發溶劑,待溶劑完全揮發后,用酒精和水清洗微球直至上清液無明顯顏色,得到寬熒光發射光譜和mri雙影像功能微球。
上述制備的微球中,包含以下含量的各組分:聚合物97.5%,熒光素2%,釓劑0.5%。
同樣熒光素用量條件下,可以明顯觀察到聚苯乙烯微球的熒光亮度更高,因聚苯乙烯對熒光素有更強的吸附作用。同樣的,以聚苯乙烯制備的微球對mscs的毒性和以plga類聚合物制備的微球的毒性接近,而以聚苯乙烯制備的微球示蹤的mscs熒光信號提高1-2倍,但mri信號要弱20-50%。
實施例5
本發明的寬熒光發射光譜和mri雙影像功能微球示蹤間充質干細胞的制備方法,包括以下步驟:
(1)稱量2mg吖啶橙、2mg羅丹明、2mg吲哚菁綠,與25mg聚乙丙交酯混合,再用1ml氯仿溶解,得到油相。準備100μlgd-dtpa造影劑作內水相。
(2)將步驟(1)得到的油相和內水相超聲混合5次(2s,100w,bilon92-ii),得到初乳劑。
(3)向步驟(2)的產物加入4mlpva水溶液(5wt%),超聲混合5次(2s,100w)形成復乳劑。
(4)將步驟(3)的產物稀釋到paa水溶液中(5wt%,40ml),室溫下過夜攪拌、避光揮發。
(5)用50ml高速離心管收集步驟(4)含微球溶液,先用無水乙醇清洗一次,高速離心(14500rpm,20min),棄上清,超聲均勻,再加入純水清洗,高速離心(12000rpm,10min),重復2-3次,最終所得微球沉淀溶于1ml純水。
(6)均勻抽取10μl步驟(5)溶液,烘干后稱量,計算得到步驟(5)微球溶液濃度,以聚乙丙交酯制備的寬熒光發射光譜和mri雙影像功能微球的濃度為1-2mg/ml。
(7)抽取100μl所制備的微球溶液,用純水稀釋成2ml,在納米粒度及zeta電位分析儀(zetasizernanozs90)測得微球粒徑,所制微球粒徑分布范圍為200-300nm。
實施例6
本發明不同濃度的微球對細胞生存率的影響情況的測試方法如下:
(1)96孔板每空接種5000個細胞。
(2)將實施例1所制得微球,用培養液稀釋成濃度分別為0.2、0.4、0.8、1、2mg/ml微球溶液,錫箔紙包裹,4℃冰箱過夜孵育。
(3)在不同濃度實驗組和空白對照組中分別相應的微球培養液和培養液,分別培養24h、48h。
(4)用多功能酶標儀(synergy2)測得od值,與空白對照相比,統計分析各組細胞存活率,結果顯示2mg/ml微球溶液細胞生存率低于空白對照組。
圖1為不同濃度微球溶液對細胞生存率的影響結果,對照組為純聚乙丙交酯-聚乙二醇共聚物空白微球(沒有染料和釓劑),在1.0mg/ml濃度以下,對照組和本發明的微球均未觀察到明顯毒性,濃度為2mg/ml時,兩組細胞死亡率明顯增加,因此微球的用量在1.0mg/ml濃度以下為宜。
本發明微球的示蹤情況測試方法如下:
(1)3月齡未孕雌性sd大鼠6只行去勢手術切除雙側卵巢,術后飼養3個月。
(2)sd大鼠3.6%水合氯醛麻醉后,切開股骨外皮膚,暴露骨膜,用直徑為3mm的打孔電鉆在股骨皮質上,緩慢勻速鑿出深度1mm的圓形骨缺損區域。
(3)將寬熒光發射光譜和mri雙功能微球標記好的hucmscs取5×105-5×106個細胞,用30μlpbs重懸,1ml注射器抽取后注入到股骨皮質圓形缺損區域,縫合皮膚。
(4)小動物熒光影像系統、micro-ct、mri定期掃描骨缺損部位的骨質修復狀況。
通過連續觀察骨缺損區域的熒光變化和骨修復情況,綜合多種影像手段,可以闡明示蹤干細胞對骨缺損區域的修復過程,得出干細胞修復骨缺損的修復機制。
圖4圖示了本發明微球示蹤的間充質干細胞注入大鼠顱骨后的ct掃描結果,與對照組(control,未做任何處理)相比,本發明微球示蹤mscs組骨缺損處骨小梁結構更為致密,骨間隙變窄,骨密度增高,修復后骨缺損區域面積僅為對照組的20-40%左右,證明該組對于骨缺損修復效果更佳。
實施例7
此外,微球表面還可以連接一些修飾化合物,修飾化合物為聚精氨酸、聚賴氨酸、聚酰亞胺或聚乙二胺。修飾化合物能夠提高微球的干細胞內吞量。具體修飾方法如下:
向實施例1或4制備的微球溶液中加入聚精氨酸、聚酰亞胺或聚乙二胺,通過氨酯化反應,修飾化合物表面的氨基與微球表面的羧基反應后連接到微球表面。氨酯化反應,可以通過偶聯劑edc(1-(3-二甲氨基丙基)-3-乙基碳二亞胺)輔助進行。也可以通過戊二醛為交聯劑,將修飾化合物的氨基與含氨基的聚苯乙烯微球偶聯。將最終所得的微球與間充質干細胞用實施例2中的方法進行培養,得到寬熒光光譜和mri雙影像功能微球示蹤間充質干細胞。與未修飾組化合物的微球相比,修飾了化合物的微球示蹤的間充質干細胞的熒光強度可增加50-100%,mri亮度可增加30-100%。
以上所述僅是本發明的優選實施方式,并不用于限制本發明,應當指出,對于本技術領域的普通技術人員來說,在不脫離本發明技術原理的前提下,還可以做出若干改進和變型,這些改進和變型也應視為本發明的保護范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!