一種結核桿菌PGL?tb1寡糖綴合物及其制備方法與應用與流程
本發明涉及一種結核桿菌PGL-tb1寡糖綴合物及其制備方法與應用,屬于結核疫苗研制技術領域。
背景技術:
結核病是由結核分枝桿菌(Mycobacterium tuberculosis,Mtb)感染引起的慢性傳染病。全世界大概有1/3的人感染MTB,其中5%~10%的感染者發展為TB患者,每年大約有200萬結核病患者死亡。結核病化學治療已是比較完善的治療控制結核病的有效方法。但是,隨著原發及獲得性耐多藥結核病以及廣泛耐藥結核病的增多,目前的結核病化學治療面臨著各種挑戰。化療雖然能改善患者的病情,延長生命,卻給患者帶來痛苦大、毒副作用強及嚴重不良反應等缺點。至今,卡介苗(BCG)仍是預防結核病唯一可用疫苗,但其免疫保護效果不穩定,保護率從0到80%。對于有免疫缺陷的患者,接種卡介苗有可能導致結核的感染(Lancet Infect.Dis.2004:584)。目前,越來越多的國家面臨多重耐藥菌株感染、HIV合并感染,新型結核疫苗的研發迫在眉睫。
研究表明,結核分枝桿菌細胞壁上特殊的糖復合物在維持細胞壁結構和致病過程中發揮著極其重要的作用。酚糖脂(phenolic glycolipid,PGL)位于分枝桿菌細胞壁的最外層,主要由某些致病分枝桿菌所產生,其中結核分枝桿菌僅在某些臨床分離株中含有酚糖脂。一般認為酚糖脂與分枝桿菌的毒力有關,結構保守(Infect Immun,2012,80:1381)。酚糖脂包含有一個由長鏈β二醇結構形成的脂質核心,該二醇結構在正常情況下與多甲基分枝的脂肪酸形成二酯。該脂質核心在ω末端與一個糖基化的芳香環核心相連。依菌株不同,PGL含有1~4個糖類殘基,其中大部分為O-甲基化的脫氧糖。僅少量結核分枝桿菌的菌株可以合成PGL-tb,且這些菌株合成的PGL-tb糖類組分主要形式為2,3,4-三-O-甲基-L-吡喃巖藻糖基-α-(1-3)-L-吡喃鼠李糖基-α-(1-3)-2-O-甲基-L-吡喃鼠李糖。
動物實驗表明,用可產生PGL的W-Beijing HN878臨床分離株感染小鼠后,與不產生PGL的基因株相比,前者實驗小鼠的中位生存期下降了90天,毒力較強(Infect Immun,2008,76:3027),這種酚糖脂是結核桿菌的毒力因子之一。但是,由于這類天然糖抗原結構復雜性和不穩定性,以及從致病菌中直接分離純化的困難,為此,大量合成這種寡糖分子對于在分子水平上研究其功能具有非常重要的意義。因此,可以根據PGL-tb1的結構特征,合成PGL-tb1中的糖基部分,并將其作為半抗原與載體偶聯,制備糖綴合物疫苗。目前,只有荷蘭格羅寧根大學的Minnaard小組于2012年首次報道了PGL-tb1酚糖脂的全合成(Angew.Chem.Int.Ed.2012,51:11774)。以結核分枝桿菌PGL-tb1糖基部分為半抗原,與載體偶聯制備寡糖綴合物疫苗,尚未見相關報道。
技術實現要素:
本發明針對現有技術的不足,提供一種結核桿菌PGL-tb1寡糖綴合物及其制備方法與應用,其中的寡糖是結核桿菌細胞壁中酚糖脂的糖基部分。
本發明通過如下的技術方案來實現:
一種結核桿菌PGL-tb1寡糖綴合物,結構通式如下:
式(Ⅱ)
其中,寡糖是如下通式(Ⅰ)中的任一寡糖:
式(Ⅰ)
式(Ⅰ)和式(Ⅱ)中,a是0到4中的任意一個整數,b是0到4中的任意一個整數,c是0到4中的任意一個整數,m是0到30中的任意一個整數,
R1,R2,R3,R4,R5,R6,R7選自-H和-CH3;
X選自:-CH2、-NH-、-O-、-C(O)-、-S-、或
連接體是寡糖與載體直接或間接連接后得到的結構部分;
n是載體連接的寡糖的數量,n是0到30中的任意一個整數;
載體選自:牛血清白蛋白(BSA)、人血清白蛋白(HSA)、血藍蛋白(KLH)、破傷風毒素(TT)、白喉毒素無毒突變體(CRM197)和單磷酰化的脂質A(LipidA)之一。
根據本發明優選的,所述結核桿菌PGL-tb1寡糖綴合物的結構通式為如下之一:
式中,j1是0到10中的任意一個整數,j2是0到10中的任意一個整數,j3是0到10中的任意一個整數,n是0到30中的任意一個整數。
根據本發明優選的,所述載體選自:牛血清白蛋白、人血清白蛋白、血藍蛋白、破傷風毒素、白喉毒素無毒突變體和單磷酰化的脂質A之一。
本發明進一步優選的,所述結核桿菌PGL-tb1寡糖綴合物的結構通式如下:
本發明進一步優選的,所述結核桿菌PGL-tb1寡糖綴合物的結構通式如下:
本發明進一步優選的,所述結核桿菌PGL-tb1寡糖綴合物的結構通式如下:
本發明進一步優選的,所述結核桿菌PGL-tb1寡糖綴合物的結構通式如下:
另外,本發明涉及所述結核桿菌PGL-tb1寡糖綴合物的制備方法,具體技術路線如下:
將合成的帶有保護基的三糖與氯己炔通過Sonogashira偶聯反應進行連接,然后用疊氮基團取代氯原子,之后進行一步催化氫化反應,此步將脫去芐基保護基,同時將化合物中的炔基還原,疊氮基還原成氨基。根據載體的性質,選擇連接體,將產物與連接體進行偶聯,即寡糖的活化,最后,將活化的寡糖連接到載體上,分離純化后得到PGL-tb1寡糖綴合物,。
上述制備方法,只表示制備本發明的式(Ⅱ)化合物的方法之一例子。本發明化合物的制備方法并不僅限于這些方法,在本說明書的實施例中,由于更具體地說明了本發明化合物的制備方法,所以,本領域的人員,根據上述說明和具體實施例的說明,根據需要,對此加以適當的修改,就能制造出PGL-tb1寡糖綴合物。
上述結核桿菌PGL-tb1寡糖綴合物在制備結核疫苗中的應用。
本發明所述的結核桿菌PGL-tb1寡糖綴合物中,寡糖的化學結構是明確且單一的,而非混合物,可以通過化學方法大量合成,通過設計連接體與載體偶聯,制備抗原,能夠解決卡介苗免疫保護力低和不穩定的問題,對某些免疫力低下的特殊人群同樣會產生較好的免疫效果,而且能夠避免抗結核化學藥品大量使用帶來的細菌耐藥性問題。
附圖說明
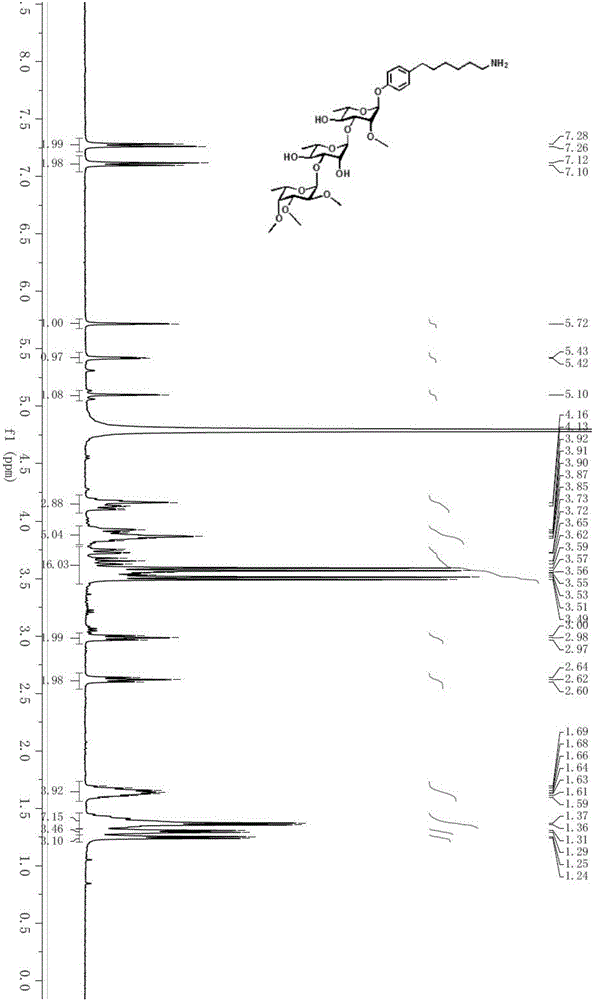
圖1是化合物A3的1HNMR譜圖;
圖2是A3-CRM197寡糖綴合物的SDS-PAGE圖;
圖3是A3-CRM197寡糖綴合物的特異性二免抗體滴度圖;
圖4是A3-CRM197寡糖綴合物的特異性三免抗體滴度圖.
具體實施方式
為了更好的理解本發明的技術方案,下面結合實施例作進一步詳細描述,但本發明所保護范圍不限于此。
一種結核桿菌PGL-tb1寡糖綴合物,結構通式如下:
式(Ⅱ)
其中,寡糖是如下通式(Ⅰ)中的任一寡糖:
式(Ⅰ)
式(Ⅰ)和式(Ⅱ)中,a是0到4中的任意一個整數,b是0到4中的任意一個整數,c是0到4中的任意一個整數,m是0到30中的任意一個整數,
R1,R2,R3,R4,R5,R6,R7選自-H和-CH3;
X選自:-CH2、-NH-、-O-、-C(O)-、-S-、或之一;
連接體是寡糖與載體直接或間接連接后得到的結構部分;
n是載體連接的寡糖的數量,n是0到30中的任意一個整數;
載體選自:牛血清白蛋白(BSA)、人血清白蛋白(HSA)、血藍蛋白(KLH)、破傷風毒素(TT)、白喉毒素無毒突變體(CRM197)和單磷酰化的脂質A(LipidA)之一。
根據本發明優選的,所述結核桿菌PGL-tb1寡糖綴合物的結構通式為如下之一:
式中,j1是0到10中的任意一個整數,j2是0到10中的任意一個整數,j3是0到10中的任意一個整數,n是0到30中的任意一個整數。
所述載體選自:牛血清白蛋白、人血清白蛋白、血藍蛋白、破傷風毒素、白喉毒素無毒突變體和單磷酰化的脂質A之一。
上述結核桿菌PGL-tb1寡糖綴合物通用的合成方法,步驟如下:
⑴寡糖與連接體的反應
取三苯基磷(0.07個當量)、碘化亞銅(0.14個當量)和雙三苯基磷二氯化鈀(0.07個當量)溶于三乙胺中,在40℃條件下攪拌反應15分鐘,配置成催化劑,備用。取制備好的寡糖底物和6-氯己炔(10個當量)溶于三乙胺中,然后加入已配置好的催化劑。在40℃條件下攪拌反應2小時。經TLC檢測顯示反應完成,向反應液中加入乙酸乙酯,用2mol/L鹽酸溶液萃取,然后,有機相繼續用飽和氯化鈉溶液萃取,無水硫酸鈉干燥,減壓濃縮,硅膠柱層析分離純化,得到目標產物(所用的洗脫液為石油醚(PE)/乙酸乙酯(EA))。
⑵疊氮化反應
將原料(1個當量)溶于N,N-二甲基甲酰胺(DMF)中,加入疊氮鈉(10個當量)、四丁基碘化銨(TBAI)(1個當量),在60℃油浴條件下攪拌過夜反應,經TLC檢測顯示反應完成。向反應液中加水,二氯甲烷萃取,之后有機相用飽和碳酸氫鈉溶液萃取,合并有機相,繼續用飽和氯化鈉溶液萃取,無水硫酸鈉干燥,經減壓濃縮,硅膠柱層析分離純化,得到目標產物(所用的洗脫液為石油醚(PE)/乙酸乙酯(EA))。
⑶催化氫化
取原料溶于乙酸乙酯和乙醇的混合溶液(乙酸乙酯:乙醇=4:1),在氮氣保護下加入催化量氫氧化鈀碳(Pd(OH)2/C),滴加稀鹽酸,向反應瓶中通入氫氣,置換出氮氣,反應液在氫化反應釜中,攪拌24小時,反應結束后,經TLC檢測顯示反應完成,反應液通過硅藻土抽濾,減壓濃縮,硅膠柱層析分離純化,產物經Sephadex LH20柱子進一步純化,冷凍干燥,得到目標產物(所用的洗脫液為二氯甲烷(DCE)/甲醇(MeOH))。
⑷寡糖綴合物的合成
寡糖的活化:將寡糖溶于乙醇(EtOH)和水(H2O)的混合液中(EtOH:H2O=1:1),加入方酸二乙酯(5個當量),之后每5分鐘滴加飽和碳酸鈉溶液,直至反應液pH=8,室溫下攪拌反應1.5小時。經TLC檢測顯示反應完成,硅膠柱層析分離純化(所用的洗脫液為二氯甲烷(DCE)/甲醇(MeOH))。產物用水溶解后,使用Sephadex LH20柱子進行進一步純化,之后冷凍干燥,得到目標產物。
寡糖蛋白綴合物的合成:按照20:1的摩爾比取活化的寡糖和蛋白(寡糖:蛋白=20:1)溶于緩沖溶液(Na2B4O70.07mol/L,KHCO30.035mol/L,pH9.0)中,室溫靜置72小時。之后,用超濾的方法除去小分子物質,超濾完畢后將蛋白水溶液凍干,得到寡糖-蛋白綴合物。
實施例1
(2,3,4-三-O-甲基-α-L-巖藻糖基)-(1→3)-α-L-鼠李糖基-(1→3)-(1-(6-(4-羥基苯基)-己胺基)-2-O-甲基-α-L-鼠李糖)-CRM197綴合物的合成(PGL-tb1-CRM197)的合成
⑴2,3,4-三-O-甲基-α-L-巖藻糖基-(1→3)-2,4-二-O-芐基-α-L-鼠李糖基-(1→3)-1-(1-氯-6-(4-羥基苯基)-5-己炔)-2-O-甲基-4-芐基-α-L-鼠李糖的(A1)合成
稱取9.9mg三苯基磷(39μmol),14.4mg碘化亞銅(75μmol)和26.4mg雙三苯基磷二氯化鈀(39μmol)溶于重蒸的三乙胺(18mL)中,在40℃條件下攪拌反應15分鐘,配置成催化劑,備用。以2,3,4-三-O-甲基-α-L-巖藻糖基-(1→3)-2,4-二-O-芐基-α-L-鼠李糖基-(1→3)-1-對碘苯基-2-O-甲基-4-芐基-α-L-鼠李糖(1.5g,0.51mmol,參照Angew.Chem.Int.Ed.2012,51:11774的合成方法)和6-氯己炔0.6mL(5.08mmol)溶于6.09mL三乙胺中,然后,加入催化劑12.19mL,在40℃條件下攪拌反應2小時。反應結束后,以PE:EA(2:1)為展開劑,經TLC檢測顯示反應完成,Rf=4.3。向反應液中加入乙酸乙酯(80mL),用鹽酸溶液(2mol/L,2×30mL)萃取,然后,有機相用用飽和食鹽水溶液(30mL)洗滌,無水硫酸鈉干燥,減壓濃縮,硅膠柱層析分離純化(PE:EA從10:1-1:2),最后得淺黃色油狀液體430mg(0.44mmol),產率87%。
⑵2,3,4-三-O-甲基-α-L-巖藻糖基-(1→3)-2,4-二-O-芐基-α-L-鼠李糖-(1→3)-1-(1-疊氮-6-(4-羥基苯基)-5-己炔)-2-O-甲基-4-芐基-α-L-鼠李糖(A2)的合成
取430mg(0.44mmol)化合物A1,按照實施例1中通用合成方法B進行疊氮化反應,將A1溶于DMF中,加入287.4mg(4.44mmol)疊氮鈉,163.2mg(0.44mmol)四丁基碘化銨(TBAI),在60℃油浴條件下攪拌過夜反應,反應結束后,以PE:EA(2:1)為展開劑,經TLC檢測顯示反應完成,Rf=5.3。向反應液中加水,二氯甲烷萃取,之后有機相用飽和NaHCO3水溶液萃取,水洗,合并有機相,用飽和食鹽水溶液洗,無水硫酸鈉干燥,經減壓濃縮,硅膠柱層析分離純化(PE:EA 10:1-1:4),最后得淺黃色油狀液體357mg。產率82.4%。
⑶2,3,4-三-O-甲基-α-L-巖藻糖基-(1→3)-α-L-鼠李糖基-(1→3)-1-對苯己氨基-2-O-甲基-α-L-鼠李糖(A3)的合成
按照通用方法中的步驟⑶催化氫化進行催化氫化,稱取A2150mg,溶于EtOAc-EtOH=4:1(V/V)的溶劑中,加入477.5mg Pd(OH)2/C,滴加0.1mL(2mol/L)稀鹽酸,之后放入氫化反應釜中,反應24h,反應結束后,以DCM-MeOH(7:1)為展開劑,經TLC檢測顯示反應完成,Rf=3.7。反應液通過抽濾,減壓濃縮,硅膠柱層析分離純化DCM-MeOH(25:1~1:1),得到無色油狀液體,產物經Sephadex LH20進一步純化,冷凍干燥,得到白色固體64mg,產率60.8%。1H NMR(400MHz,D2O),見說明書附圖1,δ(ppm):7.27(d,J=8.0Hz,2H),7.11(d,J=8.4Hz,2H),5.72(s,1H),5.42(d,J=3.6Hz,1H),5.10(s,1H),4.21–4.09(m,3H),3.96–3.44(m,22H),2.98(t,2H),2.62(t,2H),1.64(m,4H),1.45-1.32(m,8H),1.30(d,J=6.4Hz,3H),1.25(d,J=6.4Hz,3H).質譜:HRMS(ESI+):m/z:計算值:C34H57NO13Na[M+Na]+,710.3728,實測值:710.3722。
⑷PGL-tb1-CRM197糖綴合物的合成(A3-CRM197)
按通用合成方法步驟⑷的方法合成A3-CRM197綴合物,取716mg CRM197粉末(5%CRM197,95%蔗糖)溶于4mL緩沖溶液(Na2B4O70.07mol/L,KHCO30.035mol/L,pH9.0)中,然后加入10mg化合物A3與方酸二乙酯的結合物,室溫靜置72小時。之后,將反應液加入到15mL超濾離心管(截留分子量30KDa)中,4000轉/分鐘,離心30分鐘,然后加去離子水,再次離心,如此重復7次。冷凍干燥,得到樣品31.4mg。質譜:MALDI-TOF-MS(m/z)60277
A3-CRM197綴合物的十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳(SDS-PAGE),見附圖2,結果表征揭示,與未綴合的CRM197的載體蛋白相比,A3-CRM197綴合物向更高質量的期望位移和條帶展寬。
實施例3
2,3,4-三-O-甲基-α-L-巖藻糖基-(1→3)-α-L-鼠李糖基-(1→3)-1-對苯己氨基-2-O-甲基-α-L-鼠李糖-BSA糖綴合物的合成
取A3(5mg),BSA(20mg)按通用合成方法步驟⑷的方法合成A3-BSA綴合物(23mg)。質譜:MALDI-TOF-MS(m/z)66415
實施例4
寡糖綴合物A3-CRM197的免疫原性抗體滴度測定
實施例1中制備的寡糖綴合物A3-CRM197在小鼠(NIH小鼠,雌性,SPF級)體內進行免疫試驗。采用腹部皮下注射的方式,以寡糖用量計算,分為三個劑量組:0.5μg,2.0μg,5.0μg,分別在第1、14、28天進行免疫。本實驗共設7個組,每組10只,具體如表1所示。
表1實驗動物分組
第2至4組在第二次免疫兩周后采集全血,第5至7組在最后一次免疫兩周后采集全血。制備抗血清研究其免疫原性,用相應寡糖的BSA綴合物作為固定抗原,以酶聯免疫法(ELISA)檢測多糖特異性抗體的滴度,二免和三免的結果分別如圖2和圖3所示。
經過免疫后,小鼠血清中IgG抗體滴度水平顯著增高,免疫應答強烈,而且顯示出劑量依賴性,說明綴合物誘導產生的免疫響應主要是IgG型,屬于T細胞參與的免疫應答,此應答能夠使宿主細胞產生免疫記憶,促進抗體成熟。動物實驗結果說明綴合物A3-CRM197是一種非常有潛力的結核疫苗。
- 還沒有人留言評論。精彩留言會獲得點贊!