蛋白酶體抑制劑在制備降低動物脂含量或脂儲積能力產品中的應用的制作方法
本發明涉及生物醫學領域中蛋白酶體抑制劑在制備降低動物脂含量或脂儲積能力產品中的應用。
背景技術:
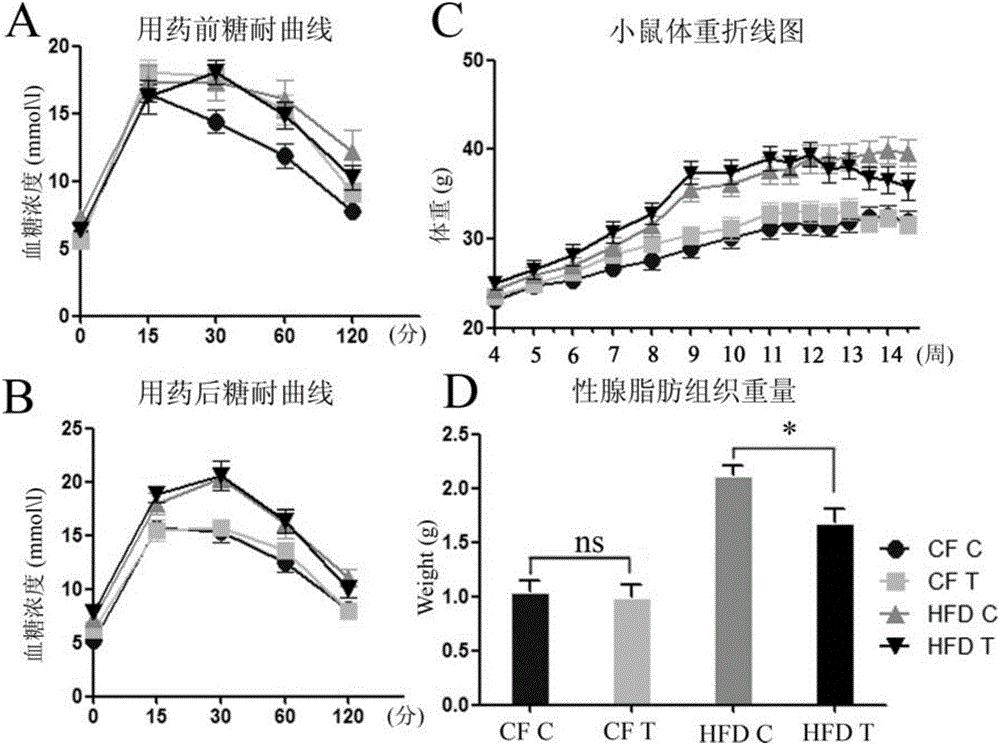
:在正常細胞中,蛋白酶體可以通過降解被泛素化標記的蛋白從而達到調控蛋白質的水平以及功能。除此之外蛋白酶體在清除細胞中的異常蛋白或者錯誤折疊蛋白同樣發揮著重要的作用。蛋白酶體抑制劑可能通過抑制一些促進細胞凋亡的因子的降解,從而達到抑制癌細胞無限增殖的目的。Bortezomib(中文譯為:硼替佐米),其化學式如式1:千禧制藥(MillenniumPharmaceuticals)定硼替佐米商品名為Velcade。中國的正式商品名為萬珂,硼替佐米是其主成分,是一種癌癥治療藥物。硼替佐米是全球第一個用于治療人類疾病的蛋白酶體抑制劑(proteasomeinhibitor),也是唯一一個被FDA批準的用于人類臨床疾病的蛋白酶體抑制劑藥物,可延緩、停止及治療多發性骨髓瘤(multiplemyeloma)和被套細胞淋巴瘤(Mantlecelllymphoma),屬于標靶治療的新型抗癌藥。硼替佐米于1995年由美國一家制藥公司Myogenics公司(后來改名為ProScript)的科學家發現,藥物代號為PS-341。該藥物僅僅做了小規模的針對多發性骨髓瘤病人的一期臨床試驗。1999年10月Leukosite公司又被MillenniumPharmaceuticals收購,千禧制藥公司并與美國強生公司合作繼續發展PS-341。臨床研究指出,一群對治療沒有效應或已經復發的骨髓瘤病患,接受萬珂的治療后,有35%對萬珂有效應,而且其中有10%的患者屬于完全或接近完全的緩解。如此的效應率具有高度意義,因為后期疾病的患者或對其他治療無反應的多發性骨髓瘤患者,有完全緩解的很罕見。兩個二期臨床試驗的證據顯示,PS-341確實具備持續性的療效反應,因此美國食品藥品監督管理局(FDA)在2003年5月快速審查通過準 許其用于治療已接受過至少兩種處方而表現出疾病惡化的多發性骨髓瘤,之后于2008年同意應用于所有多發性骨髓瘤病人。脂滴是細胞內中性脂(neutrallipids)的主要貯存場所,廣泛存在于細菌、酵母、植物、昆蟲以及動物細胞中。研究表明,多種代謝性疾病,如肥胖、脂肪肝、心血管疾病及糖尿病、中性脂貯存性疾病和NiemannPickC疾病,往往都伴隨著脂滴的大小和單位面積數目(密度)的異常。技術實現要素:本發明所要解決的技術問題是提供蛋白酶體抑制劑的降低生物體內脂的含量和脂儲積能力的新功能。為解決上述技術問題,本發明首先提供了下述1-5中任一應用:1、蛋白酶體抑制劑在制備降低動物脂含量或脂儲積能力產品中的應用;2、蛋白酶體抑制劑在制備降低動物組織脂含量或脂儲積能力產品中的應用;3、蛋白酶體抑制劑在制備降低動物細胞脂含量或脂儲積能力產品中的應用;4、蛋白酶體抑制劑在制備治療動物脂肪肝產品中的應用;5、蛋白酶體抑制劑在制備降低動物體重產品中的應用。本發明中,所述動物可為哺乳動物,如人或小鼠。所述哺乳動物具體可為小鼠(C57BL/6)。所述動物細胞具體可為人類宮頸癌HeLa細胞。所述動物組織可為脂肪組織或非脂肪組織。所述脂肪組織具體可為性腺脂肪組織。所述非脂肪組織具體可為肝臟組織。本發明中,所述蛋白酶體抑制劑可為硼替佐米(Bortezomib)、以所述硼替佐米為活性成分的藥物、MG132或以所述MG132為活性成分的藥物。所述硼替佐米具體可為SelleckChemicals公司產品,產品目錄號為S1013。所述MG132具體可為SelleckChemicals公司產品,產品目錄號位S2619。本發明中,所述動物脂含量是指動物中性脂含量,可體現在動物細胞和/或組織中脂滴的大小和單位面積數目(密度)上。所述動物組織脂含量是指動物組織中性脂含量,可體現在動物組織中脂滴的大小和單位面積數目(密度)上。所述動物細胞脂含量是指動物細胞中性脂含量,可體現在動物細胞中脂滴的大小和單位面積數目(密度)上。本發明中,所述脂肪肝為非酒精性脂肪性肝病(NAFLD),是指除酒精和其他明確的損肝因素外所致的肝細胞內脂肪過度沉積為主要特征的臨床病理綜合征。實驗證明,蛋白酶體抑制劑可以降低動物脂含量,施用蛋白酶體抑制劑后動物的脂肪肝表型得到了明顯的改善:HFDT組(高脂飲食小鼠蛋白酶體抑制劑處理組)小鼠肝臟組織中的脂滴直徑高于HFDC組(高脂飲食小鼠空白處理組)小鼠肝臟組織 中的脂滴直徑(p<0.001),CFT組(正常體重小鼠蛋白酶體抑制劑處理組)小鼠肝臟組織中的脂滴直徑高于CFC組(正常體重小鼠空白處理組)小鼠肝臟組織中的脂滴直徑(p<0.001);HFDC組(高脂飲食小鼠空白處理組)小鼠每3mm2肝臟組織中的脂滴個數高于HFDT組(高脂飲食小鼠蛋白酶體抑制劑處理組)小鼠每3mm2肝臟組織中的脂滴個數(p<0.001),CFC組(正常體重小鼠空白處理組)小鼠每3mm2肝臟組織中的脂滴個數高于CFT組(正常體重小鼠蛋白酶體抑制劑處理組)小鼠每3mm2肝臟組織中的脂滴個數(p<0.001)。HFDT組(高脂飲食小鼠蛋白酶體抑制劑處理組)小鼠的性腺脂肪組織重量顯著高于HFDC組(高脂飲食小鼠空白處理組)小鼠的性腺脂肪組織重量,HFDT組(高脂飲食小鼠蛋白酶體抑制劑處理組)小鼠的性腺脂肪組織重量為HFDC組(高脂飲食小鼠空白處理組)小鼠的0.79倍。實驗證明,蛋白酶體抑制劑可以降低動物細胞的脂儲積能力:MG132可以減少人類宮頸癌HeLa細胞中的脂滴數量,并且人類宮頸癌HeLa細胞中的脂滴數量隨MG132濃度的升高而降低。實驗證明,蛋白酶體抑制劑可以降低肥胖動物的體重:硼替佐米對正常體重小鼠無影響,HFDT組(高脂飲食小鼠蛋白酶體抑制劑處理組)小鼠體重為HFDC組(高脂飲食小鼠空白處理組)小鼠的0.90倍。實驗證明,蛋白酶體抑制劑可以用來制備降低動物、動物細胞與動物組織的脂含量和脂儲積能力以及動物體重的產品。附圖說明圖1為硼替佐米處理對小鼠體重和性腺脂肪組織的影響。其中,A為硼替佐米處理前各組小鼠的糖耐受情況;B為硼替佐米處理后各組小鼠的糖耐受情況;C為不同時期各組小鼠體重的變化情況;D為在處理28天各組小鼠性腺脂肪組織的重量,ns表示T-test中無顯著差異,*表示P<0.05。圖2為各組小鼠肝臟組織和性腺脂肪組織中的脂滴。其中,A為各組小鼠肝臟組織和性腺脂肪組織中的脂滴照片;B為各組小鼠肝臟組織中的脂滴直徑;C為各組小鼠肝臟組織中的脂滴密度。ns表示T-test中無顯著差異,***表示P<0.001。圖3為不同培養基中人類宮頸癌HeLa細胞中的脂滴。其中,20uM、60uM和100uM分別表示20μM、60μM和100μM。具體實施方式下面結合具體實施方式對本發明進行進一步的詳細描述,給出的實施例僅為了闡明本發明,而不是為了限制本發明的范圍。下述實施例中的實驗方法,如無特殊說明,均為常規方法。下述實施例中所用的材料、試劑等,如無特殊說明,均可從商業途徑得到。下述實施例中的小鼠(C57BL/6)為北京維通利華實驗動物技術有限公司產品,專業名稱為C57BL/6NCrlBR,品系代碼為213。下述實施例中的人類宮頸癌HeLa細胞系為ACTT(AmericanTypeCultureCollection)產品,商品名為HeLa(CCL-2TM)。下述實施例中的脂肪含量為10%(脂肪提供熱量百分比)的鼠糧為ResearchDiets,Inc產品,產品目錄號為D12450H。下述實施例中的脂肪含量為45%(脂肪提供熱量百分比)的鼠糧為ResearchDiets,Inc產品,產品目錄號為D12451。下述實施例中的硼替佐米為SelleckChemicals產品,產品目錄號為S1013。下述實施例中的MG132為SelleckChemicals產品,產品目錄號位S2619。下述實施例中的OA培養基的制備方法為:向無水乙醇中加入OA得到OA濃度為100mM的OA母液,向DMEM完全培養基中加入OA母液得到OA濃度為100μM的OA培養基。下述實施例中的OA-20μMMG132培養基的制備方法為:向DMSO中加入MG132得到MG132濃度為20mM的MG132母液,向上述OA培養基中加入MG132母液得到MG132濃度為20μM的OA-20μMMG132培養基。下述實施例中的OA-60μMMG132培養基的制備方法為:向DMSO中加入MG132得到MG132濃度為20mM的MG132母液,向上述OA培養基中加入MG132母液得到MG132濃度為60μM的OA-60μMMG132培養基。下述實施例中的OA-100μMMG132培養基的制備方法為:向DMSO中加入MG132得到MG132濃度為20mM的MG132母液,向上述OA培養基中加入MG132母液得到MG132濃度為100μM的OA-100μMMG132培養基。下述實施例中的OA培養基、OA-20μMMG132培養基、OA-60μMMG132培養基和OA-100μMMG132培養基中的油酸(Oleicacid,O.A.)可使在這些培養基中培養的細胞產生大量大小均一的脂滴。下述實施例中的動物體內脂含量是指動物體內中性脂含量;細胞中的脂含量是指細胞中的中性脂含量。實施例1、蛋白酶體抑制劑可以降低動物體內脂含量本實施例中用到的蛋白酶體抑制劑為硼替佐米。一、肥胖小鼠模型的建立通過不同脂肪含量的配方鼠糧對小鼠(C57BL/6)進行不同肥胖程度的誘導,具體方法如下:選取32只4周齡小鼠(C57BL/6),隨機分為兩組,每組16只:一組飼喂脂肪含量為10%(脂肪提供熱量百分比)的鼠糧7周,得到16只11周齡的正常體重小鼠;另一組飼喂脂肪含量為45%(脂肪提供熱量百分比)的鼠糧7周,得到16只11周齡的高脂飲食(highfatdiet,HFD)小鼠,這16只高脂飲食小鼠具有與人類肥胖人群相似的II型糖尿病癥狀,如胰島素抵抗。從小鼠4周齡至11周齡,每周測量體重一次,上述小鼠的體重如圖1中C所示。二、硼替佐米可以降低動物體內脂含量將硼替佐米溶于DMSO中,得到硼替佐米溶液。稱量正常體重小鼠體重后,按照1μg硼替佐米/g體重的標準分別對8只正常體重小鼠灌胃上述硼替佐米溶液,將灌胃當天記為處理第0天(小鼠11周齡),分別在處理第3天、處理第7天(小鼠12周齡)、處理第10天、處理第14天(小鼠13周齡)、處理第17天、處理第21天(小鼠14周齡)和處理第24天各灌胃一次,每次灌胃硼替佐米溶液的體積均和第一次灌胃硼替佐米溶液的體積相同,分別在處理第3天、處理第7天、處理第10天、處理第14天、處理第17天、處理第21天、處理第24天和處理第28天(小鼠15周齡)稱量小鼠體重(表1和圖1中C),硼替佐米處理結束后得到8只15周齡正常體重硼替佐米處理小鼠(CFT組小鼠),硼替佐米處理過程中,這8只小鼠均用脂肪含量為10%(脂肪提供熱量百分比)的鼠糧飼喂。按照上述方法,將硼替佐米溶液替換為等體積的DMSO,其他均不變,得到8只15周齡正常體重空白處理小鼠(CFC組小鼠),DMSO處理過程中小鼠體重如表1和圖1中C所示。稱量高脂飲食小鼠體重后,按照1μg硼替佐米/g體重的標準分別對8只高脂飲食小鼠灌胃上述硼替佐米溶液,將灌胃當天記為處理第0天(小鼠11周齡),分別在處理第3天、處理第7天(小鼠12周齡)、處理第10天、處理第14天(小鼠13周齡)、處理第17天、處理第21天(小鼠14周齡)和處理第24天各灌胃一次,每次灌胃硼替佐米溶液的體積均和第一次灌胃硼替佐米溶液的體積相同,分別在處理第3天、處理第7天、處理第10天、處理第14天、處理第17天、處理第21天、處理第24天和處理第28天(小鼠15周齡)稱量小鼠體重(表1和圖1中C),硼替佐米處理結束后得到8只15周齡高脂飲食硼替佐米處理小鼠(HFDT組小鼠),硼替佐米處理過程中,這8只小鼠均用脂肪含量為45%(脂肪提供熱量百分比)的鼠糧飼喂。按照上述方法,將硼替佐米溶液替換為等體積的DMSO,其他均不變,得到8只15周齡高脂飲食空白處理小鼠(HFDC組小鼠),DMSO處理過程中小鼠體重如表1 和圖1中C所示。在處理第0天各組小鼠灌胃前和處理第28天各組小鼠體重稱量后檢測小鼠的糖耐受情況,具體方法如下:對各組已空腹12小時的小鼠,分別依照體重按10μl/g體重的劑量腹腔注射濃度為0.2g/ml的葡萄糖溶液,在注射葡萄糖前和注射葡萄糖后15分鐘、30分鐘、60分鐘和120分鐘分別測定每只小鼠的血糖含量(圖1中A和B)。在處理第28天,分別取出以上各組小鼠的性腺脂肪組織(gWAT,性腺脂肪組織是和小鼠性腺緊密相連的一堆脂肪塊,可以直接從小鼠體內取出)并稱取重量(圖1中D),然后用蘇木素/伊紅(HE)染色后觀察性腺脂肪組織中的脂滴(圖2中A)。在處理第28天,分別取出以上各組小鼠的肝臟組織,用蘇木素/伊紅(HE)染色后觀察肝臟組織中的脂滴并統計脂滴的直徑和分布密度(圖2和表2)。表1、每次灌胃前各組小鼠的體重(g)處理時間HFDT組HFDC組CFT組CFC組處理第0天37.43±3.8036.20±3.8231.13±3.4630.11±3.21處理第3天38.98±3.8737.68±4.2732.87±3.2131.17±3.13處理第7天38.60±3.8137.76±4.4532.96±3.0331.82±3.44處理第10天39.43±3.7038.92±4.4532.97±3.3031.70±3.42處理第14天37.77±4.0438.88±4.4832.77±2.9431.31±2.99處理第17天38.17±3.8939.11±4.1633.28±3.0531.98±3.47處理第21天36.83±3.6839.41±4.3131.62±1.8732.41±3.46處理第24天36.63±4.1439.92±4.3632.31±2.2532.52±3.50處理第28天35.82±4.1439.60±4.3031.58±2.4731.98±3.22結果顯示,糖耐受實驗表明硼替佐米小鼠的糖耐受沒有影響。在處理第0天,用于硼替佐米處理的8只正常體重小鼠和用于DMSO處理的8只正常體重小鼠體重基本無差異,用于硼替佐米處理的8只高脂飲食小鼠和用于DMSO處理的8只高脂飲食小鼠體重基本無差異,用于硼替佐米處理的8只高脂飲食小鼠的體重為用于硼替佐米處理的8只正常體重小鼠的1.2倍;在處理第28天,正常體重空白處理小鼠(CFC組小鼠)與正常體重硼替佐米處理小鼠(CFT組小鼠)體重基本無差異,而高脂飲食硼替佐米處理小鼠(HFDT組小鼠)體重為高脂飲食空白處理小鼠(HFDC組小鼠)的0.9倍,表明,硼替佐米對正常體重小鼠無影響,但可以降低高脂飲 食小鼠(即肥胖小鼠)的體重。在處理第28天,正常體重空白處理小鼠(CFC組小鼠)、正常體重硼替佐米處理小鼠(CFT組小鼠)、高脂飲食空白處理小鼠(HFDC組小鼠)和高脂飲食硼替佐米處理小鼠(HFDT組小鼠)的性腺脂肪組織重量分別為1.04±0.27g、0.99±0.26g、2.12±0.24g和1.68±0.36g。正常體重空白處理小鼠(CFC組小鼠)與正常體重硼替佐米處理小鼠(CFT組小鼠)的性腺脂肪組織重量基本無差異,而高脂飲食硼替佐米處理小鼠(HFDT組小鼠)的性腺脂肪組織重量顯著高于高脂飲食空白處理小鼠(HFDC組小鼠)的性腺脂肪組織重量,高脂飲食硼替佐米處理小鼠(HFDT組小鼠)的性腺脂肪組織重量為高脂飲食空白處理小鼠(HFDC組小鼠)的0.79倍。表明,硼替佐米對正常體重小鼠無影響,但可以降低高脂飲食小鼠(即肥胖小鼠)的性腺脂肪組織重量。表2、各組小鼠的肝臟組織中的脂滴直徑和分布密度組別脂滴直徑(μm)脂滴密度(每3mm2脂滴個數)CFC組22.57±8.507264.3±95.37CFT組6.843±2.46312.38±8.749HFDC組21.72±6.245459.0±72.23HFDT組7.076±2.825233.3±84.53結果顯示,CFC組小鼠與HFDC組小鼠肝臟組織中的脂滴直徑基本無差異,HFDT組小鼠與CFT組小鼠肝臟組織中的脂滴直徑基本無差異,HFDT組小鼠肝臟組織中的脂滴直徑高于HFDC組小鼠肝臟組織中的脂滴直徑(p<0.001),CFT組小鼠肝臟組織中的脂滴直徑高于CFC組小鼠肝臟組織中的脂滴直徑(p<0.001)。HFDC組小鼠每3mm2肝臟組織中的脂滴個數高于CFC組小鼠每3mm2肝臟組織中的脂滴個數(p<0.001),HFDT組小鼠每3mm2肝臟組織中的脂滴個數高于CFT組小鼠每3mm2肝臟組織中的脂滴個數(p<0.001),HFDC組小鼠每3mm2肝臟組織中的脂滴個數高于HFDT組小鼠每3mm2肝臟組織中的脂滴個數(p<0.001),CFC組小鼠每3mm2肝臟組織中的脂滴個數高于CFT組小鼠每3mm2肝臟組織中的脂滴個數(p<0.001)。表明,硼替佐米可以降低小鼠肝臟組織中的脂滴直徑與脂滴密度,小鼠的脂肪肝表型得到了明顯的改善(圖2中A)。實施例2、蛋白酶體抑制劑可以降低細胞中的脂含量本實施例中用到的蛋白酶體抑制劑為MG132。分別向OA培養基、OA-20μMMG132培養基、OA-60μMMG132培養基和OA-100μMMG132培養基中加入人類宮頸癌HeLa細胞系,每種培養基中人類宮頸癌HeLa細胞的密度相同,然后分別在37℃下培養24小時,經過4%PFA固定后,用BODIPY標記各培養基的人類宮頸癌HeLa細胞的脂滴后,觀察各培養基中細胞中的脂滴,結果如圖3所示。結果顯示,MG132可以減少人類宮頸癌HeLa細胞中的脂滴數量,并且人類宮頸癌HeLa細胞中的脂滴數量隨MG132濃度的升高而降低,表明MG132可以降低細胞的脂儲積能力,而且具備劑量效應。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1
- 一種制備自噬小體型瘤苗的培養基添加劑及其制備方法與制造工藝
- N-萘烷基取代的含氮雜環衍生物、制備方法及其抗腫瘤用途與制造工藝
- 作為BET蛋白抑制劑的1H?吡咯并[2,3?c]吡啶?7(6H)?酮和吡唑并[3,4?c]吡啶?7(6H)?酮的制造方法與工藝
- 一種人腫瘤抑制蛋白變體及其應用的制造方法與工藝
- 一種人腫瘤抑制蛋白變體及其應用的制造方法與工藝
- G蛋白信號調節因子6及其抑制劑在治療脂肪肝和Ⅱ型糖尿病中的功能和應用的制造方法與工藝
- 蛋白酶體抑制劑在制備降低動物脂含量或脂儲積能力產品中的應用的制造方法與工藝
- GINS2基因或蛋白的抑制劑在制備抗腫瘤藥物中的應用的制造方法與工藝
- ZNF383蛋白在制備抑制p53蛋白活性的產品中的應用的制造方法與工藝
- 蛋白酶體抑制劑MLN9708的合成方法與制造工藝