配合花粉形糖類載體的干粉吸入劑及其制備和使用方法與流程
本發明涉及醫藥制劑領域,具體涉及一種配合花粉形糖類載體的干粉吸入劑及其制備和使用方法。
背景技術:
近年來,由于大氣污染和吸煙造成的影響,慢性阻塞性肺疾(copd)、肺癌及哮喘患者越來越多,干粉吸入劑(dpi)是治療這些疾病的最佳方法。但由于干粉吸入劑技術門檻高,仿制難度較大,國內干粉吸入劑市場被國外品牌極大的占據,國內急需進一步的技術完善和革新。
現有技術中記載了干粉吸入劑、其制備方法和用途(申請號cn200810151281.5),通過發泡技術制備了含低密度的可吸入藥物粉末,從原料藥的制備上提高了抗腫瘤藥物的肺部傳遞效果,但干粉吸入劑最重要的技術參數還包含載體的設計和配比,該方法實用性不足。
現有技術中記載了氫溴酸東莨菪堿鼻用干粉吸入劑及制備方法(申請號cn200510033328.4),該方法通過吸附技術制備了含藥物成分的輔料載體,穩定性和實用性較高,但受載體技術的限制,該方法僅用于鼻粘膜給藥,無法用于肺部給藥(狹義上的干粉吸入劑領域)。
為了有效利用載體遞送藥物,現有技術記載了一種干粉吸入劑藥物組合物及其制備方法(申請號cn201610147903.1),在制備干粉吸入劑藥物后,將藥物與符合尺寸的一水乳糖載體混合,利用乳糖微粒來運載干粉吸入劑藥物,提高干粉吸入劑有效運達肺部的比率,但由于一水乳糖顆粒表面積有限,無論如何研磨、造粒,都存在低的藥物運載量。
因此,通過高效實用的制備工藝,尋求新型的、藥物運載量大的、呼吸道遷移能力好的、穩定性強的糖類載體微粒,且采用簡單便捷的使用方法,來提高干粉吸入劑在肺部給藥上的遞釋效率,是當前需要解決的問題。
技術實現要素:
針對現有技術中的缺陷,本發明目的在于提供一種配合花粉形糖類載體的干粉吸入劑及其制備和使用方法,通過生產花粉形糖類載體,配合藥物、微粉實現吸入劑的三元給藥系統,實現高的藥物運載量、呼吸道遷移能力和穩定性,以取得更佳的吸入藥療效。
為實現上述目的,本發明提供的技術方案為:
第一方面,本發明提供了一種配合花粉形糖類載體的干粉吸入劑,其特征在于:所述干粉吸入劑含三元混合組分,包括0.01-2份的有效藥物成分(氣體動力學直徑中值優選為0.5-5μm)、0-20份的糖類粗粉載體(氣體動力學直徑中值優選為10-100μm)和0-20份的糖類細粉載體(氣體動力學直徑中值優選為1-10μm),其中糖類粗粉載體和/或糖類細粉載體采用制備的花粉形糖類載體微粒(顆粒表面粗糙、內部多孔,bet孔表面積為10-60m2/g),且糖類粗粉載體的密度優選為糖類細粉載體密度的1-3倍,糖類粗粉載體的粒徑優選為糖類細粉載體粒徑的5-10倍;所述干粉吸入劑的細粉分布比例(fpf)為10-50%。
應當說明的是,三元混合組分制備干粉吸入劑是提高干粉吸入劑遞釋效率的方法,即將有效藥物成分、粗粉載體和細粉載體混合,通過細粉載體占據粗粉載體上的高能位點(吸附力強的位置),降低有效藥物成分和粗粉載體的結合強度,使有效藥物成分更容易在呼吸道中被釋放。
同時,有效藥物成分的氣體動力學直徑中值優選為0.5-5μm,低于該值則容易擴散沉積,高于該值則容易在肺部撞擊或沉降沉積,均影響藥效;糖類粗粉載體的氣體動力學直徑中值優選為10-100μm,低于該值則達不到粗載體的運載效果,高于該值則顆粒太大,容易在喉部撞擊或沉降沉積;作為調控粗粉載體能量點位時,糖類細粉載體的氣體動力學直徑中值優選為1-10μm,更優選的氣體動力學直徑中值為5-10μm,糖類粗粉載體的密度優選為糖類細粉載體密度的1-3倍,糖類粗粉載體的粒徑優選為糖類細粉載體粒徑的5-10倍,其他范圍對三元混合的效果均勻影響,具體表現在達不到占據粗粉載體上的高能位點的作用;此外,糖類細粉載體還可作為在溶液中吸附藥物分子的載體,即原料藥的一部分,根據肺部呼吸道尺寸,其氣體動力學直徑中值優選為1-5μm,同理,高或低于該值均會通過撞擊、沉積或擴散造成顆粒沉積,影響療效。
糖類粗粉載體和/或糖類細粉載體采用制備的花粉形糖類載體微粒,所述花粉形糖類載體微粒通過溶液重結晶過程制備,尺寸可控制在1-100μm,在此范圍對應的bet孔表面積為10-60m2/g,表面粗糙,外觀類似花粉形(或描述為花形、花球形、糙面球形、毛球形、齒面顆粒等),切開顆粒觀察到內部具有多孔結構。
此外,由于僅5μm以下的細粉才能抵達肺泡,干粉吸入劑的細粉分布比例(fpf)說明了藥物藥效,高達50%的fpf能保證好的療效和運載能力,低于10%則療效不佳。
也就是說,本發明提供的配合花粉形糖類載體的干粉吸入劑,通過設計和優化三元混合組分系統,提高了藥物的呼吸道傳輸效果,藥效更佳。
第二方面,本發明提供了所述配合花粉形糖類載體的干粉吸入劑的制備步驟:通過溶液重結晶過程制備得到花粉形糖類載體微粒;用糖類細粉載體物理混合或溶液吸附有效藥物成分;用糖類粗粉載體與額外糖類細粉載體均勻混合;將上述有效藥物成分、糖類粗、細粉載體三元混合。
在本發明的進一步實施方式中,溶液重結晶過程采用的溶劑為乙醇(酒精),結晶析出的粉末微粒(1-100μm)在過濾后通過吹氣風干,然后用氣流分離器分選出不同形貌和粒徑規格的粉末微粒,得到花粉形糖類載體微粒。應當說明的是,溶液重結晶即將非定形態(通過超飽和瞬間析出或噴霧干燥制備)的糖類物質在有機溶劑中進行重結晶,可選用多種不溶解糖類物質的有機溶劑,考慮到低毒性和價格,優選乙醇(酒精),穩定后(15分鐘以上)分離獲得粉末微粒,根據《水熱結晶學》(施爾畏等著,科學出版社2004年出版)記載,粉末微粒的大小受結晶過程的濃度、溫度、攪拌速度等因素控制,具體條件參數在實施例中說明,且考慮到吸入劑載體設計,如前所述,糖類粗粉載體的尺寸為10-100μm、糖類細粉載體的尺寸為1-10μm。為防止熱法干燥在高溫下造成形貌變化,干燥粉末微粒優選吹氣風干,同時,不同形貌和粒徑規格的顆粒其隨氣體運動的慣性不同,氣流分離器用來分離得到所需的花粉形糖類載體微粒。
在本發明的進一步實施方式中,首先,使用糖類細粉載體0-20份,有效藥物成分0.01-2份,混合或吸附時間為5-60分鐘;隨后,使用糖類粗粉載體0-20份,糖類細粉載體0-20份,混合或吸附時間為5-60分鐘;將上述有效藥物成分、糖類粗、細粉載體三元混合的時間為5-60分鐘。應當說明的是,糖類細粉載體可僅作為三元混合系統的調節物質,也可作為藥物分子的吸附劑,每步的混合時間均在5-60分鐘,更短時間混合會造成混合不充分、聚集效果不好,混合時間過長則會造成藥物和載體的解聚,也沒有必要。
在本發明的進一步實施方式中,所述的有效藥物成分為包括m-受體拮抗劑(優選為噻托溴銨、溴化異丙托品)、β2-受體激動劑(優選為沙美特羅、沙丁胺醇)、皮質激素劑(優選為布地奈德、氟替卡松)、多肽及蛋白藥物(優選胰高血糖素、胰島素、降鈣素、多粘菌素、白介素、蛋白酶抑制劑、細胞刺激因子、脫氧核糖核酸酶、白蛋白)、氨基酸、福米特羅、羥丙茶堿、氟尼縮松、抗腫瘤藥物、二羥丙茶堿、倍氯米松、特布他林、氨茶堿、茶堿、酚丙喘寧、丙卡特羅、曲安縮松及其衍生物在內的一種或多種混合藥物。應當說明的是,以上藥物均為干粉吸入劑中作為有效藥物成分的物質,本發明所述的有效藥物成分包括但不限于以上舉例,以上藥物成分通過物理方式與載體混合,不涉及特殊要求的工藝,其中,m-受體拮抗劑(優選為噻托溴銨、溴化異丙托品)、β2-受體激動劑(優選為沙美特羅、沙丁胺醇)、皮質激素劑(優選為布地奈德、氟替卡松)、氨基酸、福米特羅、羥丙茶堿、氟尼縮松、抗腫瘤藥物、二羥丙茶堿、倍氯米松、特布他林、氨茶堿、茶堿、酚丙喘寧、丙卡特羅、曲安縮松及其衍生物可通過在有機溶液中物理吸附法被細粉載體吸附,或物理研磨后直接混合,而多肽及蛋白藥物(優選胰高血糖素、胰島素、降鈣素、多粘菌素、白介素、蛋白酶抑制劑、細胞刺激因子、脫氧核糖核酸酶、白蛋白)由于不能用有機溶劑溶劑,只能采用物理研磨后直接混合的方式。
在本發明的進一步實施方式中,所述糖類細粉載體、所述糖類粗粉載體和所述花粉形糖類載體的材料為包括但不限于乳糖、棉子糖、海藻糖、葡萄糖、蔗糖、赤蘚糖醇、甘露醇、木糖醇、山梨醇、右旋糖苷、環糊精在內的一種或多種可食用材料。應當說明的是,以上糖類物質為干粉吸入劑中作為載體或藥物吸附載體的物質,通過本發明所述的溶液重結晶過程制備得到對應的花粉形糖類載體微粒,而乳糖是目前fda唯一授權安全載體,優選采用乳糖作為載體,其他材料由于也是糖類物質,也是可以作為藥用載體的,但還沒有相關批文出臺。
采用本發明提供的配合花粉形糖類載體的干粉吸入劑的制備方法,通過溶液重結晶過程制備得到花粉形糖類載體微粒,利用三元混合系統穩定藥物傳輸能力,制備得到的干粉吸入劑其氣體流動性、穩定性、藥效、實用性更佳。
第三方面,本發明提供的一種配合花粉形糖類載體的干粉吸入劑的使用方法,其特征在于:將制備的配合花粉形糖類載體的干粉吸入劑裝入吸入器或吸入器用膠囊中,在進一步實施方式中,使用吸入器吸入給藥時,每吸或每膠囊的單位給藥計量優選為10-50mg,可多次給藥。應當說明的是,根據干粉吸入器的設計,有瓶裝型吸入器和膠囊型吸入器等品種,瓶裝型吸入器的給藥量受按壓噴霧量控制,膠囊型吸入器的給藥量受單位膠囊中裝載的粉末量控制,優選的單位給藥計量為10-50mg,單次給藥量低于10mg則給藥太少,療效太低,需要多次給藥;單次給藥量高于50mg則每吸粉末量太多,容易造成浪費和呼吸不適。
本發明的附加方面和優點將在下面的描述中部分給出,部分將從下面的描述中變得明顯,或通過本發明的實踐了解到。
附圖說明
圖1為本發明實施例中的配合花粉形糖類載體的干粉吸入劑的制備方法的流程圖。
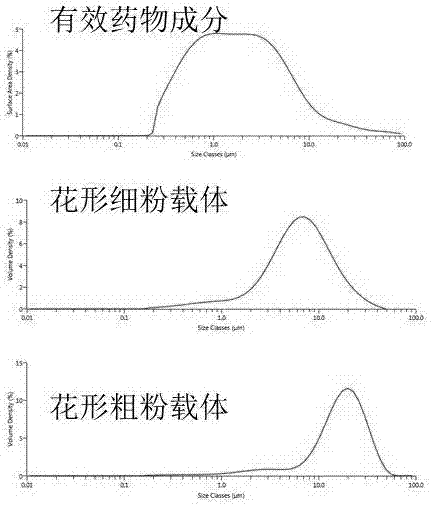
圖2為本發明實施例二中制備的干粉吸入劑的三元混合組分(有效藥物成分、糖類細、粗粉載體)的激光粒徑掃描圖。
圖3為本發明實施例三中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖。
圖4為本發明實施例四中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖。
圖5為本發明實施例五中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖。
圖6為本發明實施例六中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖。
圖7為本發明實施例七中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖。
圖8為本發明實施例八中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖。
圖9為本發明實施例九中制備的花粉形糖類載體在切開后的sem掃描電鏡圖。
圖10為本發明實施例十中制備的花粉形糖類載體在吸附藥物分子后的微、介孔結構變化圖。
圖11為本發明實施例十一中配合花粉形糖類載體的干粉吸入劑,對比配合常規一水乳糖載體的干粉吸入劑,在呼吸道模擬模型中的顆粒傳輸測試圖。
圖12為本發明實施例十二中配合常規一水乳糖載體的干粉吸入劑和配合粗、細粉花粉形糖類載體的干粉吸入劑在肺部模擬模型中的藥物沉積測試比對圖,及配合常規一水乳糖載體或花粉形載體的干粉吸入劑的sem掃描電鏡圖。
具體實施方式
下面將結合本發明實施例中的附圖,對本發明實施例中的技術方案進行清楚、完整地描述,顯然,所描述的實施例僅是本發明一部分實施例,而不是全部的實施例。基于本發明中的實施例,本領域普通技術人員在沒有做出創造性勞動前提下所獲得的所有其他實施例,都屬于本發明保護的范圍。
實施例一
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑,含三元混合組分,包括0.01-2份的有效藥物成分(氣體動力學直徑中值優選為0.5-5μm)、0-20份的糖類粗粉載體(氣體動力學直徑中值優選為10-100μm)和0-20份的糖類細粉載體(氣體動力學直徑中值優選為1-10μm),其中糖類粗粉載體和/或糖類細粉載體采用制備的花粉形糖類載體微粒(顆粒表面粗糙、內部多孔,bet孔表面積為10-60m2/g),且糖類粗粉載體的密度優選為糖類細粉載體密度的1-3倍,糖類粗粉載體的粒徑優選為糖類細粉載體粒徑的5-10倍;所述干粉吸入劑的細粉分布比例(fpf)為10-50%。
針對本發明的配合花粉形糖類載體的干粉吸入劑,本發明設計了該干粉吸入劑的制備方法。
圖1為本發明實施例中的配合花粉形糖類載體的干粉吸入劑的制備方法的流程圖,如圖1所示,本發明提供的配合花粉形糖類載體的干粉吸入劑的制備方法為:
s1:通過溶液重結晶過程制備得到花粉形糖類載體微粒;
s2:用糖類細粉載體物理混合或溶液吸附有效藥物成分;
s3:用糖類粗粉載體與額外糖類細粉載體均勻混合;
s4:將上述有效藥物成分、糖類粗、細粉載體三元混合。
下面結合具體實施例對本發明提供的配合花粉形糖類載體的干粉吸入劑載體的制備方法作進一步說明。
實施例二
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的制備方法,包括如下步驟:
s1:將50克噴霧干燥制備的不定形乳糖微粒與500ml乙醇混合,攪拌30分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為7微米的花形糖類細粉載體和中值粒徑為20微米的花形糖類粗粉載體;
s2:將市售的布地奈德微粉進行精研磨,得到中值直徑為1.5微米的有效藥物成分,按比例將2份所述糖類細粉載體與0.05份所述有效藥物成分物理混合5分鐘;
s3:額外的,按比例將5份所述糖類細粉載體與13份所述糖類細粉載體物理混合5分鐘;
s4:將上述有效藥物成分、糖類粗、細粉載體物理混合,混合時間為5分鐘。
為驗證制備方法的精確性,產品用激光粒度測量儀進行了測驗,圖2為本發明實施例二中制備的干粉吸入劑的三元混合組分(有效藥物成分、糖類細、粗粉載體)的激光粒徑掃描圖,如圖2所示,上述有效藥物成分、糖類粗、細粉載體得顆粒尺寸基本呈正態分布,有效藥物成分的中值直徑為1.5微米,花形糖類細粉載體的中值直徑為7微米,花形糖類粗粉載體的中值直徑為20微米,滿足本發明提出的三元混合組分干粉吸入劑的要求。應當說明的是,三元混合組分的尺寸對藥效影響較大,有效藥物成分、粗粉載體和細粉載體混合后,細粉載體通過占據粗粉載體上的高能位點(吸附力強的位置),降低有效藥物成分和粗粉載體的結合強度,使有效藥物成分更容易在呼吸道中被釋放。
實施例三
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的制備方法,包括如下步驟:
s1:將10克超飽和溶液析出制備的不定形乳糖微粒與100ml乙醇混合,攪拌15分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為8微米的花形糖類細粉載體和中值粒徑為30微米的花形糖類粗粉載體;
s2:將市售的噻托溴銨微粉進行精研磨,得到中值直徑為2微米的有效藥物成分;
s3:按比例將5份所述糖類細粉載體與15份所述糖類細粉載體物理混合60分鐘;
s4:將上述有效藥物成分、糖類粗、細粉載體物理混合,混合時間為60分鐘。
實施例四
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的制備方法,包括如下步驟:
s1:將100克超飽和溶液析出制備的不定形乳糖微粒與1l酒精混合,攪拌30分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為2微米的花形糖類細粉載體和中值粒徑為5微米的花形糖類粗粉載體;
s2:將噻托溴銨溶于乙醇,將0.1m的噻托溴銨乙醇溶液與所述花形糖類細粉載體混合吸附30分鐘,過濾去除上清液,風干沉淀顆粒;
s3/s4:按比例將19份所述糖類細粉載體與1份所述糖類細粉載體物理混合5分鐘。
實施例五
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的制備方法,包括如下步驟:
s1:將10克噴霧干燥制備的不定形赤蘚糖醇微粒與100ml甲醇混合,攪拌30分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為5微米的花形糖類細粉載體和中值粒徑為100微米的花形糖類粗粉載體;
s2:將市售的羥丙茶堿進行精研磨,得到中值直徑為0.5微米的有效藥物成分,按比例將0.01份所述有效藥物成分與20份所述糖類細粉載體物理混合15分鐘;
s3/s4:此干粉吸入劑不采用糖類粗粉載體。
實施例六
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的制備方法,包括如下步驟:
s1:將50克噴霧干燥制備的不定形棉子糖微粒與500ml丙酮混合,攪拌5分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為1微米的花形糖類細粉載體和中值粒徑為20微米的花形糖類粗粉載體;
s2:將市售的胰高血糖素微粉進行精研磨,得到中值直徑為1微米的有效藥物成分,按比例將1份所述糖類細粉載體與2份所述有效藥物成分物理混合10分鐘;
s3:額外的,按比例將2份所述糖類細粉載體與15份所述糖類細粉載體物理混合20分鐘;
s4:將上述有效藥物成分、糖類粗、細粉載體物理混合,混合時間為15分鐘。
實施例七
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的制備方法,包括如下步驟:
s1:將30克噴霧干燥制備的不定形葡萄糖微粒與500ml乙酸乙酯混合,攪拌10分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為10微米的花形糖類細粉載體和中值粒徑為15微米的花形糖類粗粉載體;
s2:將市售的沙美特羅微粉進行精研磨,得到中值直徑為0.5微米的有效藥物成分,按比例將5份所述糖類細粉載體與1份所述有效藥物成分物理混合5分鐘;
s3:額外的,按比例將4份所述糖類細粉載體與10份所述糖類細粉載體物理混合30分鐘;
s4:將上述有效藥物成分、糖類粗、細粉載體物理混合,混合時間為60分鐘。
實施例八
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的制備方法,包括如下步驟:
s1:將30克噴霧干燥制備的不定形甘露醇微粒與300ml乙醇混合,攪拌15分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為2微米的花形糖類細粉載體和中值粒徑為10微米的花形糖類粗粉載體;
s2:將市售的氟尼縮松微粉進行精研磨,得到中值直徑為1微米的有效藥物成分,按比例將2份所述糖類細粉載體與0.5份所述有效藥物成分物理混合10分鐘;
s3:額外的,按比例將7.5份所述糖類細粉載體與10份所述糖類細粉載體物理混合10分鐘;
s4:將上述有效藥物成分、糖類粗、細粉載體物理混合,混合時間為10分鐘。
為了觀測實施例中制得的干粉吸入劑的微觀形貌,將上述實施例三、實施例四、實施例五、實施例六、實施例七和實施例八制備得到的配合花粉形糖類載體的干粉吸入劑,進行了電鏡顯微掃描(sem)的形貌測定。
圖3為本發明實施例三中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖,如圖3所示,有效藥物成分的微觀尺寸約為2微米,糖類細粉載體的微觀尺寸約為8微米,糖類粗粉載體的微觀尺寸約為30微米,三元混合組分較為均勻混合;且干粉吸入劑的細粉分布比例為30%。
圖4為本發明實施例四中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖,如圖4所示,觀測不到有效藥物成分(被吸附到糖類細粉載體微粒中了),糖類細粉載體的微觀尺寸約為2微米,糖類粗粉載體的微觀尺寸約為5微米,三元混合組分較為均勻混合;且干粉吸入劑的細粉分布比例為50%。
圖5為本發明實施例五中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖,如圖5所示,有效藥物成分的微觀尺寸約為0.5微米,糖類細粉載體的微觀尺寸約為2微米,糖類粗粉載體的微觀尺寸約為100微米,三元混合組分較為均勻混合;由于實施例五沒有采用粗粉載體,故干粉吸入劑的細粉分布比例為100%。
圖6為本發明實施例六中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖,如圖6所示,有效藥物成分的微觀尺寸約為1微米,糖類細粉載體的微觀尺寸約為1微米,糖類粗粉載體的微觀尺寸約為20微米,三元混合組分較為均勻混合;且干粉吸入劑的細粉分布比例為15%。
圖7為本發明實施例七中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖,如圖7所示,由于溶劑影響,糖類載體無法形成花粉形,而是形成多孔長條形,有效藥物成分的微觀尺寸約為0.5微米,糖類載體的尺寸約為10-15微米,粗、細載體的尺寸相近;且干粉吸入劑的細粉分布比例為10%。
圖8為本發明實施例八中制備的配合花粉形糖類載體的干粉吸入劑的sem掃描電鏡圖,如圖8所示,有效藥物成分的微觀尺寸約為1微米,糖類細粉載體的微觀尺寸約為2微米,糖類粗粉載體的微觀尺寸約為10微米,三元混合組分較為均勻混合;且干粉吸入劑的細粉分布比例為40%。
通過sem測定,所述糖類微粒載體的形態多呈花粉形多孔微粒,直徑大小在1-100微米間,形貌受糖類材料和溶劑影響。應當說明的是,有效藥物成分的氣體動力學直徑中值優選為0.5-5μm,低于該值則容易擴散沉積,高于該值則容易在肺部撞擊或沉降沉積,均影響藥效;糖類粗粉載體的氣體動力學直徑中值優選為10-100μm,低于該值則達不到粗載體的運載效果,高于該值則顆粒太大,容易在喉部撞擊或沉降沉積;作為調控粗粉載體能量點位時,糖類細粉載體的氣體動力學直徑中值優選為1-10μm,更優選的氣體動力學直徑中值為5-10μm,糖類粗粉載體的密度優選為糖類細粉載體密度的1-3倍,糖類粗粉載體的粒徑優選為糖類細粉載體粒徑的5-10倍,其他范圍對三元混合的效果均勻影響,具體表現在達不到占據粗粉載體上的高能位點的作用;此外,糖類細粉載體還可作為在溶液中吸附藥物分子的載體,即原料藥的一部分,根據肺部呼吸道尺寸,其氣體動力學直徑中值優選為1-5μm,同理,高或低于該值均會通過撞擊、沉積或擴散造成顆粒沉積,影響療效。由于僅5μm以下的細粉才能抵達肺泡,干粉吸入劑的細粉分布比例(fpf)說明了藥物藥效,高達50%的fpf能保證好的療效和運載能力,低于10%則療效不佳。
實施例九
本實施例提供了一種制備和觀測花形載體顆粒內部孔結構的方法,包括如下步驟:將50克超飽和溶液法制備的不定形乳糖微粒與600ml乙醇混合,攪拌8分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為10微米的花形糖類載體;用共聚焦離子切割該載體顆粒后,在sem下觀測。
圖9為本發明實施例九中制備的花粉形糖類載體在切開后的sem掃描電鏡圖,如圖9所示,介孔和大孔可以直接觀測得到,其中較小的孔包括18nm和32nm的介孔,驗證了該花粉形糖類載體的多孔性。
實施例十
本實施例提供了一種制備和測量花形載體顆粒吸附藥物分子前后孔結構變化的方法,包括如下步驟:將50克噴霧干燥制備的不定形甘露醇微粒與800ml乙醇混合,攪拌15分鐘后過濾去除上清液,風干的沉淀顆粒通過氣流分離器分選出中值粒徑為3微米的花形糖類細粉載體;隨后,將市售的沙丁胺醇溶于丙酮,用10份花形糖類細粉載體進行60分鐘的溶液吸附,離心后風干;用氣體吸附儀對吸附和未吸附沙丁胺醇的花形糖類細粉載體進行測量,得出孔結構變化表征數據。
圖10為本發明實施例十中制備的花粉形糖類載體在吸附藥物分子后的微、介孔結構變化圖,如圖10所示,在吸附藥物分子后,花粉形糖類載體的微孔和介孔數有所下降,且bet孔表面積從60m2/g下降到了10m2/g,說明藥物分子被吸附在納米孔結構中了。
值得說明的是,所述糖類粗粉載體和/或糖類細粉載體采用制備的花粉形糖類載體微粒,所述花粉形糖類載體微粒通過溶液重結晶過程制備,尺寸可控制在1-100μm,在此范圍對應的bet孔表面積為10-60m2/g,表面粗糙,外觀類似花粉形(或描述為花形、花球形、糙面球形、毛球形、齒面顆粒等),切開顆粒觀察到內部具有多孔結構。
在實施例描述的溶液重結晶過程中,優選采用的溶劑為乙醇(酒精),結晶析出的粉末微粒尺寸為1-100μm,在過濾后通過吹氣風干,然后用氣流分離器分選出不同形貌和粒徑規格的粉末微粒,得到花粉形糖類載體微粒。應當說明的是,溶液重結晶即將非定形態(通過超飽和瞬間析出或噴霧干燥制備)的糖類物質在有機溶劑中進行重結晶,可選用多種不溶解糖類物質的有機溶劑,考慮到低毒性和價格,優選乙醇(酒精),穩定后(15分鐘以上)分離獲得粉末微粒,根據《水熱結晶學》(施爾畏等著,科學出版社2004年出版)記載,粉末微粒的大小受結晶過程的濃度、溫度、攪拌速度等因素控制,具體條件參數在實施例中說明,且考慮到吸入劑載體設計,如前所述,糖類粗粉載體的尺寸為10-100μm、糖類細粉載體的尺寸為1-10μm。為防止過熱造成形貌變化,干燥粉末微粒優選吹氣風干,同時,不同形貌和粒徑規格的顆粒其隨氣體運動的慣性不同,氣流分離器用來分離得到所需的花粉形糖類載體微粒。
在實施例描述的三元混合過程中,首先,使用糖類細粉載體0-20份,有效藥物成分0.01-2份,混合或吸附時間為5-60分鐘;隨后,使用糖類粗粉載體0-20份,糖類細粉載體0-20份,混合或吸附時間為5-60分鐘;將上述有效藥物成分、糖類粗、細粉載體三元混合的時間為5-60分鐘。應當說明的是,糖類細粉載體可僅作為三元混合系統的調節物質,也可作為藥物分子的吸附劑,每步的混合時間均在5-60分鐘,更短時間混合會造成混合不充分、聚集效果不好,混合時間過長則會造成藥物和載體的解聚,也沒有必要。
對于實施例中使用的藥品和載體:一方面,所述的有效藥物成分為包括m-受體拮抗劑(優選為噻托溴銨、溴化異丙托品)、β2-受體激動劑(優選為沙美特羅、沙丁胺醇)、皮質激素劑(優選為布地奈德、氟替卡松)、多肽及蛋白藥物(優選胰高血糖素、胰島素、降鈣素、多粘菌素、白介素、蛋白酶抑制劑、細胞刺激因子、脫氧核糖核酸酶、白蛋白)、氨基酸、福米特羅、羥丙茶堿、氟尼縮松、抗腫瘤藥物、二羥丙茶堿、倍氯米松、特布他林、氨茶堿、茶堿、酚丙喘寧、丙卡特羅、曲安縮松及其衍生物在內的一種或多種混合藥物。應當說明的是,以上藥物均為干粉吸入劑中作為有效藥物成分的物質,本發明所述的有效藥物成分包括但不限于以上舉例,以上藥物成分通過物理方式與載體混合,不涉及特殊要求的工藝,其中,m-受體拮抗劑(優選為噻托溴銨、溴化異丙托品)、β2-受體激動劑(優選為沙美特羅、沙丁胺醇)、皮質激素劑(優選為布地奈德、氟替卡松)、氨基酸、福米特羅、羥丙茶堿、氟尼縮松、抗腫瘤藥物、二羥丙茶堿、倍氯米松、特布他林、氨茶堿、茶堿、酚丙喘寧、丙卡特羅、曲安縮松及其衍生物可通過在有機溶液中物理吸附法被細粉載體吸附,或物理研磨后直接混合,而多肽及蛋白藥物(優選胰高血糖素、胰島素、降鈣素、多粘菌素、白介素、蛋白酶抑制劑、細胞刺激因子、脫氧核糖核酸酶、白蛋白)由于不能用有機溶劑溶劑,只能采用物理研磨后直接混合的方式。另一方面,所述糖類細粉載體、所述糖類粗粉載體和所述花粉形糖類載體的材料為包括但不限于乳糖、棉子糖、海藻糖、葡萄糖、蔗糖、赤蘚糖醇、甘露醇、木糖醇、山梨醇、右旋糖苷、環糊精在內的一種或多種可食用材料。應當說明的是,以上糖類物質為干粉吸入劑中作為載體或藥物吸附載體的物質,通過本發明所述的溶液重結晶過程制備得到對應的花粉形糖類載體微粒,而乳糖是目前fda唯一授權安全載體,優選采用乳糖作為載體,其他材料由于也是糖類物質,也是可以作為藥用載體的,但還沒有相關批文出臺。
綜上,采用實施例提供的配合花粉形糖類載體的干粉吸入劑的制備方法,通過溶液重結晶過程制備得到花粉形糖類載體微粒,利用三元混合系統穩定藥物傳輸能力,制備得到的干粉吸入劑其氣體流動性、穩定性、藥效、實用性更佳。
下面結合具體實施例對本發明提供的配合花粉形糖類載體的干粉吸入劑的使用方法作進一步說明。
實施例十一
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的使用方法,包括如下步驟:將配合花粉形糖類載體的干粉吸入劑裝入吸入器中,在進一步實施方式中,使用吸入器吸入給藥時,每吸的單位給藥計量為10mg,給藥3次。
為驗證給藥方法的實施例提供的配合花粉形糖類載體的干粉吸入劑的功效,圖11為本發明實施例十一中配合花粉形糖類載體的干粉吸入劑,對比配合常規一水乳糖載體的干粉吸入劑,在呼吸道模擬模型中的顆粒傳輸測試圖。
如圖11所示,在30l/min的吸入速度下,配合花粉形糖類載體的干粉吸入劑更能隨氣體通過彎道,這時由于花粉形外貌和大的接觸面積使其在靠近呼吸道壁的時,受到更大的側風壓力,從而改變行進方向;而配合常規一水乳糖載體的干粉吸入劑則慣性較大,容易直接沖到呼吸道壁上,導致撞擊沉積,從而影響藥效。
實施例十二
本實施例提供了一種配合花粉形糖類載體的干粉吸入劑的使用方法,包括如下步驟:將制備的配合花粉形糖類載體的干粉吸入劑裝入吸入器用膠囊中,在進一步實施方式中,使用吸入器吸入給藥時,每膠囊的單位給藥計量為50mg,給藥一次。
為驗證本實施例給藥方法的實施例提供的配合花粉形糖類載體的干粉吸入劑的功效,圖12為本發明實施例十二中制備的配合常規一水乳糖載體的干粉吸入劑和配合粗、細粉花粉形糖類載體的干粉吸入劑在肺部模擬模型中的藥物沉積測試比對圖,及配合常規一水乳糖載體或花粉形載體的干粉吸入劑的sem掃描電鏡圖。
如圖12所示,配合細粉花粉形糖類載體的干粉吸入劑能更深入的進入肺部,達到肺泡,其次是配合粗粉花粉形糖類載體的干粉吸入劑,而配合常規一水乳糖載體的干粉吸入劑由于具有更高的撞擊、沉降沉積的可能性,從而較難達到肺部深處;此外,sem掃描電鏡圖對比了配合常規一水乳糖載體或花形載體的干粉吸入劑的形貌,滿足本發明花粉形的外貌設定。
還需要說明的是,根據干粉吸入器的設計,有瓶裝型吸入器和膠囊型吸入器等品種,瓶裝型吸入器的給藥量受按壓噴霧量控制,膠囊型吸入器的給藥量受單位膠囊中裝載的粉末量控制,優選的單位給藥計量為10-50mg,單次給藥量低于10mg則給藥太少,療效太低,需要多次給藥;單次給藥量高于50mg則每吸粉末量太多,容易造成浪費和呼吸不適。
盡管上面已經示出和描述了本發明的實施例,可以理解的是,上述實施例是示例性的,不能理解為對本發明的限制,本領域的普通技術人員在本發明的范圍內可以對上述實施例進行變化、修改、替換和變型,而并不使相應技術方案的本質脫離本發明各實施例技術方案的范圍,其均應涵蓋在本發明的權利要求和說明書的范圍當中。
- 還沒有人留言評論。精彩留言會獲得點贊!